Resumos
As enzimas proteolíticas termoestáveis produzidas por microrganismos do gênero Bacillus possuem grande importância comercial, sendo sua aplicação predominante (35%) na indústria de detergentes. Neste trabalho, foi avaliada a produção de proteases pelo termofílico Bacillus sp. SMIA-2, utilizando-se substratos de baixo custo. A fim de verificar a utilidade da protease para aplicações industriais, a estabilidade e a atividade da enzima a diferentes valores de pH e temperatura foram também estudadas. A atividade da protease secretada por Bacillus sp. SMIA-2 em culturas submersas contendo 0,5% (m/v) de pectina de maçã, 0,1% (m/v) de proteínas do soro e 0,3% (m/v) de água de maceração de milho foi máxima após 24 h de incubação da cultura, com níveis de 54,3 U.mg-1 Proteína. A redução na concentração da pectina para 0,3% (m/v) e o aumento nos níveis das proteínas do soro para 0,3% (m/v) no meio de cultura aumentaram a produção da protease, que alcançou sua máxima atividade em 30 h, com níveis de 72,2 U.mg-1 Proteína. Estudos sobre a protease revelaram que as suas características mais importantes foram a alta temperatura ótima para atividade da enzima (70 °C) e a alta estabilidade em uma grande faixa de pH. A protease reteve em torno de 80% de sua atividade original quando incubada à temperatura ambiente por 2 h na faixa de pH entre 6,0 e 12,0. Essas propriedades constituem importantes vantagens para um possível uso da enzima em indústrias de detergentes.
Proteases; Bacillus sp.; Bactéria termofílica; Detergentes
The thermostable proteolytic enzymes produced by the genus Bacillus are commercially very important, being predominantly applied (35%) in detergents. In this work the production of proteases by a thermophilic Bacillus sp. SMIA-2 using low-cost substrates was evaluated. In order to assess the use of the protease for industrial use, the stability of the enzyme activity at different pH values and temperatures was also studied. The protease activity secreted by Bacillus sp. SMIA-2 in submerged cultures containing 0.5% (w/v) apple pectin, 0.1% (w/v) whey protein concentrate and 0.3% (w/v) corn steep liquor reached a maximum after 24 h, with levels of 54.3 U.mg-1 protein. A reduction in the pectin concentration to 0.3% (w/v) and increase in the whey protein levels to 0.3% (w/v) in the culture medium improved the protease production, which reached a maximum after 30 h, with levels of 72.2 U.mg-1 protein. Studies on the characterization of the protein revealed that the most important kinetic properties of the enzyme were the high optimal temperature (70 °C) and high stability in a very broad pH range. The protease retained about 80% of its original activity when incubated at room temperature for 2 h in a pH range between 6.0 - 12.0. These properties represent important advantages for the possible use of the enzyme in detergent industries.
Proteases; Bacillus sp.; Thermophilic bacterium; Detergents
Nota Científica: Utilização da pectina, proteínas do soro de queijo e água de maceração de milho para a produção de proteases por Bacillus sp. termofílico
Scientific Note: Use of pectin, whey protein and corn steep liquor for the production of protease by thermophilic Bacillus sp.
Silvania Alves LadeiraI; Andréia Boechat DelatorreI; Marcela Vicente Vieira AndradeI; Meire Lelis Leal MartinsII, * * Autor Correspondente | Corresponding Author
IUniversidade Estadual do Norte -Fluminense Darcy Ribeiro (UENF) Centro de Ciências e Tecnologias -Agropecuárias (CCTA) Laboratório de Tecnologia de Alimentos (LTA) Campos dos Goytacazes/RJ - Brasil e-mail: silvanialadeira@hotmail.com andreiadelatorre@hotmail.com marcelaandrade14@yahoo.com.br
IIUniversidade Estadual do Norte -Fluminense Darcy Ribeiro (UENF) Centro de Ciências e Tecnologias -Agropecuárias (CCTA) Laboratório de Tecnologia de Alimentos (LTA) Av. Alberto Lamego, 2000 Parque Califórnia CEP: 28013-602 Campos dos Goytacazes/RJ - Brasil e-mail: meire@uenf.br
RESUMO
As enzimas proteolíticas termoestáveis produzidas por microrganismos do gênero Bacillus possuem grande importância comercial, sendo sua aplicação predominante (35%) na indústria de detergentes. Neste trabalho, foi avaliada a produção de proteases pelo termofílico Bacillus sp. SMIA-2, utilizando-se substratos de baixo custo. A fim de verificar a utilidade da protease para aplicações industriais, a estabilidade e a atividade da enzima a diferentes valores de pH e temperatura foram também estudadas. A atividade da protease secretada por Bacillus sp. SMIA-2 em culturas submersas contendo 0,5% (m/v) de pectina de maçã, 0,1% (m/v) de proteínas do soro e 0,3% (m/v) de água de maceração de milho foi máxima após 24 h de incubação da cultura, com níveis de 54,3 U.mg-1 Proteína. A redução na concentração da pectina para 0,3% (m/v) e o aumento nos níveis das proteínas do soro para 0,3% (m/v) no meio de cultura aumentaram a produção da protease, que alcançou sua máxima atividade em 30 h, com níveis de 72,2 U.mg-1 Proteína. Estudos sobre a protease revelaram que as suas características mais importantes foram a alta temperatura ótima para atividade da enzima (70 °C) e a alta estabilidade em uma grande faixa de pH. A protease reteve em torno de 80% de sua atividade original quando incubada à temperatura ambiente por 2 h na faixa de pH entre 6,0 e 12,0. Essas propriedades constituem importantes vantagens para um possível uso da enzima em indústrias de detergentes.
Palavras-chave: Proteases; Bacillus sp.; Bactéria termofílica; Detergentes.
SUMMARY
The thermostable proteolytic enzymes produced by the genus Bacillus are commercially very important, being predominantly applied (35%) in detergents. In this work the production of proteases by a thermophilic Bacillus sp. SMIA-2 using low-cost substrates was evaluated. In order to assess the use of the protease for industrial use, the stability of the enzyme activity at different pH values and temperatures was also studied. The protease activity secreted by Bacillus sp. SMIA-2 in submerged cultures containing 0.5% (w/v) apple pectin, 0.1% (w/v) whey protein concentrate and 0.3% (w/v) corn steep liquor reached a maximum after 24 h, with levels of 54.3 U.mg-1 protein. A reduction in the pectin concentration to 0.3% (w/v) and increase in the whey protein levels to 0.3% (w/v) in the culture medium improved the protease production, which reached a maximum after 30 h, with levels of 72.2 U.mg-1 protein. Studies on the characterization of the protein revealed that the most important kinetic properties of the enzyme were the high optimal temperature (70 °C) and high stability in a very broad pH range. The protease retained about 80% of its original activity when incubated at room temperature for 2 h in a pH range between 6.0 - 12.0. These properties represent important advantages for the possible use of the enzyme in detergent industries.
Key words: Proteases; Bacillus sp.; Thermophilic bacterium; Detergents.
1 Introdução
Proteases constituem um dos mais importantes grupos de enzimas industriais e têm aplicação em diferentes indústrias, como de alimentos, têxtil, farmacêutica e de detergentes (SINGH et al., 2003; MAURER, 2004; JOO e CHANG, 2005). A venda dessas enzimas representa cerca de 65% do total de enzimas comercializadas no mundo (VISHWANATHA et al., 2010).
Proteases termoestáveis produzidas por microrganismos do gênero Bacillus são o grupo mais importante de enzimas produzidas comercialmente (ASHGER, 2007). Os microrganismos desse gênero são capazes de se desenvolver em condições extremas de temperatura e pH, o que permite a produção dessas enzimas em uma ampla faixa de pH e temperatura (WANG et al., 2007). A maior parte das bactérias pertencentes ao gênero Bacillus sp. apresenta uma variedade de sistemas de enzimas hidrolíticas e são capazes de utilizar substâncias orgânicas típicas de resíduos. Alem disso, com exceção do grupo Bacillus cereus, são saprófitas inofensivos, que não produzem toxinas e são incluídos no grupo de organismos geralmente reconhecidos como seguros (MAHMOOD et al., 1998).
Apesar das vantagens que as enzimas de microrganismos termofílicos do gênero Bacillus sp. oferecem para o uso rotineiro na indústria, a aplicação biotecnológica desses microrganismos tem sido muito limitada até agora. As razões para essa contradição são muitas, mas a principal delas está relacionada com o escasso número de linhagens termofílicas para a pesquisa de enzimas termoestáveis específicas, disponíveis em coleções (AQUINO, 2003).
O elevado custo da produção de enzimas é o principal obstáculo para sua aplicação industrial (GODFREY e WEST, 1996). Considerando-se que o substrato para o desenvolvimento desses microrganismos corresponde à faixa de 30 a 40% do custo da produção de enzimas em escala industrial (JOO e CHANG, 2005), a pesquisa de metodologias e substratos alternativos é importante para a indústria (ASHIS et al., 2008; DIAS et al., 2008; PELIZER et al., 2007). Assim, este estudo avaliou a produção de proteases por Bacillus sp. termofílico SMIA-2, cultivado em pectina, proteínas do soro de leite e água de maceração de milho. Algumas propriedades das proteases, como estabilidade e atividade a diferentes valores de temperatura e pH foram também determinadas, a fim de se avaliar o potencial das enzimas para aplicações industriais.
2 Material e métodos
2.1 Organismo e condições da cultura
O microrganismo usado neste estudo foi uma bactéria termofílica, Bacillus sp., cepa SMIA-2, previamente isolada de amostras de solo coletadas na cidade de Campos dos Goytacazes-Rio de Janeiro, Brasil (NUNES e MARTINS, 2001).
O meio de cultura utilizado para a produção da protease continha (g.L-1): pectina de maçã - 5,0; concentrado de proteínas do soro de queijo - 1,0; água de maceração de milho - 3,0; KCl - 0,3; MgSO4 - 0,5; K2HPO4 - 0,87; CaCl2 - 0,29; ZnO - 2,03 × 10-3 ; FeCl3.6H2O - 2,7 × 10 -2; MnCl2.4H2O - 1,0 × 10 -2; CuCl2.2H2O - 8,5 × 10 -4; CoCl2.6H2O - 2,4 × 10 -3; NiCl3.6H2O - 2,5 × 10 -4 e H3BO3 - 3,0 × 10 -4 . Posteriormente, esse meio foi modificado, reduzindo-se a concentração da pectina de maçã para 3,0 g.L-1 e aumentando a concentração das proteínas do soro para 3,0 g.L-1.
O pH dos meios foi ajustado para 7,0 com NaOH 1,0 M e estes foram esterilizados em autoclave a 121 + 2 °C por 15 min.
O meio de produção (50 mL em frascos Erlenmeyer de 250 mL) foi inoculado com 0,1% (m/v) de inóculo e incubada a 50 °C em um agitador Thermo Forma Orbital Shaker (Ohio, USA) operado a 150 rpm. A intervalos de tempo determinados, foram retirados frascos em triplicata para medida do pH e da densidade ótica a 600 nm, com a utilização de um espectrofotômetro Hitachi modelo U-2000.
2.2 Ensaio enzimático
Para a remoção das células, o meio de cultura foi centrifugado a 15.500 g por 15 min a 4 °C, em uma centrífuga modelo HERMLEZ 382 K (Wehingen, Germany), e o sobrenadante livre de células foi utilizado para dosagem da atividade da enzima.
A atividade enzimática foi determinada em triplicata pela quantificação de peptídeos solúveis em ácido tricloroacético (TCA) 15% (JANSEN et al., 1994). O substrato utilizado para essa determinação foi uma solução de azocaseína 0,2% (m/v), preparada em tampão Tris/HCl (pH 8,5; 0,2 M). Uma mistura contendo 0,5 mL do extrato enzimático e 1,0 mL do substrato foi incubada em banho-maria a 70 °C por 10 min. A reação foi paralisada pela adição de 0,5 mL de TCA e a solução centrifugada a 15.000 g por 5 min a 4 °C. O mesmo procedimento foi realizado com o branco, exceto que o TCA foi adicionado antes do extrato enzimático. Uma unidade foi definida como a quantidade da enzima requerida para produzir um aumento na absorvância a 420 nm igual a 0,1 em 60 min. A concentração de proteínas foi determinada pelo método descrito por Peterson (1977).
2.3 Efeito do pH na atividade e na estabilidade da protease
A influência do pH sobre a atividade da protease foi avaliada na faixa de 6,0 a 12,0, com intervalo de 0,5 unidade. Para o preparo do substrato, foi utilizada uma mistura tamponante contendo os seguintes tampões (0,2 M): fosfato de sódio, pH 6,0-8,0; Tris/HCl, pH 8,5-10,0, e glicina-NaOH, pH 10,5-12,0.
O pH ótimo foi determinado utilizando-se o substrato (azocaseína 0,2% m/v) preparado nas soluções tampões com diferentes valores de pH e medindo-se a atividade enzimática conforme descrito anteriormente.
A estabilidade da protease a diferentes valores de pH foi avaliada incubando-se o extrato enzimático nos tampões já descritos, sem o substrato, por 2 h à temperatura ambiente. Após esse tratamento, a atividade residual da protease foi determinada segundo descrito anteriormente.
2.4 Efeito da temperatura na atividade e na estabilidade da protease
A determinação da temperatura ótima para a atividade enzimática foi alcançada realizando-se o ensaio enzimático descrito anteriormente em temperaturas que variaram de 40 a 100 °C, com intervalos de 10 °C.
A estabilidade térmica foi avaliada incubando-se a enzima em temperaturas que variaram de 40 a 100 °C, com intervalos de 10 °C por 2 h. Posteriormente, para cada temperatura, a atividade residual foi analisada à temperatura ótima da enzima, determinada anteriormente (NASCIMENTO e MARTINS, 2004).
O efeito do íon Ca+2 sobre a atividade da enzima foi verificado incubando-se o extrato enzimático a 60 °C na presença e na ausência de CaCl2 (10 mM) por 3 h. Após intervalos de 15 min, foram retiradas amostras em triplicata para a determinação da atividade enzimática residual, conforme descrito anteriormente.
3 Resultados e discussão
3.1 Perfil do crescimento do microrganismo e atividade proteásica
O crescimento do Bacillus sp. SMIA-2 e a atividade da protease em meio líquido contendo pectina de maçã (0,5% m/v), proteínas do soro (0,1% m/v) e água de maceração de milho (0,3% m/v) em função do tempo de fermentação são mostrados na Figura 1. A produção enzimática teve início após 6 h de incubação da cultura e foi aumentando com o desenvolvimento microbiano, atingindo valor máximo após 24 h, com níveis de 54,3 U.mg-1 proteína. De acordo com Ward (1985), os microrganismos do gênero Bacillus geralmente produzem maiores quantidades de proteases ao final da fase exponencial de crescimento, acrescentando que a função dessas enzimas ainda não é bem conhecida, mas sua produção está correlacionada com uma elevada taxa de renovação de proteínas durante a esporulação.
Após alcançar o valor máximo, a atividade da protease decresceu, atingindo cerca de 58 e 10% da atividade máxima em 42 e 54 h de crescimento, respectivamente. Esses resultados sugerem que tal comportamento da protease não é satisfatório, uma vez que poderia comprometer a sua produção em larga escala, pois o período em que essa enzima permaneceu estável foi curto. Esse processo de inativação, que é característico na produção de proteases por microrganismos, torna difícil a produção enzimática em larga escala, em razão da dificuldade de se isolar a enzima em sua atividade máxima (NASCIMENTO et al., 2007). Vários pesquisadores conseguiram aumentar a estabilidade da protease por meio de modificações no meio de crescimento, como o aumento da concentração do cálcio, a remoção de agentes quelantes e a diminuição da concentração de fosfato de potássio, sem, contudo, prejudicar o crescimento do microrganismo (BAKHTIAR et al., 2002; GHORBEL et al., 2003; AZEREDO et al., 2004).
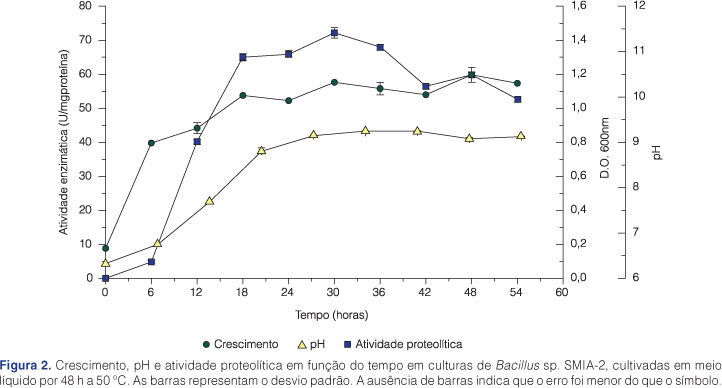
A redução da concentração da pectina de maçã de 0,5% (m/v) para 0,3% (m/v) e o aumento da concentração das proteínas do soro de 0,1% (m/v) para 0,3% (m/v) promoveram um acréscimo nos valores da atividade da protease a partir de 18 h de incubação da cultura (Figura 2). Além disso, a enzima foi estável entre 18 e 36 h de incubação da cultura e, em 54 h, foi observada uma redução de apenas 30% na atividade da enzima, o que é de grande importância para a sua produção em larga escala. Tanto a água de maceração do milho, resultante do processamento dos grãos de milho, como as proteínas do soro, extraídas durante o processo de fabricação de queijo, são subprodutos ricos em aminoácidos, peptídeos e minerais, e são de baixo custo.
Um decréscimo da densidade ótica da cultura foi observado quando o meio foi modificado. A máxima densidade ótica obtida no meio anterior foi 1,8 com 24 h de incubação do microrganismo, enquanto que, no meio modificado, a máxima densidade ótica foi de 1,2 com 30 h de incubação da cultura. Dessa maneira, as condições que favoreceram o crescimento celular foram diferentes daquelas que estimularam a produção da protease, demonstrando a natureza complexa do processo bioquímico envolvido na obtenção dessa enzima.
O pH do meio aumentou com o início do desenvolvimento microbiano e da produção da protease, provavelmente em função do consumo de nitrogênio orgânico, como aminoácidos e peptídeos, e estabilizou prestes a atingir o valor de 9,0 após a enzima alcançar sua máxima atividade. Por causa dessa relação entre o pH e a síntese de proteases, a variação do pH pode ser utilizada para fornecer informações importantes sobre a produção da enzima, como o início e o final de sua síntese.
3.2 Efeito do pH na atividade e na estabilidade da protease
A protease foi ativa em uma ampla faixa de pH, apresentando máxima atividade (100% = 62,8 U.mg-1 proteína) em torno de pH 8,5 (Figura 3). De acordo com Beg e Gupta (2003), as proteases comerciais de origem microbiana geralmente possuem atividade ótima na faixa de pH que varia de 8,0 a 12,0, o que as torna de grande interesse para utilização em formulações de detergentes, em função do pH alcalino desses produtos.
Em relação à estabilidade ao pH, a enzima foi estável em uma ampla faixa de pH, mantendo aproximadamente 85% de sua atividade máxima quando incubada por 2 h na faixa de pH compreendida entre 6,0 e 12 (Figura 3). Estes resultados possibilitam a aplicação da enzima em diversos setores industriais, incluindo a indústria de detergentes. O valor do pH de atuação de uma enzima é um importante parâmetro para se determinar a viabilidade de sua aplicação em um dado detergente. A atividade catalíticos em valores elevados de pH (10,0-11,0), ou mesmo moderadamente elevados (8,0-9,0), indica que a enzima é bastante viável para ser utilizada em detergentes. A Alcalase®, enzima muito utilizada na indústria de detergentes, possui pH ótimo de atuação na faixa de 8,0 a 9,0 (GODFREY e WEST, 1996).
3.3 Temperatura ótima e estabilidade térmica
A atividade da enzima aumentou com a elevação da temperatura, atingindo seu valor máximo a 70 °C, conforme mostrado na Figura 4. Nas temperaturas de 80 e 90 °C, a enzima apresentou 65 e 35% de sua atividade máxima, respectivamente. Em Bacillus licheniformis SMI 4. C.1., a melhor atividade de protease foi observada a 70 °C (MAURER, 2004).
A protease manteve em torno de 80% de sua atividade quando incubada por 2 h a 60 °C e reduziu drasticamente sua estabilidade a temperaturas mais altas. A incubação da enzima a 90 e 100 °C por 2 h resultou na completa inibição da atividade da protease.
Vários pesquisadores demonstraram que a adição de metais ao extrato bruto de algumas enzimas promove o aumento da sua termoestabilidade (JOO et al., 2002; GHORBEL et al., 2003; SINGH et al., 2003). De fato, foi observado, neste trabalho, que a incubação da enzima a 60 °C na presença de 10 mM CaCl2 aumentou consideravelmente a sua atividade (Figura 5). Ghorbel et al. (2003) verificaram um aumento na termoestabilidade de uma protease produzida por Bacillus cereus BG1 quando incubada na temperatura de 60 °C em presença de Ca+2. De acordo com os autores, o papel do Ca+2 na estabilização da protease pode ser explicado pela grande força de interação entre as moléculas de proteína, por causa da ligação desses íons no sítio ativo da mesma, impedindo sua desnaturação.
4 Conclusões
Os resultados mostraram o potencial do uso das proteínas do soro e da água de maceração de milho como meio de cultura para a produção de proteases por Bacillus sp SMIA-2. A enzima mostrou atividade ótima à temperatura de 70 °C e pH 8,5, e foi estável na faixa de pH de 6,0 a 12,0. Essas propriedades constituem importantes vantagens para um possível uso da enzima na indústria de detergentes.
Agradecimentos
Os autores agradecem ao CNPq (Conselho Nacional de Desenvolvimento Científico e Tecnológico), pelo apoio financeiro, e à CAPES (Coordenação de Aperfeiçoamento de Pessoal de Nível superior), pela concessão de Bolsa de Mestrado.
Recebido | Received: 29/06/2009
Aprovado | Approved: 04/10/2011
Publicado | Published: mar./2012
- AQUINO, A. C. M. M.; JORGE, J. A.; TERENZI, H. F.; POLIZELI, M. L. T. M. Studies on a thermostable α-amylase from the thermophilic fungus Scytalidium thermophilum. Applied Microbiology and Biotechnology, Heidelberg, v. 61, n. 3, p. 323-328, 2003. http://dx.doi.org/10.1007/s00253-003-1290-y
- ASHIS, K.; MUKHERJEE, H. A.; SUDHIR, K. R. Production of alkaline protease by a thermophilic Bacillus subtilis under solid-state fermentation (SSF) condition using Imperata cylindrical grass and potato peel as low-cost medium: Characterization and application of enzyme in detergent formulation. Biochemical Engineering Journal, London, v. 39, n. 2, p. 353-361, 2008. http://dx.doi.org/10.1016/j.bej.2007.09.017
- ASHGER, M.; ASAD, M. J.; RAHMAN, S. U.; LEGGE, R. L. A thermostable α-amylase from a moderately thermophilic Bacillus subtilis strain for starch processing. Journal of Food Engineering, New York, v. 79, n. 3, p. 950-955, 2007. http://dx.doi.org/10.1016/j.jfoodeng.2005.12.053
- AZEREDO, L. A. I.; FREIRE, D. M. G.; SOARES, R. M. A.; LEITE, S. G. F.; COELHO, R. R. R. Production and partial characterization of thermophilic proteases from Streptomyces sp. isolated from Brazilian cerrado soil. Enzyme and Microbial Technology, New York, v. 34, p. 354-358, 2004. http://dx.doi.org/10.1016/j.enzmictec.2003.11.015
- BAKHTIAR, S.; ANDERSON, M. M.; GESSESSE, A.; MATTIASON, B.; KAUL, R. H. Stability characteristics of the Calcium-Independent alkaline protease from Nesterenkonia sp. Enzyme and Microbial Technology, New York, v. 32, n. 5, p. 525-531, 2002. http://dx.doi.org/10.1016/S0141-0229(02)00336-8
- BEG, Q. K.; GUPTA, R. Purification and characterization of an oxidation-stable, thiol-dependent serine alkaline protease from Bacillus mojavensis. Enzyme and Microbial Technology, New York, v. 32, n. 2, p. 294-304, 2003. http://dx.doi.org/10.1016/S0141-0229(02)00293-4
- DIAS, D. R.; VILELA, D. M.; SILVESTRE, M. P. C.; SCHWAN, R. F. Alkaline protease from Bacillus sp. isolated from coffee bean grown on cheese whey. World Journal of Microbiology and Biotechnology, Oxford, v. 24, n. 9, p. 2027-2034, 2008. http://dx.doi.org/10.1007/s11274-008-9706-6
- GHORBEL, B.; KAMOUN, A. S.; NASRI, M. Stability studies of protease from Bacillus cereus BG1. Enzyme and Microbial Technology, New York, v. 32, n. 5, p. 513-518, 2003. http://dx.doi.org/10.1016/S0141-0229(03)00004-8
- GODFREY, T.; WEST, S. Industrial Enzimology 2. ed. Stockton Press, 1996. 609 p.
- JANSEN, P. H.; PEEK, K.; MORGAN, H. W. Effect of culture conditions on the production of a extracellular proteinase by Thermus sp. Rt41A. Applied Microbiology and Biotechnology, Heidelberg, v. 41, n. 4, p. 400-406, 1994. http://dx.doi.org/10.1007/BF00939027
- JOO, H.S; CHANG, C.S. Production of protease from a new Alkalophilic Bacillus sp. I-312 grow on soybean meal: optimization and some properties. Process Biochemistry, Grã Bretanha, v. 40, n. 3-4, p. 1263-1270, 2005. http://dx.doi.org/10.1016/j.procbio.2004.05.010
- JOO, H. S.; KUMAR, C. G.; PARK, G. C.; KIM, T. K.; PAIK, S. R.; CHANG, C. S. Otimization of the production of an extracellular alkaline protease from Bacillus horikoshii. Process Biochemistry, Grã Bretanha, v. 38, n. 2, p. 155-159, 2002. http://dx.doi.org/10.1016/S0032-9592(02)00061-4
- MAHMOOD, A. U; GREENMAN, J.; SCRAGG, A. H. Orange and potato peel extracts: Analysis and use as Bacillus substrates for the production of extracellular enzymes in continuous culture. Enzyme Microbial and Technology, New york, v. 22, n. 2, p. 130-137, 1998. http://dx.doi.org/10.1016/S0141-0229(97)00150-6
- MAURER, K. H. Detergents proteases. Current Opinion in Biotechnology, London, v.15, n. 3, p. 330-334, 2004. http://dx.doi.org/10.1016/j.copbio.2004.06.005
- NASCIMENTO, W. C. A.; MARTINS, M. L. L. Production and properties of an extracellular protease from thermophilic Bacillus sp. Brazilian J of Microbiology, São Paulo, v. 35, n. 1-2, p. 91-96, 2004. http://dx.doi.org/10.1590/S1517-83822004000100015
- NASCIMENTO, W. C. A.; CARVALHO, R. V.; SILVA, C. R.; MARTINS, M. L. L. Otimização de um meio de cultura para produção de proteases por um Bacillus sp. Termofílico. Ciência e Tecnologia de Alimentos, São Paulo, v. 27, n. 2, p. 417-421, 2007. http://dx.doi.org/10.1590/S0101-20612007000200035
- NUNES, A. S.; MARTINS, M. L. L. Isolation, properties and kinetics of growth of a thermophilic Bacillus. Brazilian Journal of Microbiology, São Paulo, v. 32, n. 3, p. 271-275, 2001. http://dx.doi.org/10.1590/S1517-83822001000400003
- PELIZER, L. H.; PONTIERI, M. H.; MORAES, I. O. Utilização de resíduos agro-industriais em processos biotecnológicos com perspectiva de redução do impacto ambiental. Journal of Technology Management & Innovation, Santiago, v. 2, n. 1, p. 118-127, 2007.
- PETERSON, G. L. A simplification of the protein assay method of Lowry et al. which is more generally applicable. Analytical Biochemistry, New York, v. 83, n. 2, p. 346-356, 1977. http://dx.doi.org/10.1016/0003-2697(77)90043-4
- SINGH, J.; VOHRA, R. M.; SAHOO, D. K. Enhanced production of alkaline protease by Bacillus sphaericus using fed-batch culture. Process Biochemistry, Grã Bretanha, v. 39, n. 9, p. 1093-1098, 2003. http://dx.doi.org/10.1016/S0032-9592(03)00217-6
- VISHWANATHA, K. S.; RAO, A. G. A.; SINGH, S. A. Acid protease production by solid-state fermentation using Aspergillus oryzae MTCC 5341: optimization of process parameters. Journal of Industrial Microbiology and Biotechnology, Heidelberg, v. 37, p. 129-138, 2010. http://dx.doi.org/10.1007/s10295-009-0654-4
- WANG, Q.; FAN, X.; HUAB, Z.; CHENB, J. Optimizing bioscouring condition of cotton knitted fabrics with an alkaline pectinase from Bacillus subtilis WSHB04-02 by using response surface methodology. Biochemical Engineering Journal, London, v. 34, n. 1, p. 107-113, 2007. http://dx.doi.org/10.1016/j.bej.2006.11.004
- WARD, O. P. Proteolytic enzymes. Comprehensive Biotechnology, Oxford, v. 3, n. 7, p. 789-818. 1985.
Datas de Publicação
-
Publicação nesta coleção
29 Mar 2012 -
Data do Fascículo
Mar 2012
Histórico
-
Recebido
29 Jun 2009 -
Aceito
04 Out 2011