Resumos
O objetivo deste trabalho foi analisar os efeitos da infecção causada pelo Toxoplasma gondii sobre a parede do duodeno de gatos. Foram utilizados seis gatos (Felis catus), com cerca de três meses de vida, distribuídos aleatoriamente em Grupo controle (G1; n = 3) e Grupo infectado (G2; n = 3). Os animais do G2 receberam, por via oral, 200 cistos teciduais da cepa ME49 (tipo II) do T. gondii. Após 40 dias, os animais foram submetidos à eutanásia, laparotomia e retirada do duodeno, que foi fixado em solução de Bouin e submetido à rotina histológica para obtenção de cortes transversais de 3 µm. Os cortes foram corados com Hematoxilina-Eosina (HE), Azan, Ácido Periódico de Schiff (PAS), Alcian-Blue e Tricrômio de Mallory. Realizou-se uma avaliação qualitativa da parede intestinal e medidas comparativas entre os dois grupos, com relação: à espessura da túnica mucosa, túnica muscular, parede total, altura dos vilos, profundidade das criptas e altura dos enterócitos e seus núcleos. As células caliciformes, os linfócitos intraepiteliais e as células de Paneth foram quantificados. Os resultados mostraram que a infecção levou à atrofia da túnica mucosa, túnica muscular e parede intestinal do duodeno de gatos do G2 (p < 0,05). A altura dos enterócitos apresentou um aumento significativo (p < 0,05) nos animais do G2. Na avaliação qualitativa, as fibras colágenas ocupavam visivelmente uma maior área dos estratos da parede intestinal, o que sugere que estejam aumentadas. Observou-se a redução da secreção de sulfomucinas e o aumento das células de Paneth nesses mesmos animais (p < 0,05).
duodeno; toxoplasmose; epitélio intestinal; histologia; felinos
This paper analyzes the effects of the infection caused by Toxoplasma gondii on the cat duodenal wall. Six cats (Felis catus) with 3-month-old were randomly divided into Control Group (G1; n = 3) and Infected Group (G2; n = 3). The animals from G2 received orarilly 200 T. gondii tissye cysts of ME49-strain (type II). After 40 days, the animals were submitted to euthanasia, laparotomy and had their duodenum removed, fixed in Bouin solution and submitted to histological routine obtaining 3 µm transverse cuts. The cuts were stained with Hematoxylin-Eosin (HE), Azan, Periodic acid - Schiff (PAS), Alcian-Blue, and Mallory trichrome. Qualitative assessment of the intestine wall as well as comparative measurements with respect to the thickness of mucosa, muscle tunic, total wall, the height of the villous, the depth of the crypts, and the height of the enterocytes and their nuclei were carried out. Calciform cells, the intraepithelial lymphocytes, and the Paneth cells were quantified. The results showed that the infection led to the atrophy of the mucosa, muscle tunic, and the intestinal wall of the duodenum of G2 cats (p < 0.05). The enterocytes height presented significant (p < 0.05) increase for G2 animals. According to the qualitative analysis, the collagen fibers were visibly taken a broader area on the intestinal wall layers, what suggests they have increased in size. Decrease in the sulphomucins secretion and the increase of Paneth cells were observed for these animals (p < 0.05).
duodenum; toxoplasmasmosis; intestinal epithelium; histology; felines
ARTIGO COMPLETO
Efeitos da infecção crônica por Toxoplasma gondii sobre a parede intestinal de gatos domésticos
The effects of the infection caused by Toxoplasma gondii on the cat duodenal wall
Juliana Maria da Silva; Aristeu Vieira da Silva; Eduardo José de Almeida Araújo; Débora de Mello Gonçales Sant'Ana
Universidade Paranaense UNIPAR
Autor para correspondência Autor para correspondência: Débora de Mello Gonçales Sant'Ana Mestrado em Ciência Animal, Instituto de Pesquisa, Universidade Paranaense UNIPAR Praça Mascarenhas de Moraes, 4282, 87502-120 Umuarama, PR - Brasil e-mail: debora@unipar.br
RESUMO
O objetivo deste trabalho foi analisar os efeitos da infecção causada pelo Toxoplasma gondii sobre a parede do duodeno de gatos. Foram utilizados seis gatos (Felis catus), com cerca de três meses de vida, distribuídos aleatoriamente em Grupo controle (G1; n = 3) e Grupo infectado (G2; n = 3). Os animais do G2 receberam, por via oral, 200 cistos teciduais da cepa ME49 (tipo II) do T. gondii. Após 40 dias, os animais foram submetidos à eutanásia, laparotomia e retirada do duodeno, que foi fixado em solução de Bouin e submetido à rotina histológica para obtenção de cortes transversais de 3 µm. Os cortes foram corados com Hematoxilina-Eosina (HE), Azan, Ácido Periódico de Schiff (PAS), Alcian-Blue e Tricrômio de Mallory. Realizou-se uma avaliação qualitativa da parede intestinal e medidas comparativas entre os dois grupos, com relação: à espessura da túnica mucosa, túnica muscular, parede total, altura dos vilos, profundidade das criptas e altura dos enterócitos e seus núcleos. As células caliciformes, os linfócitos intraepiteliais e as células de Paneth foram quantificados. Os resultados mostraram que a infecção levou à atrofia da túnica mucosa, túnica muscular e parede intestinal do duodeno de gatos do G2 (p < 0,05). A altura dos enterócitos apresentou um aumento significativo (p < 0,05) nos animais do G2. Na avaliação qualitativa, as fibras colágenas ocupavam visivelmente uma maior área dos estratos da parede intestinal, o que sugere que estejam aumentadas. Observou-se a redução da secreção de sulfomucinas e o aumento das células de Paneth nesses mesmos animais (p < 0,05).
Palavras-chaves: duodeno, toxoplasmose, epitélio intestinal, histologia, felinos.
ABSTRACT
This paper analyzes the effects of the infection caused by Toxoplasma gondii on the cat duodenal wall. Six cats (Felis catus) with 3-month-old were randomly divided into Control Group (G1; n = 3) and Infected Group (G2; n = 3). The animals from G2 received orarilly 200 T. gondii tissye cysts of ME49-strain (type II). After 40 days, the animals were submitted to euthanasia, laparotomy and had their duodenum removed, fixed in Bouin solution and submitted to histological routine obtaining 3 µm transverse cuts. The cuts were stained with Hematoxylin-Eosin (HE), Azan, Periodic acid Schiff (PAS), Alcian-Blue, and Mallory trichrome. Qualitative assessment of the intestine wall as well as comparative measurements with respect to the thickness of mucosa, muscle tunic, total wall, the height of the villous, the depth of the crypts, and the height of the enterocytes and their nuclei were carried out. Calciform cells, the intraepithelial lymphocytes, and the Paneth cells were quantified. The results showed that the infection led to the atrophy of the mucosa, muscle tunic, and the intestinal wall of the duodenum of G2 cats (p < 0.05). The enterocytes height presented significant (p < 0.05) increase for G2 animals. According to the qualitative analysis, the collagen fibers were visibly taken a broader area on the intestinal wall layers, what suggests they have increased in size. Decrease in the sulphomucins secretion and the increase of Paneth cells were observed for these animals (p < 0.05).
Keywords: duodenum, toxoplasmasmosis, intestinal epithelium, histology, felines.
Introdução
O Toxoplasma gondii apresenta um ciclo sexual heteroxeno facultativo (FERREIRA; FORONDA; SCHUMAKER, 2003; BEVERLEY, 1976). As etapas sexuadas ocorrem apenas nos felídeos (hospedeiros definitivos) por meio do ciclo intestinal (DENKERS; GAZZINELLI, 1998; FERREIRA; FORONDA; SCHUMAKER, 2003); já as etapas assexuadas podem ocorrer em todos os animais homeotérmicos (hospedeiros intermediários), por meio do ciclo extraintestinal (BLACK; BOOTHROYD, 2000; BEVERLEY, 1976).
O intestino delgado do gato é um órgão-chave no ciclo de vida do T. gondii (CHAPLIN; SILVA; ARAÚJO, 1991; DUBEY, 1994) e está envolvido com os ciclos intestinal e extraintestinal do parasito (NOGAMI et al., 1998; DENKERS; GAZZINELLI, 1998; FERGUSON et al., 1979). A integridade morfológica e imunológica da barreira intestinal é essencial para que o primeiro tenha o seu desenvolvimento normal e o segundo tenha limitação em sua gravidade (FERGUSON et al., 1979; BEVERLEY, 1976; DAVIS; DUBEY, 1995).
Quando chegam à mucosa intestinal, parasitos enfrentam uma barreira imunológica caracterizada especialmente pela presença da IgA (WERSHIL; FURUTA, 2008), que desempenha um papel importante no combate a infecção oral do T. gondii (BOUT et al., 1999), e uma barreira física formada pelos enterócitos (BARRAGAN; SIBLEY, 2003). Para vencer a barreira física, os parasitos desenvolveram várias estratégias de aderência e invasão dos enterócitos e disseminação além do epitélio (BEVERLEY, 1976; RACHINEL et al., 2004; BARRAGAN; SIBLEY, 2003; BUZONI-GATEL; WERTS, 2006). O ciclo enteroepitelial do T. gondii (fase sexuada) ocorre predominantemente no interior dos enterócitos (BOUT et al., 1999) e mais raramente no interior de células caliciformes de felinos (FREYRE; FÁLCONM, 1989). Os enterócitos rompem-se durante a eliminação dos oocistos e temporariamente a barreira intestinal fica comprometida (BEVERLEY, 1976).
Apesar da importância do intestino dos felídeos no ciclo de vida do T. gondii, poucos são os estudos que avaliaram as consequências dessa infecção sobre a parede intestinal de gatos. O objetivo deste trabalho foi analisar os efeitos da infecção pelo T. gondii sobre a morfometria da parede intestinal, a distribuição de fibras colágenas, linfócitos intraepiteliais e células de Paneth e a dinâmica de mucinas secretadas no duodeno de gatos.
Material e Métodos
1. Delineamento experimental
Este trabalho foi previamente aprovado pelo Comitê de Ética em Pesquisa Envolvendo Experimentação Animal da UNIPAR (protocolo 1008/2008).
Foram utilizados seis gatos (Felis catus), com aproximadamente três meses de vida, distribuídos aleatoriamente em Grupo Controle (G1; n = 3) e Grupo Infectado (G2; n = 3). Todos os animais foram previamente desverminados com praziquantel (5 mg.kg1) e pomoato de pirantel (57,5 mg.kg1) (Drontal Gatos® Bayer S/A) e submetidos à colheita de sangue no intuito de verificar a presença de anticorpos anti-Toxoplasma gondii por meio da técnica de aglutinação direta, considerando como positivo título acima de 25. A negatividade a esse teste foi o critério de inclusão do animal no estudo.
2. Cepa de T. gondii
Foram utilizados para a inoculação experimental cistos teciduais de T. gondii da cepa ME-49, classificada como pertencente ao genótipo II (AJZENBERG et al., 2004), e obtida de camundongos previamente infectados com taquizoítos desse parasito, por via intraperitonial, como descrito por Dubey e Beattie (1988).
3. Infecção experimental
Os animais do Grupo 2 receberam por gavage uma única dose de 200 cistos teciduais da cepa ME49 de T. gondii. Todos os animais foram mantidos em gaiolas individuais e receberam água e ração comercial ad libitum. As fezes foram coletadas durante 30 dias, utilizando-se o método de Sheather (SLOSS et al., 1999) para a determinação do período inicial de liberação de oocistos.
4. Eutanásia e coleta de material biológico
Quarenta dias após a inoculação, o soro de cada animal foi submetido ao método de aglutinação direta para detecção de anticorpos anti-T. gondii (SILVA; CUTOLO; LANGONI, 2002) e, em seguida, submetidos à eutanásia. Os animais foram anestesiados pela via intramuscular, utilizando-se 7 mg.kg1 Zoletil® [(tiletamina + zolazepam (Virbac, São Paulo)] + 1mg.kg1 Calmiun® [xilazina 2% (Embu-Guaçu, São Paulo)], seguido da administração de 5 mL de cloreto de potássio a 10% intracardíaco. Foi realizada laparotomia vertical pela linha mediana ventral e retirada do duodeno, fixando-o em solução de Bouin.
5. Análise da parede intestinal
Após fixação, os segmentos foram desidratados em série ascendente de álcool etílico, diafanizados em xilol e incluídos em parafina para obtenção dos cortes transversais seriados de 3 mm, que foram corados com Hematoxilina e Eosina (HE) para análise morfométrica da parede intestinal e quantificação dos linfócitos intraepiteliais; Azan para evidenciação de fibras colágenas - Tricrômico-Mallory para detecção das células de Paneth; Ácido Periódico de Shiff (PAS) - para detecção de mucinas neutras e sialomucinas lábeis; Alcian-Blue (AB) pH 2,5 para detecção de sialomucinas e sulfomucinas e Alcian-Blue (AB) pH 1,0 para detecção das sulfomuncinas. No caso das técnicas para detecção de glicoconjugados (PAS e AB), realizou-se contracoloração com hematoxilina.
A avaliação qualitativa da parede intestinal foi realizada a partir de cortes corados com HE, Azan, Tricrômio de Mallory e PAS. Observou-se a organização dos tecidos que compõem os diferentes estratos da parede intestinal, comparando-os entre os dois grupos e procurando-se identificar diferentes estágios de vida do parasito. Com a técnica de PAS, procurou-se identificar cistos teciduais, já que a parede elástica dessas estruturas contém glicoconjugados neutros (GUIMARÃES; CARVALHO; BARBOSA, 2003; WEISS; KIM, 2007).
A análise morfométrica da parede intestinal foi realizada a partir de imagens de cortes corados com HE, capturadas com o auxílio de uma câmera digital (Moticam 2000, 2.0 Megapixel) acoplada a um microscópico de luz trinocular (MOTIC B5). Imagens capturadas com a objetiva de 4× foram utilizadas para medir a espessura total da parede e a espessura da túnica mucosa. A objetiva de 10× foi utilizada para medir a profundidade das criptas e altura dos vilos e a espessura da túnica muscular. Com a objetiva de 100× foi possível realizar a mensuração do maior eixo dos enterócitos e de seus núcleos presentes nos vilos e nas criptas. Foram realizadas 80 medidas nos vilos e nas criptas de cada parâmetro avaliado, distribuídas por toda a circunferência intestinal de cada gato.
Quantificaram-se as células caliciformes presentes em 0,32 mm2 da túnica mucosa presente nos vilos e nas criptas de cada animal. Na mesma área da túnica mucosa, foram quantificados os linfócitos intraepiteliais presentes nos vilos de cada animal, utilizando-se também a objetiva de 40×. Foi quantificado o número de células de Paneth presentes na base das criptas de toda a circunferência intestinal em 10 cortes seriados de cada animal, utilizando-se a objetiva de 40×.
6. Análise estatística
Os dados, inicialmente, foram submetidos ao teste D'Agostino-Pearson para verificar o tipo de distribuição. Dados com distribuição livre, apresentados como mediana (percentil 25; percentil 75), e a comparação entre os grupos foi realizada pelo teste de Mann-Whitney. Dados com distribuição normal foram apresentados como média ± desvio-padrão, e a comparação entre os dois grupos foi realizada pelo teste t de Student para amostras independentes. Valores de p menores que 0,05 foram considerados significantes para ambos os testes.
Resultados
Durante o período experimental, os animais do grupo G2 apresentaram, de forma intermitente, fezes amolecidas. A liberação de oocistos ocorreu a partir do sétimo dia de infecção. Os gatos do Grupo controle (G1) tiveram resultado negativo, e os do G2, positivo para a detecção de anticorpos anti-T. gondii.
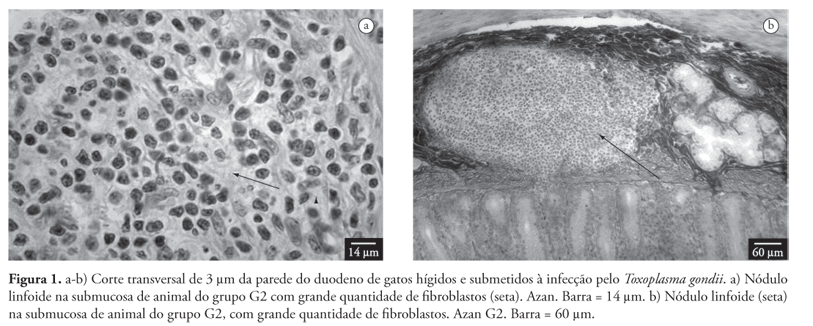
Não foram observadas alterações macroscópicas no intestino e mesentério dos animais de ambos os grupos. Observou-se a manutenção da estrutura normal da parede sem a presença de infiltrados inflamatórios nos animais do G2. Em um dos animais desse grupo verificou-se pequeno nódulo linfoide na submucosa com grande quantidade de fibroblastos, alguns macrófagos e pequena quantidade de colágeno em sua estrutura (Figura 1).
Na avaliação qualitativa, observou-se que as fibras colágenas ocupavam visivelmente uma maior área dos estratos da parede intestinal, o que sugere que estejam aumentadas nos animais do grupo G2 (Figura 2). Com as lâminas coradas por PAS, não foram observados cistos teciduais ou outros estágios de vida do T. gondii.
A análise morfométrica da parede intestinal demonstrou que a infecção causada por parasitos obtidos de cistos teciduais de T. gondii, provocou uma redução (p < 0,05) na espessura da túnica mucosa, túnica muscular e parede total do duodeno de gatos (Tabela 1; Figura 3). Foi observado um aumento na altura dos enterócitos localizados nos vilos e nas criptas, assim como do maior diâmetro do núcleo dos enterócitos localizados nos vilos (Tabela 2; Figura 3). A análise da dinâmica de glicoconjugados revelou uma diminuição (p < 0,05) das células caliciformes marcadas pela técnica histoquímica AB (pH 1,0) nos vilos do duodeno dos animais do G2 (Tabela 3).
A quantificação dos linfócitos intraepiteliais demonstrou nos animais do grupo G1 presença de 21,15 ± 10,89 células e, nos animais do grupo G2, a presença de 24,93 ± 9,26 células (p > 0,05). Verificou-se que o número de células de Paneth, no grupo G1, foi de 3,33 ± 2,31 e, no G2, foi de 13,33 ± 3,21 (p < 0,05).
Discussão
No presente estudo, observaram-se diferentes alterações morfométricas da parede intestinal de gatos frente à infecção com cistos teciduais de T. gondii (cepa ME-49), como a atrofia da túnica mucosa, túnica muscular e parede total. A atrofia intestinal é descrita como característica à tolerância imune que resulta da cronificação de uma infecção parasitária (ELIA; SOUZA, 2001). Os animais, por serem imunocompetentes, podem levar à cronificação da infecção e consequente formação de cistos teciduais no hospedeiro, apesar de não terem sido observados cistos teciduais nas secções realizadas no intestino, o que, segundo Dubey (1994), é um achado raro.
Após 40 dias, não foi observado aumento no número dos linfócitos intraepiteliais (IELs), possivelmente por se tratar de uma infecção crônica. Os enterócitos são as primeiras células a serem invadidas pelo T. gondii e, após a infecção, passam a secretar citocinas e quimiocinas, que são capazes de orientar a resposta imune (BOUT et al., 1999). Sofrem alterações morfológicas provocadas por moléculas citotóxicas secretadas pelos IELs. Essas moléculas atraem outras células imunes, como leucócitos polimorfonucleares (PMNs), macrófagos (MF) e células dendríticas (DCs) (KASPER; BUZONI-GATEL, 2001). A presença do parasito associada à resposta imune pode levar a danos epiteliais, permitindo bactérias comensais se instalarem no intestino, além de desorganizar a camada epitelial (BUZONI-GATEL; WERTS, 2006). Em estudos realizados com camundongos infectados pelo T. gondii, observaram-se áreas descontínuas de inflamação intestinal, com infiltrados de células inflamatórias mononucleares e PMNs na lamina própria, submucosa e camadas musculares (REMINGTON, 1974). Apesar da ausência de observação de enterite neste estudo, os enterócitos tornaram-se maiores, independentemente de sua localização. Acredita-se que essa alteração morfológica seja um reflexo de uma modificação do citoesqueleto dessa célula, no intuito de aumentar a distância entre a luz intestinal e a lâmina própria, dificultando o acesso parasitário à circulação sanguínea e linfática. Essa alteração também pode ser entendida como um mecanismo compensatório à atrofia da mucosa intestinal provocada pela infecção.
As células de Paneth existem na base das criptas intestinais e participam da imunidade inata por meio de diversos mecanismos, como a secreção de substâncias antimicrobianas (WERSHIL; FURUTA, 2008) e do transporte de imunoglobulinas como a IgA e IgG (LEVINE; HAGGITT, 1989). Neste estudo, observou-se o aumento do número das células de Paneth nos animais infectados pelo T. gondii, possivelmente contribuindo com o transporte de imunoglobulinas para controlar o nível populacional da microbiota intestinal, já que a atrofia da mucosa intestinal induzida pela infecção com T. gondii favorece uma invasão indesejada desses microrganismos.
A diarreia pode ser uma forma de expulsar parasitos (CASTRO et al., 1976) e foi encontrada após a infecção por cistos teciduais da cepa ME49 de T. gondii em galinhas (GALLI et al., 2008). Apesar da diarreia ser um dos sintomas mais frequentes em gatos com toxoplasmose, (CASTRO; et al., 1976) neste estudo não foi observada. Em animais com toxoplasmose, a presença de diarreia está diretamente relacionada com a atrofia das vilosidades e hiperplasia das criptas (ELIA; SOUZA, 2001), achados histológicos não observados nos animais infectados pelo T. gondii neste experimento. Em animais com infecção parasitária, ocorre a indução de processo inflamatório pelas células musculares intestinais. Neste estudo, observou-se uma redução da espessura da túnica muscular, o que preliminarmente pode ser entendido que a força muscular imprimida no conteúdo intestinal era menor, o que diminuiria o trânsito intestinal no intestino delgado. Por outro lado, esse fenômeno deve estar invertido no intestino grosso para justificar a observação de fezes menos sólidas observadas neste estudo. Estudos fisiológicos devem ser realizados para confirmar essa hipótese, pois esse entendimento aumentaria o risco de invasão de microrganismos no intestino delgado, considerando o resultado deste estudo de atrofia da mucosa intestinal.
Outra possível explicação para a alteração da textura das fezes seria o envolvimento dos neurônios mientéricos que coordenam a motilidade intestinal (FURNESS, 2006) e que possuem uma íntima associação com o sistema imune (SPILLER; GRUNDY, 2004). Galinhas infectadas com oocistos de T. gondii apresentaram diarreia, atrofia da túnica mucosa e redução significativa do número de neurônios mientéricos (BONAPAZ et al., 2009). São necessários estudos complementares que analisem o plexo mientérico e as subpopulações neuronais para compreensão dos mecanismos envolvidos nas fezes amolecidas e na atrofia muscular.
A análise dos cortes corados por Azan mostram um aumento da quantidade de fibras colágenas nos animais infectados pelo T. gondii. Possivelmente, o aumento na concentração de fibras de colágeno se deve a um processo de regeneração ou cicatrização resultante da infecção crônica pelo T. gondii. A infecção parasitária leva a uma inflamação (KASPER; BUZONI-GATEL, 2001) e, na inflamação crônica, os macrófagos liberam a Interleucina-1 (IL-1), promovendo a proliferação de fibroblastos e estimulando a síntese de fibras colágenas que são gradualmente remodeladas por várias semanas ou meses, à medida que a área retorna ao normal (BIER, 2008). Observou-se que somente as células marcadas por Alcian-Blue (AB). pH 1,0 diminuíram no grupo infectado por T. gondii (p < 0,05), demonstrando que houve alteração no perfil secretório de mucinas ácidas sulfatadas, que indica redução da secreção das sulfomucinas nos vilos. Esse resultado sugere que o equilíbrio na composição química do muco que recobre a mucosa foi quebrado, passando ao possível predomínio de muco neutro. Como o muco neutro tem maior capacidade de proteção, por ser mais denso em meio aquoso, quando as células são expostas a agentes abrasivos e irritantes (BEAMISH, 1972; ZIESKE; BERNSTEIN, 1982), é possível que esse achado seja uma resposta para proteção do epitélio intestinal em razão da atrofia da mucosa. Estudos anteriores, realizados com galinhas infectadas pelo T. gondii, demonstraram resultados semelhantes com o aumento da secreção proporcional de mucinas neutras (SHIRAISHI et al, 2009; BONAPAZ et al., 2009).
Conclui-se que a infecção crônica pelo T. gondii levou à atrofia da túnica mucosa, túnica muscular e da parede intestinal do duodeno de gatos. Induziu também um aumento na altura dos enterócitos e levou as fibras colágenas a ocuparem uma maior área dos estratos da parede, à redução da secreção de sialomucinas e ao aumento das células de Paneth. A verificação da eliminação de oocistos se deu como forma de comprovação da efetividade da infecção.
Recebido em 30 de Março de 2009
Aceito em 22 de Setembro de 2009
- AJZENBERG, D. et al. Genetic diversity: clonality and sexuality in Toxoplasma gondii International Journal of Parasitology, v. 34, n. 10, p. 1185-1196, 2004.
- BARRAGAN, A.; SIBLEY, D. Migration of Toxoplasma gondii across biological barriers. Trends in Microbiology, v. 11, n. 9, p. 426-430, 2003.
- BLACK, M. W.; BOOTHROYD, J. C. Lytic cycle of Toxoplasma gondii. Microbiology and Molecular Biology Review, v. 64, n. 3, p. 607-623, 2000.
- BEAMISH, R. J. Lethal pH for white sucker Catostomus commersoni (Lacépède). Transaction of American Fisheries Society, v. 101, n. 2, p. 335-358, 1972
- BEVERLEY, J. K. A. Toxoplasma in animals. The Veterinary Record, v. 99, n. 7, p. 123-127, 1976.
- BIER, O. Imunologia básica e aplicada São Paulo: Guanabara Koogan, 2008. 449 p.
- BONAPAZ, R. et al. Effects of infection with Toxoplasma gondii oocysts on the intestinal wall and the myenteric plexus of Gallus gallus Pesquisa Veterinária Brasileira, 2009. (no prelo)
- BOUT, D. et al. Interaction between Toxoplasma gondii and enterocyte. Immunobiology, v. 201, n. 2, p. 225-228, 1999.
- BUZONI-GATEL, D.; WERTS, C. Toxoplasma gondii and subversion of the immune system. Trends in Parasitology, v. 22, n. 10, p. 448-452, 2006.
- CASTRO, G. A. et al. Altered small bowel propulsion associated with parasitism. Gastroenterology, v. 71, n. 4, p. 620-625, 1976.
- CHAPLIN, E. L.; SILVA, N. R. S.; ARAÚJO, F. A. P. Eliminação de Oocistos Tipo- Toxoplasma por felinos Naturalmente Infectados. Arquivos da Faculdade de Veterinária UFRGS, v. 19, p. 77-81, 1991.
- DAVIS, S. W.; DUBEY, J. P. Mediation of immunity to Toxoplasma gondii oocyst shedding in cats. The Journal of Parasitolology, v. 81, n. 6, p. 882-886, 1995.
- DENKERS, E. Y, GAZZINELLI, R. T. Regulation and function of T-cell-mediated immunity during Toxoplasma gondii infection. Clinical Microbiology Reviews, v. 11, n. 4, p. 569- 588, 1998.
- DUBEY, J. P.; BEATTIE, C. P. Toxoplasmosis of animals and man Boca Ratton: CRC Press, 1988. 220 p.
- DUBEY, J. P. Toxoplasmosis. Zoonosis Update, v. 205, n. 11, p. 1593-1598, 1994.
- ELIA, C. C. S.; SOUZA, H. S. P. Imunologia da mucosa intestinal: da bancada ao leito. São Paulo: Editora Atheneu, 2001. 197 p.
- FERGUSON, D. J. P. et al. The expression and Distribution of Dense Granule Proteins in the Enteric (coccidian) Forms of Toxoplasma gondii in the small intestine of the cat. Experimental Parasitology, v. 91, n. 3, p. 203-211, 1979.
- FERREIRA, M. U.; FORONDA, A. S.; SCHUMAKER, T. T. S. Fundamentos biológicos da parasitologia humana São Paulo: Manole, 2003. p. 17-25.
- FREYRE, A.; FÁLCONM, J. D. Toxoplasmosis en las especies domésticas y como zoonosis Montevideo: Universidad de la República, 1989. 332 p.
- FURNESS, J. B. The enteric nervous system Malden: Blackwell Publishing, 2006. p. 3-28.
- GALLI, S. et al. Infecção experimental de frangos domésticos (Gallus gallus) com cepas geneticamente distintas de Toxoplasma gondii Veterinária e Zootecnia, v. 15, n. 3, p. 542-550, 2008.
- GUIMARÃES, E. V.; CARVALHO, L.; BARBOSA, H. S. An alternative technique to reveal polysaccharides in Toxoplasma gondii Tissue Cysts. Memórias do Instituto Oswaldo Cruz, v. 97, n. 7, p. 915-917, 2003.
- KASPER, L. H.; BUZONI-GATEL, D. Ups and downs of mucosal cellular immunity against protozoan parasites. Infection and Immunity, v. 69, n. 1, p. 1-8, 2001.
- LEVINE, D. S.; HAGGITT, R. C. Normal histology of the colon. The American Journal of Surgical Pathology, v. 13, n. 11, p. 966-984, 1989.
- NOGAMI, S. et al. Seroprevalence against Toxoplasma gondii in Domiciled Cats in Japan. The Journal of veterinary medical science, v. 60, n. 9, p. 1001-1004, 1998.
- RACHINEL, N. et al. The induction of Acute Ileitis by a Single Microbial Antigen of Toxoplasma gondii. The Journal of Immunology, v. 173, p. 2725-2735, 2004.
- REMINGTON, J. S. Toxoplasma in the adult. New York Academiy of Medicine, v. 50, n. 2, p. 211-227, 1974.
- SHIRAISHI, C. S. et al. Análise morfométrica da parede intestinal e dinâmica de mucinas secretadas no íleo de frangos infectados por T. gondii. Ciência Rural, v. 39, n. 7, p. 2146-2153, 2009
- SLOSS, M. W. Parasitologia Clínica Veterinária 6 ed. São Paulo: Manole, 1999.
- SPILLER, R.; GRUNDY, D. Pathophysiology of the enteric nervous system: a basis for understanding functional diseases. Oxford: Blackwell Publishing, 2004. 272 p.
- WEISS, L.; KIM, K. Toxoplasma gondii The model apicomplexan: perspectives and methods. Rio de Janeiro: Elsevier, 2007. p. 19-48.
- WERSHIL, B. K.; FURUTA, G. T. Gastrointestinal mucosal immunity. Journal of Allergy and Clinical Immunology, v. 121, n. 2, p. S380-383, 2008.
- ZIESKE, J. D.; BERNSTEIN, I. A. Modification of cell surface glycoprotein: addition of fucosyl residues during epidermal differentiation. The Journal of Cell Biology, v. 95, n. 2, p. 626-631, 1982.
Datas de Publicação
-
Publicação nesta coleção
17 Set 2010 -
Data do Fascículo
Mar 2010
Histórico
-
Recebido
30 Mar 2009 -
Aceito
22 Set 2009