Resumo
Campo de murundus ou covoal é uma das fitofisionomias do Cerrado menos conhecidas floristicamente, cujo componente arbóreo é mais estudado que o componente herbáceo-subarbustivo. Apresentamos o levantamento florístico da família Asteraceae em um campo de murundus do município de Jataí, Goiás. As coletas foram realizadas por meio do método de caminhamento. Um total de 41 espécies foi registrado na área estudada, das quais 34 são autóctones e sete espécies são alóctones para o Cerrado. O número de espécies encontrado é superior ao registrado em campos de murundus do Parque Estadual do Araguaia e apenas Ayapana amygdalina e Chrysolaena obovata são comuns às duas áreas. As espécies comuns entre a área estudada e 14 outras localidades no Cerrado são Achyrocline alata, A. satureioides, Ayapana amygdalina, Mikania officinalis e Chromolaena laevigata. Algumas espécies são endêmicas e dentre estas, duas são restritas ao Cerrado, uma delas inclusive nova para a ciência. Do total apenas uma está registrada ocorrendo em campos de murundus na lista do Cerrado. Este estudo é o primeiro realizado para a família Asteraceae em campo de murundus e espera-se contribuir com a ampliação do conhecimento sobre as espécies que ocorrem nesta fisionomia.
Palavras-chave:
Compositae; covoal; flora herbáceo-subarbustiva; parque de cerrado
Abstract
Campos de murundus or covoal (earthmounds) is one of the less floristically known phytophysiognomies of the Cerrado, in which the arboreal component is more studied than the herbaceous-subshrub components. We present a floristic survey of Asteraceae family in campo de murundus in the municipality of Jataí, state of Goias, Brazil. The collections were made using the walking method. A total of 41 species was recorded, from which 34 species are autochthonous and seven are allochthonous to the Cerrado. The species number found is higher than that registered in campo de murundu” of Araguaia State Park, and only Ayapana amygdalina and Chrysolaena obovata are common to both areas. Species common to the studied area and 14 other localities in the Cerrado are Achyrocline alata, A. satureioides, Ayapana amygdalina, Mikania officinalis, and Chromolaena laevigata. Some species are endemic and from these, two are restricted to the Cerrado, one of them is new to science. Only one of the registered species is recorded as occurring in campos de murundus in the Brazilian Cerrado checklist. This study is the first carried out for Asteraceae in campos de murundus and we hope to contribute to expanding the knowledge of species occurring in this phytophysiognomy.
Key words:
Compositae; covoal; herbaceous-subshrub flora; parque de cerrado
Introdução
Campo de murundus, covoal ou parque de cerrado é uma fitofisionomia savânica do Cerrado (sensuRibeiro & Walter 2008Ribeiro JF & Walter BMT (2008) As principais fitofisionomias do Bioma Cerrado. In: Sano SM, Almeida SP & Ribeiro JF (eds.) Cerrado: ecologia e flora. Embrapa Cerrados, Planaltina. Pp. 151-212.) que apresenta características peculiares que a torna ecologicamente distinta dos demais ambientes savânicos. Uma das principais características é a presença de relevo na forma de pequenas e inúmeras elevações convexas e arredondadas, isoladas umas das outras, com dimensões variáveis em altura e diâmetro sobre um terreno plano ou levemente inclinado e que são conhecidas popularmente por “murundu”, “monchão”, “cocoruto”, “morrote”, “capãozinho” ou “ilha” e geralmente estão associados a cupinzeiros (Araújo-Neto et al. 1986Araújo-Neto MD, Furley PA, Haridasan M & Johnson CE (1986) The Murundus of the Cerrado region of Central Brazil. Journal of Tropical Ecology 2: 17-35.; Furley 1986Furley PA (1986) Classification and distribution of murundus in the Cerrado of central Brazil. Journal of Biogeography 13: 265-268.; Schneider & Silva 1991Schneider MO & Silva DB (1991) Estrutura pedológica e dinâmica hídrica do “covoal” do Córrego da Fortaleza. Sociedade & Natureza 3: 75-89.; Oliveira-Filho 1992aOliveira-Filho AT (1992a) Floodplain ‘murundus’ of Central Brazil: evidence for the termite-origin hypothesis. Journal of Tropical Ecology 8: 1-19.; Marimon & Lima 2001Marimon BS & Lima ES (2001) Caracterização fitofisionômica e levantamento florístico preliminar no pantanal dos rios Mortes-Araguaia. Acta Botanica Brasilica 15: 213-229.; Resende et al. 2004Resende ILM, Araújo GMA, Oliveira APA, Oliveira AP & Ávila Júnior RS (2004) A comunidade vegetal e as características abióticas de um campo de murundu em Uberlândia MG. Acta Botanica Brasilica 18: 9-17.; Ribeiro & Walter 2008Ribeiro JF & Walter BMT (2008) As principais fitofisionomias do Bioma Cerrado. In: Sano SM, Almeida SP & Ribeiro JF (eds.) Cerrado: ecologia e flora. Embrapa Cerrados, Planaltina. Pp. 151-212.) (Fig. 1).
Campo de Murundus no período chuvoso (a) e de seca (b) no sudoeste de Goiás, Brasil. Fotos: Frederico, A.G.G.
Figure 1
Campo de Murundus during rainy (a) and dry (b) periods in Southwestern Goiás, Brazil.
Em geral, a fitofisionomia possui o lençol freático superficial que proporciona uma inundação sazonal nas depressões entre os murundus (Schneider & Silva 1991Schneider MO & Silva DB (1991) Estrutura pedológica e dinâmica hídrica do “covoal” do Córrego da Fortaleza. Sociedade & Natureza 3: 75-89.; Oliveira-Filho 1992bOliveira-Filho AT (1992b) The vegetation of Brazilian “murundus”: the island-efect on the plant community. Journal of Tropical Ecology 8: 465-486.; Castro-Júnior 2002Castro-Júnior PR (2002) Dinâmica da água em campos de murundus do Planalto dos Parecis. Tese de doutorado. Universidade de São Paulo, São Paulo. 193p.). Esta dinâmica hídrica confere aos campos de murundus a condição de reservatório natural, por armazenar a água pluvial no solo para fornecê-la lenta e continuamente às nascentes e cursos d’água de primeira ordem nos meses com restrição pluviométrica, perenizando assim, o setor de cabeceira da bacia hidrográfica (Schneider & Silva 1991Schneider MO & Silva DB (1991) Estrutura pedológica e dinâmica hídrica do “covoal” do Córrego da Fortaleza. Sociedade & Natureza 3: 75-89.; Castro-Júnior 2002Castro-Júnior PR (2002) Dinâmica da água em campos de murundus do Planalto dos Parecis. Tese de doutorado. Universidade de São Paulo, São Paulo. 193p.).
Desta forma, os murundus atuam como “ilhas” para o estabelecimento de um estrato lenhoso semelhante ao do Cerrado sentido restrito, além de funcionar como local de refúgio para fauna (Araújo-Neto et al. 1986Araújo-Neto MD, Furley PA, Haridasan M & Johnson CE (1986) The Murundus of the Cerrado region of Central Brazil. Journal of Tropical Ecology 2: 17-35.; Oliveira-Filho 1992aOliveira-Filho AT (1992a) Floodplain ‘murundus’ of Central Brazil: evidence for the termite-origin hypothesis. Journal of Tropical Ecology 8: 1-19.; Ribeiro & Walter 2008Ribeiro JF & Walter BMT (2008) As principais fitofisionomias do Bioma Cerrado. In: Sano SM, Almeida SP & Ribeiro JF (eds.) Cerrado: ecologia e flora. Embrapa Cerrados, Planaltina. Pp. 151-212.). Coexistindo com o estrato lenhoso, ocorre um estrato vegetal dominado por plantas herbáceas adaptadas à saturação hídrica ao longo das depressões entre os murundus (Araújo-Neto et al. 1986Araújo-Neto MD, Furley PA, Haridasan M & Johnson CE (1986) The Murundus of the Cerrado region of Central Brazil. Journal of Tropical Ecology 2: 17-35.; Schneider & Silva 1991Schneider MO & Silva DB (1991) Estrutura pedológica e dinâmica hídrica do “covoal” do Córrego da Fortaleza. Sociedade & Natureza 3: 75-89.; Ribeiro & Walter 2008Ribeiro JF & Walter BMT (2008) As principais fitofisionomias do Bioma Cerrado. In: Sano SM, Almeida SP & Ribeiro JF (eds.) Cerrado: ecologia e flora. Embrapa Cerrados, Planaltina. Pp. 151-212.).
A fitofisionomia campo de murundus apresenta expressiva riqueza florística, porém, apenas parcialmente conhecida. O componente arbustivo-arbóreo foi mais estudado (e.g.,Oliveira Filho & Martins 1991Oliveira Filho AT & Martins FR (1991) A comparative study of five cerrado areas in southern Mato Grosso Brazil. Edinburgh Journal of Botany 48: 37-332.; Oliveira-Filho 1992bOliveira-Filho AT (1992b) The vegetation of Brazilian “murundus”: the island-efect on the plant community. Journal of Tropical Ecology 8: 465-486.; Marimon & Lima 2001Marimon BS & Lima ES (2001) Caracterização fitofisionômica e levantamento florístico preliminar no pantanal dos rios Mortes-Araguaia. Acta Botanica Brasilica 15: 213-229.; Resende et al. 2004Resende ILM, Araújo GMA, Oliveira APA, Oliveira AP & Ávila Júnior RS (2004) A comunidade vegetal e as características abióticas de um campo de murundu em Uberlândia MG. Acta Botanica Brasilica 18: 9-17.; Marimon et al. 2012Marimon BS, Marimon-Junior BH, Mews HA, Jancoski HS, Franczak DD, Lima HS, Lenza E, Rossete AN & Moresco MC (2012) Florística de campos de murundus do Pantanal do Araguaia. Acta Botanica Brasilica 26: 181-196.; Pinto et al. 2014Pinto JRR, Mews HA, Jancoski HS, Marimon BS & Bomfim BO (2014) Woody vegetation dynamics in a floodplain campo de murundus in central Brazil. Acta Botanica Brasilica 28: 519-526.) do que o herbáceo-subarbustivo, para o qual destaca-se o estudo de Marimon et al. (2012)Marimon BS, Marimon-Junior BH, Mews HA, Jancoski HS, Franczak DD, Lima HS, Lenza E, Rossete AN & Moresco MC (2012) Florística de campos de murundus do Pantanal do Araguaia. Acta Botanica Brasilica 26: 181-196..
Asteraceae é considerada a família mais rica em número de espécies entre as Eudicotiledôneas, com aproximadamente 27.000 espécies agrupadas em cerca de 1.700 gêneros (Funk et al. 2009Funk VA, Susanna A, Stuessy TF & Robinson H (2009) Classication of Compositae. In: Funk VA, Susanna A, Stuessy TF & Bayer RJ (eds.) Systematics, evolution, and biogeography of Compositae. IAPT, Vienna. Pp. 171-176.), sendo que no Brasil ocorrem cerca de 2.064 espécies reunidas em 278 gêneros (BFG 2018). A riqueza florística de angiospermas do Cerrado é estimada em mais de 12.500 espécies nativas ou naturalizadas (BFG 2018). Deste total, a família Asteraceae contribui com 1.247 espécies (BFG 2018) ou cerca de 10%, sendo considerada floristicamente importante no Cerrado (Ratter et al. 1997Ratter JA, Ribeiro JF & Bridgewater S (1997) The Brazilian Cerrado vegetation and threats to its biodiversity. Annal of Botany 8: 223-230.; Batalha & Mantovani 2001Batalha MA & Mantovani W (2001) Floristic composition of the Cerrado in the Pé-de-Gigante reserve (Santa Rita do Passa Quatro Southeastern Brazil). Acta Botanica Brasilica 15: 289-32.; Mendonça et al. 2008Mendonça RC, Felfili JM, Walter BMT, Silva Jr. MC, Rezende AV, Filgueiras TS, Nogueira PE & Fagg CW (2008) Flora vascular do bioma Cerrado: checklist com 12.356 espécies. In: Sano SM, Almeida SP & Ribeiro JF (eds.) Cerrado: ecologia e flora. Embrapa Cerrados, Planaltina. Pp. 421-1279.; Souza & Lorenzi 2012Souza VC & Lorenzi H (2012) Botânica sistemática: guia ilustrado para identificação das famílias de angiospermas da flora brasileira baseado em APG III. 3ª ed. Instituto Plantarum, Nova Odessa. 768p.).
No Cerrado, Asteraceae está entre as famílias com maior riqueza de espécies em diversos levantamentos florísticos e, de acordo com Ferreira et al. (2009)Ferreira SC, Carvalho-Okano RM & Nakajima JN (2009) A família Asteraceae em um fragmento Florestal, Viçosa, Minas Gerais, Brasil. Rodriguésia 60: 903−942., os levantamentos que incluem a família Asteraceae geralmente estão restritos aos campos rupestres, cerrado sentido restrito e florestas. Algumas fisionomias são menos frequentemente incluídas em levantamentos florísticos, como veredas (Araújo et al. 2002Araújo GM, Barbosa AA, Arantes AA & Amaral AF (2002) Composição florística de veredas no Município de Uberlândia MG. Revista Brasileira de Botânica 25: 475-493.), formações campestres (Munhoz & Proença 1998Munhoz CBR & Proença C (1998) Composição florística no município de Alto Paraíso de Goiás na Chapada dos Veadeiros. Boletim do Herbário Ezechias Paulo Heringer 3: 102-150.; Munhoz & Felfili 2007Munhoz CBR & Felfili JM (2007) Florística do estrato herbáceo-subarbustivo de um campo limpo úmido em Brasília Brasil. Biota Neotropica 7: 207-215.) e campos de murundus, tendo sido publicado apenas o trabalho de Marimon et al. (2012)Marimon BS, Marimon-Junior BH, Mews HA, Jancoski HS, Franczak DD, Lima HS, Lenza E, Rossete AN & Moresco MC (2012) Florística de campos de murundus do Pantanal do Araguaia. Acta Botanica Brasilica 26: 181-196..
A flora herbácea-subarbustiva do Cerrado apresenta relevante número de espécies. Por ser menos inventariada do que o componente arbóreo-arbustivo, é menos conhecida. Portanto, pode estar mais seriamente ameaçada, seja devido à perda dos possíveis endemismos, pela extinção de habitats ou alterações ecológicas esperadas diante de um cenário iminente de mudanças climáticas globais.
Este estudo tem como objetivos apresentar um inventário da família Asteraceae em um campo de murundus e compará-lo com levantamentos florísticos da família conduzidos no Cerrado para analisar a distribuição geográfica das espécies.
Material e Métodos
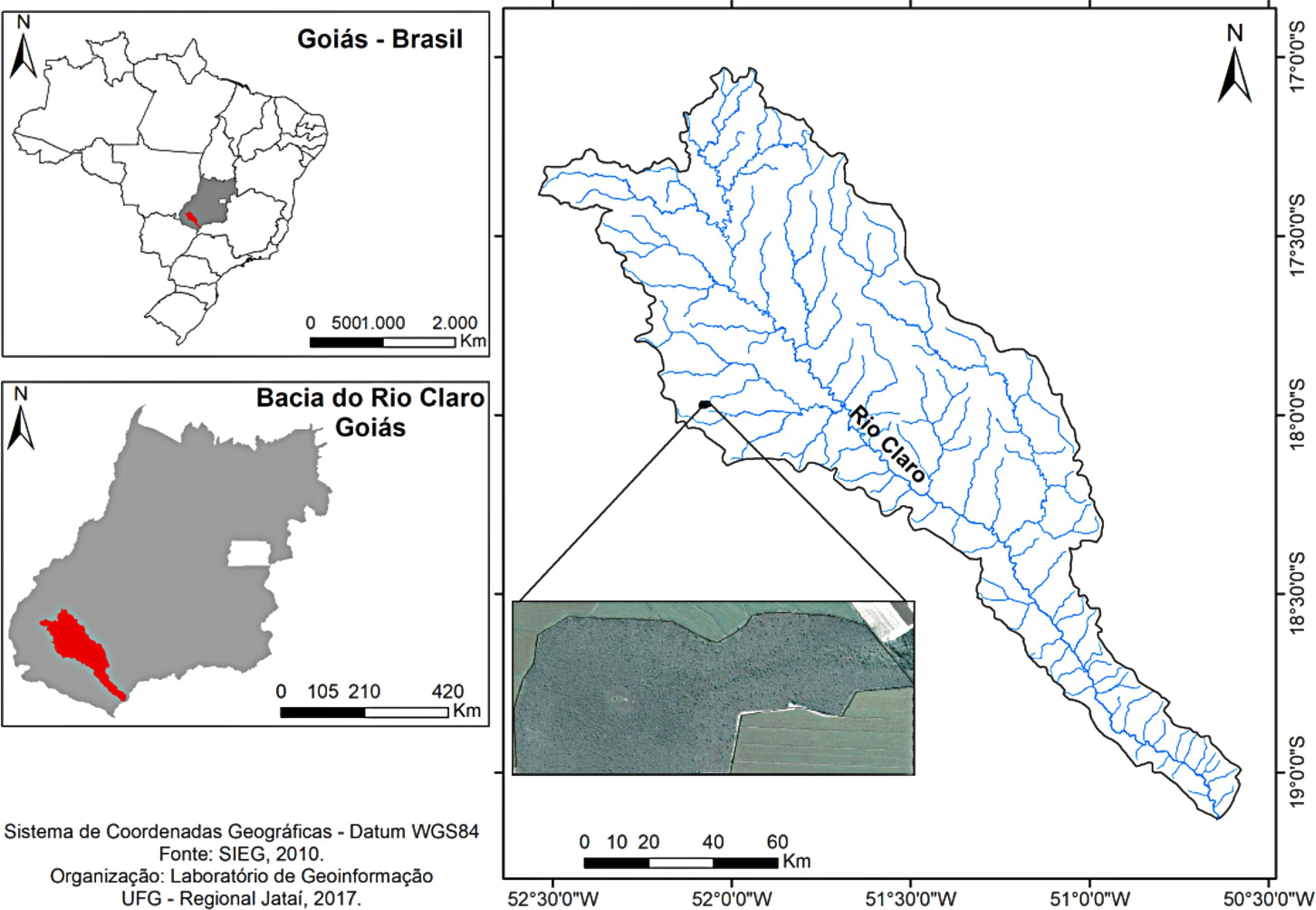
O estudo foi conduzido em um remanescente de campo de murundus com aproximadamente 300 hectares, localizado na propriedade rural Boa Vista, no município de Jataí, Goiás (Fig. 2). O local de estudo será mencionado pela sigla CMBV (campo de murundus Boa Vista) ao longo do texto.
Localização do campo de murundus no município de Jataí, Goiás.
Figure 2
Localization of earthmounds in Jatai municipality in Goias stad in Brazil.
O clima da região é do tipo Aw (Köppen), mesotérmico (Silva et al. 2008Silva FAM, Assad ED, Evangelista BA (2008) Caracterização climática do bioma Cerrado. In: Sano SM, Almeida SP & Ribeiro JF (eds.) Cerrado: ecologia e flora. Embrapa, Planaltina. Pp. 69-88.), com temperatura anual variando entre 18 e 32 °C em dois períodos climáticos bem definidos (seco: maio a outubro; chuvoso: novembro a abril) e índices pluviométricos entre 1.600 mm e 1.700 mm (Gomes Filho et al. 2011Gomes Filho RR, Silva JH, Paulino HB, Carneiro MAC & Costa CAG (2011) Velocidade de infiltração da água num plintossolo háplico de campo de murundu sob um cronossequência de interferência antrópica. Revista Brasileira de Agricultura Irrigada 5: 245-253.). O solo é classificado como plintossolo argilúvico, característico de áreas de campos de murundus da região sudoeste do estado de Goiás (Silva 2010Silva JG (2010) Índice de qualidade de um Plintossolo Argilúvico para fins agrícolas no Cerrado do Sudoeste de Goiás. Dissertação de Mestrado. Universidade Federal de Goiás, Jataí. 59p.).
A área natural de campo de murundus que ocupava cerca de 3% da propriedade foi reduzida à metade e a parte desmatada foi drenada e substituída por plantio de grãos. Há 15 anos, canais de drenagem foram feitos em todo o entorno da área de campo de murundus, com aproximadamente um metro de largura por dois de profundidade (Maricato et al. 2017Maricato HS, Pereira FC, Souza LF, Gomes DC & Guilherme FAG (2017) Aspectos físicos e estrutura da vegetação lenhosa em três campos de murundus no sudoeste goiano. Revista Brasileira de Biociências 15: 169-177.).
As coletas foram realizadas com o método de caminhamento (Filgueiras et al. 1994Filgueiras TS, Nogueira PE, Brochado AL & Guala GF (1994) Caminhamento: um método expedito para levantamentos florísticos qualitativos. Cadernos de Geociências 12: 39-43.) nas depressões e nos murundus das bordas e do interior da área, com esforço de coleta em sete visitas a campo, entre setembro de 2009 a agosto de 2011. Todos os espécimes férteis foram coletados e identificados por meio de consulta à bibliografia especializada (e.g.,Baker 1873Baker JG (1873) Compositae I: Vernoniaceae. In: Martius CFP & Eichler AG (eds.) Flora brasiliensis. Monachii, Lipsiae. Vol. 6. Pars 2. Pp. 1-180., 1876Baker JG (1876) Compositae II: Eupatoriaceae. In: Martius CFP & Eichler, AG (eds.) Flora brasiliensis. Monachii, Lipsiae. Vol. 6. Pars 2. Pp. 181-376., 1882Baker JG (1882) Compositae III: Asteroideae & Inuloideae. In: Martius CFP & Eichler AG (eds.) Flora brasiliensis. Monachii, Lipsiae. Vol. 6. Pars 2. Pp. 1-134., 1884Baker JG (1884) Compositae IV: Helianthoideae - Mutisiaceae. In: Martius CFP & Eichler AG (eds.) Flora brasiliensis. Monachii. Vol. 6. Pars 3. Pp. 135-398.; Barroso et al. 1986Barroso GM, Peixoto AL, Costa CG, Ichaso CLF, Guimarães EF & Lima HC (1986) Sistemática de angiospermas do Brasil. Vol. 3. Imprensa Universitária da Universidade Federal de Viçosa, Viçosa. 326 p.; Cabrera 1974Cabrera AL (1974) Compositae. In: Burkart A (ed.) Flora ilustrada de Entre Rios 6: 106-540. , 1978Cabrera AL (1978) Compositae. In: Cabrera AL (ed.) Flora de la Provincia de Jujuy - Republica Argentina 10: 1-726.; Moreira & Teles 2014Moreira GL & Teles AM (2014) A tribo Vernonieae (Asteraceae) na Serra Dourada, Goiás, Brasil. Iheringia, Série Botânica 69: 357-385.; Ribeiro & Teles 2015Ribeiro RN & Teles AM (2015) Eupatorieae (Asteraceae) no Parque Estadual da Serra Dourada, Goiás, Brasil. Rodriguésia 66: 887-903.; Teles & Stehmann 2016Teles AM & Stehmann JR (2016) A tribo Senecioneae (Asteraceae) em Minas Gerais, Brasil. Rodriguésia 67: 455-487.), comparação com material testemunho de herbário e consulta à especialistas. As coletas foram tombadas como material testemunho no herbário Jataiense Professor Germano Guarim Neto (HJ) da Regional Jataí e no herbário UFG, em Goiânia, ambos pertencentes à Universidade Federal de Goiás. Cada espécie foi classificada quanto ao hábito (Bernacci & Leitão-Filho 1996Bernacci LCB & Leitão-Filho HF (1996) Flora fanerogâmica da fazenda São Vicente Campinas-SP. Revista Brasileira de Botânica 19: 149-164.). Os nomes das espécies e respectivos autores foram confirmados através da consulta no IPNI (http://www.ipni.org).
Os levantamentos florísticos realizados no Cerrado que apresentavam dez ou mais espécies da família Asteraceae foram selecionados para a comparação florística (Tab. 1). A caracterização da origem das espécies como autóctone (ou seja, nativa) ou alóctone (ou seja, exótica) para o Cerrado seguiu Mendonça et al. (2008)Mendonça RC, Felfili JM, Walter BMT, Silva Jr. MC, Rezende AV, Filgueiras TS, Nogueira PE & Fagg CW (2008) Flora vascular do bioma Cerrado: checklist com 12.356 espécies. In: Sano SM, Almeida SP & Ribeiro JF (eds.) Cerrado: ecologia e flora. Embrapa Cerrados, Planaltina. Pp. 421-1279. e o projeto Flora do Brasil online (2020)Flora do Brasil 2020 em construção. Jardim Botânico do Rio de Janeiro. Disponível em <http://floradobrasil.jbrj.gov.br>. Acesso em 25 fevereiro 2018.
http://floradobrasil.jbrj.gov.br...
. Consideramos os diferentes sinônimos das
Comparação simplificada (presença/ausência) das espécies autóctones do presente estudo com levantamentos realizados no Cerrado que incluíram espécies da família Asteraceae. *Somente as espécies da família Asteraceae foram consideradas.
Table 1
Simplified comparison (presence/absence) of autochthonous species found in the present study with surveys conducted in the Cerrado that included species of the family Asteraceae. *Only species of family Asteraceae were considered.
Resultados e Discussão
Durante o período do estudo, coletamos 71 amostras férteis pertencentes à família Asteraceae no CMBV e identificamos 29 gêneros e 41 espécies (Tab. 2 - disponibilizada no link <https://figshare.com/s/59e753cd680cfc39f3ed>)(Figs. 3 e 4), das quais uma é nova para a ciência (Baccharis sp. nov.), espécie bastante singular e que no momento é conhecida apenas em uma única localidade que sofre extrema pressão antrópica. Disynaphia senecionidea (Baker) R.M.King & H.Rob. foi registrada pela primeira vez para o estado de Goiás (Tab. 2 - disponibilizada no link <https://figshare.com/s/59e753cd680cfc39f3ed>) (Figs. 3 e 4).
a. Achyrocline alata; b. Ayapana amygdalina; c. Bidens segetum; d. Chromolaena laevigata; e. Chresta sphaerocephala; f. Clibadium armani; g. Chromolaena ivifolia; h. Heterocondylus pumilus. Fotos: A.M. Teles.
Figure 3
a. Achyrocline alata; b. Ayapana amygdalina; c. Bidens segetum a; d. Chromolaena laevigata; e. Chresta sphaerocephala; f. Clibadium armani; g. Chromolaena ivifolia; h. Heterocondylus pumilus.
a. Baccharis trinervis; b. Disynaphia senecionidea; c. Pterocaulon rugosum; d. Mikania officinalis; e. Erechtites hieracifolius; f. Raulinoreitzia crenulata; g. Chromolaena maximilianii; h. Mikania cordifolia. Fotos: A.M. Teles.
Figure 4
a. Baccharis trinervis; b. Disynaphia senecionidea; c. Pterocaulon rugosum; d. Mikania officinalis; e. Erechtites hieracifolius (L.) Raf. ex DC.; f. Raulinoreitzia crenulata; g. Chromolaena maximilianii; h. Mikania cordifolia.
De acordo com Mendonça et al. (2008)Mendonça RC, Felfili JM, Walter BMT, Silva Jr. MC, Rezende AV, Filgueiras TS, Nogueira PE & Fagg CW (2008) Flora vascular do bioma Cerrado: checklist com 12.356 espécies. In: Sano SM, Almeida SP & Ribeiro JF (eds.) Cerrado: ecologia e flora. Embrapa Cerrados, Planaltina. Pp. 421-1279., 34 espécies (Tab. 2 - disponibilizada no link <https://figshare.com/s/59e753cd680cfc39f3ed>) são autóctones para o Cerrado e dentre estas, 18 gêneros são representados por uma única espécie. Os gêneros mais ricos em espécies foram Lessingianthus H.Rob. e Chromolaena DC., com quatro espécies cada, e Achyrocline (Less.) DC., Baccharis L., Mikania Willd. e Pterocaulon Elliott com duas espécies cada. Apesar da baixa ocorrência de espécies de Lessingianthus, Baccharis e Mikania neste estudo, estes são alguns dos gêneros com maior destaque no Cerrado devido à riqueza de espécies (Mendonça et al. 2008). Os gêneros Calea L. e Aspilia Thouars são gêneros que também se destacam no bioma devido à abundância de espécies, mas no presente estudo são representados por uma única espécie cada um.
Marimon et al. (2012)Marimon BS, Marimon-Junior BH, Mews HA, Jancoski HS, Franczak DD, Lima HS, Lenza E, Rossete AN & Moresco MC (2012) Florística de campos de murundus do Pantanal do Araguaia. Acta Botanica Brasilica 26: 181-196. encontraram elevado número de gêneros representados apenas por uma espécie em campos de murundus de Mato Grosso e no presente estudo, encontramos 18 gêneros representados por apenas uma espécie (Tab. 2 - disponibilizada no link <https://figshare.com/s/59e753cd680cfc39f3ed>). Portanto, essa parece ser mais uma característica importante de campos de murundus e que pode indicar que esta fitofisionomia savânica comporta elevada riqueza de espécies (Resende et al. 2004Resende ILM, Araújo GMA, Oliveira APA, Oliveira AP & Ávila Júnior RS (2004) A comunidade vegetal e as características abióticas de um campo de murundu em Uberlândia MG. Acta Botanica Brasilica 18: 9-17.; Marimon et al. 2012; Pinto et al. 2014Pinto JRR, Mews HA, Jancoski HS, Marimon BS & Bomfim BO (2014) Woody vegetation dynamics in a floodplain campo de murundus in central Brazil. Acta Botanica Brasilica 28: 519-526.).
Asteraceae está entre as principais famílias com plantas invasoras no Brasil (Souza & Lorenzi 2012Souza VC & Lorenzi H (2012) Botânica sistemática: guia ilustrado para identificação das famílias de angiospermas da flora brasileira baseado em APG III. 3ª ed. Instituto Plantarum, Nova Odessa. 768p.) e a presença de sete espécies alóctones para o Cerrado desta família no CMBV (Tab. 2 - disponibilizada no link <https://figshare.com/s/59e753cd680cfc39f3ed>) é provavelmente devido à influência da ação antrópica das áreas circunvizinhas destinadas a agricultura. Certamente o contato com a borda propiciou a invasão de espécies exóticas, como citado por Pivello et al. (1999aPivello VR, Carvalho VMC, Lopes PF, Peccinini AA & Rosso S (1999a) Abundance and distribution of native and alien grasses in a “cerrado” (Brazilian savanna) Biological Reserve. Biotropica 31: 71-82., b)Pivello VR, Shida CN & Meirelles ST (1999b) Alien grasses in Brazilian savannas: a threat to the biodiversity. Biodiversity and Conservation 8: 1281-1294., Batalha & Mantovani (2001)Batalha MA & Mantovani W (2001) Floristic composition of the Cerrado in the Pé-de-Gigante reserve (Santa Rita do Passa Quatro Southeastern Brazil). Acta Botanica Brasilica 15: 289-32. e Araújo et al. (2002)Araújo GM, Barbosa AA, Arantes AA & Amaral AF (2002) Composição florística de veredas no Município de Uberlândia MG. Revista Brasileira de Botânica 25: 475-493. para outras espécies invasoras, pois durante as coletas no CMBV observamos que as invasoras ocorriam predominantemente próximo às bordas onde estão localizados os drenos.
No presente estudo encontramos pouco mais de duas vezes o número de espécies de Asteraceae registrado por Marimon et al. (2012)Marimon BS, Marimon-Junior BH, Mews HA, Jancoski HS, Franczak DD, Lima HS, Lenza E, Rossete AN & Moresco MC (2012) Florística de campos de murundus do Pantanal do Araguaia. Acta Botanica Brasilica 26: 181-196. e duas espécies apenas (Ayapana amygdalina (Lam.) R.M.King & H.Rob. e Chrysolaena obovata (Less.) Dematt.) são comuns aos dois levantamentos. Considerando a baixa similaridade de espécies de Asteraceae entre as áreas, assim como a nova espécie de Baccharis e a nova ocorrência de Disynaphia senecionidea encontradas no CMBV, estas informações fornecem indícios de que cada área estudada apresenta flora peculiar.
A riqueza de espécies de Asteraceae no CMBV representa aproximadamente 3% do total de espécies da família no Cerrado (Mendonça et al. 2008Mendonça RC, Felfili JM, Walter BMT, Silva Jr. MC, Rezende AV, Filgueiras TS, Nogueira PE & Fagg CW (2008) Flora vascular do bioma Cerrado: checklist com 12.356 espécies. In: Sano SM, Almeida SP & Ribeiro JF (eds.) Cerrado: ecologia e flora. Embrapa Cerrados, Planaltina. Pp. 421-1279.). Considerando o número de espécies deste estudo, acrescido com as oitos espécies de Asteraceae identificadas por Marimon et al. (2012)Marimon BS, Marimon-Junior BH, Mews HA, Jancoski HS, Franczak DD, Lima HS, Lenza E, Rossete AN & Moresco MC (2012) Florística de campos de murundus do Pantanal do Araguaia. Acta Botanica Brasilica 26: 181-196., a fisionomia campos de murundus congrega 3,9% da riqueza de Asteraceae do Cerrado. Assim, a riqueza total de espécies de ambos estudos combinados também representa mais de 2% de espécies da família Asteraceae no Brasil. Considerando que o Brasil agrega 7,5% da riqueza de espécies da família no mundo e que é uma das famílias com maior riqueza de espécies nos campos de murundus em Mato Grosso (Marimon et al. 2012Marimon BS, Marimon-Junior BH, Mews HA, Jancoski HS, Franczak DD, Lima HS, Lenza E, Rossete AN & Moresco MC (2012) Florística de campos de murundus do Pantanal do Araguaia. Acta Botanica Brasilica 26: 181-196.), isto torna a importância da conservação dos campos de murundus mais proeminente para manutenção da riqueza de espécies de Asteraceae no Cerrado, no Brasil e concomitantemente no mundo.
A análise das espécies autóctones da família Asteraceae do CMBV citadas para o Brasil (BFG 2018) mostrou que Chresta sphaerocephala DC., Disynaphia senecionidea (Baker) R.M.King & H.Rob., Elephantopus micropappus Less., Eremanthus glomerulatus Less., Heterocondylus pumilus (Gardner) R.M.King & H.Rob., Baccharis sp. nov., Aspilia foliacea Baker e Chromolaena horminoides DC. são exclusivas do Brasil (Tab. 2 - disponibilizada no link <https://figshare.com/s/59e753cd680cfc39f3ed>), sendo as seis primeiras com distribuição restrita ao Cerrado. Embora Aldama squalida (S.Moore) E.E.Schill. & Panero e Lepidaploa remotiflora (Rich.) H.Rob. não sejam exclusivas do Brasil, apresentam distribuição restrita ao Cerrado. Marimon et al. (2012)Marimon BS, Marimon-Junior BH, Mews HA, Jancoski HS, Franczak DD, Lima HS, Lenza E, Rossete AN & Moresco MC (2012) Florística de campos de murundus do Pantanal do Araguaia. Acta Botanica Brasilica 26: 181-196. encontraram relevante número de espécies (47) exclusivas do Brasil em campos de murundus de Mato Grosso, evidenciando que este é um importante ecossistema por comportar muitas espécies exclusivas. As demais 20 espécies também autóctones do Cerrado registradas neste estudo não são exclusivas do Brasil e são de ampla distribuição (BFG 2018). De acordo com BFG (2018), Achyrocline satureioides (Lam.) DC. não ocorre no estado de Goiás, apesar de ocorrer no Cerrado. Entretanto, há registros desta espécie para Goiás e Distrito Federal na Plataforma Florescer (Florescer 2014Florescer (2014) Plataforma Florescer. Disponível em <http://www.florescer.unb.br/bol/>. Acesso em 30 novembro 2014.
http://www.florescer.unb.br/bol/...
).
Dentre as espécies deste estudo, nenhuma foi mencionada como de ocorrência em campos de murundus por BFG (2018) e esta discriminação foi realizada apenas para Ageratum fastigiatum (Gardner) R.M.King & H.Rob. no checklist de Mendonça et al. (2008)Mendonça RC, Felfili JM, Walter BMT, Silva Jr. MC, Rezende AV, Filgueiras TS, Nogueira PE & Fagg CW (2008) Flora vascular do bioma Cerrado: checklist com 12.356 espécies. In: Sano SM, Almeida SP & Ribeiro JF (eds.) Cerrado: ecologia e flora. Embrapa Cerrados, Planaltina. Pp. 421-1279. para espécies nativas do Cerrado. Marimon et al. (2012)Marimon BS, Marimon-Junior BH, Mews HA, Jancoski HS, Franczak DD, Lima HS, Lenza E, Rossete AN & Moresco MC (2012) Florística de campos de murundus do Pantanal do Araguaia. Acta Botanica Brasilica 26: 181-196. também encontram baixo número de espécies (18) que foram citadas como de ocorrência em campos de murundus de um total de 232 espécies arbóreas, arbustivas, subarbustivas ou herbáceas relacionadas na listagem do Cerrado (Mendonça et al. 2008Mendonça RC, Felfili JM, Walter BMT, Silva Jr. MC, Rezende AV, Filgueiras TS, Nogueira PE & Fagg CW (2008) Flora vascular do bioma Cerrado: checklist com 12.356 espécies. In: Sano SM, Almeida SP & Ribeiro JF (eds.) Cerrado: ecologia e flora. Embrapa Cerrados, Planaltina. Pp. 421-1279.). Estas informações reforçam que a flora da fitofisionomia é pouco estudada e conhecida. Portanto, existe a necessidade de investir na realização de inventários florísticos em campos de murundus, principalmente para o componente herbáceo-subarbustivo, que geralmente é menos estudado que o componente arbóreo-arbustivo. Como mencionado por Marimon et al. (2012)Marimon BS, Marimon-Junior BH, Mews HA, Jancoski HS, Franczak DD, Lima HS, Lenza E, Rossete AN & Moresco MC (2012) Florística de campos de murundus do Pantanal do Araguaia. Acta Botanica Brasilica 26: 181-196., é essencial a inclusão do estrato herbáceo-subarbustivo nos levantamentos em campos de murundus com o intuito de agregar conhecimento acerca desta fitofisionomia e do Cerrado, como subsídio à sua conservação.
A comparação entre as espécies de Asteraceae autóctones do presente estudo com as espécies de outros levantamentos florísticos realizados no Cerrado mostra que o levantamento de Hattori & Nakajima (2011)Hattori EKO & Nakajima JN (2011) A família Asteraceae na Reserva Ecológica do Panga Uberlândia Minas Gerais Brasil. Hoehnea 38: 165-214., IBGE (2004)IBGE - Instituto Brasileiro de Geografia e Estatística (2004) Reserva Ecológica do IBGE: Ambiente e plantas vasculares. IBGE, Brasília. 73p., Almeida (2008)Almeida GSS (2008) Asteraceae Dumort. nos campos rupestres do Parque Estadual do Itacolomi Minas Gerais Brasil. Tese de Doutorado. Universidade Federal de Viçosa, Viçosa. 365p. e Nakajima & Semir (2001)Nakajima JN & Semir J (2001) Asteraceae do parque Nacional da Serra da Canastra Minas Gerais Brasil. Revista Brasileira de Botânica 24: 471-478. apresentam maior semelhança florística (68%, 68%, 55%, 45%, respectivamente) com o presente estudo (Tab. 1). Isto pode ser devido à variedade de fisionomias do Cerrado em que estes estudos foram conduzidos. No entanto, as diferenças em números de espécies entre todas as áreas comparadas com a presente análise podem ser explicadas pela variação no tamanho da área, quantidade de fisionomias amostradas, duração e periodicidade de coleta (Nakajima & Semir 2001Nakajima JN & Semir J (2001) Asteraceae do parque Nacional da Serra da Canastra Minas Gerais Brasil. Revista Brasileira de Botânica 24: 471-478.).
As espécies mais comuns entre o presente estudo e outros estudos são Achyrocline satureioides (Lam.) DC., presente em 13 (81%) levantamentos, Achyrocline alata DC. e Ayapana amygdalina (Lam.) R.M.King & H.Rob. (11; 69%, respectivamente), Mikania officinalis Mart. e Chromolaena laevigata (Lam.) R.M.King & H.Rob. (10; 62%, respectivamente), Ageratum fastigiatum (Gardner) R.M.King & H.Rob., Aspilia foliacea Baker e Praxelis kleinioides (Kunth) Sch. Bip. (9; 56%, respectivamente) e Erechtites hieraciifolius Raf. ex DC. e Eremanthus glomerulatus Less. (8; 50%). Isso sugere que estas espécies possuem ampla distribuição ao longo do Cerrado.
Três espécies foram inventariadas em três estudos: Chrysolaena obovata (Less.) Dematt., (Nakajima & Semir 2001; IBGE 2004; Medeiros et al. 2012Medeiros MB, Walter BMT, Silva GP, Gomes BG, Lima ILP, Silva SR, Moser P, Oliveira WL & Cavalcanti TB (2012) Vascular flora of the Tocantins River Middle Basin Brazil. Check List 8: 852-885.), Ichthyothere terminalis S.F.Blake (Munhoz & Proença 1998Munhoz CBR & Proença C (1998) Composição florística no município de Alto Paraíso de Goiás na Chapada dos Veadeiros. Boletim do Herbário Ezechias Paulo Heringer 3: 102-150.; IBGE 2004IBGE - Instituto Brasileiro de Geografia e Estatística (2004) Reserva Ecológica do IBGE: Ambiente e plantas vasculares. IBGE, Brasília. 73p.; Medeiros et al. 2012Medeiros MB, Walter BMT, Silva GP, Gomes BG, Lima ILP, Silva SR, Moser P, Oliveira WL & Cavalcanti TB (2012) Vascular flora of the Tocantins River Middle Basin Brazil. Check List 8: 852-885.) e Raulinoreitzia crenulata (Spreng.) R.M.King & H.Rob (IBGE 2004IBGE - Instituto Brasileiro de Geografia e Estatística (2004) Reserva Ecológica do IBGE: Ambiente e plantas vasculares. IBGE, Brasília. 73p.; Hattori & Nakajima 2011Hattori EKO & Nakajima JN (2011) A família Asteraceae na Reserva Ecológica do Panga Uberlândia Minas Gerais Brasil. Hoehnea 38: 165-214.; Nakajima & Semir 2001Nakajima JN & Semir J (2001) Asteraceae do parque Nacional da Serra da Canastra Minas Gerais Brasil. Revista Brasileira de Botânica 24: 471-478.). Duas espécies foram citadas em dois estudos: Lepidaploa remotiflora (Rich.) H.Rob (Almeida 2008Almeida GSS (2008) Asteraceae Dumort. nos campos rupestres do Parque Estadual do Itacolomi Minas Gerais Brasil. Tese de Doutorado. Universidade Federal de Viçosa, Viçosa. 365p.; Medeiros et al. 2012Medeiros MB, Walter BMT, Silva GP, Gomes BG, Lima ILP, Silva SR, Moser P, Oliveira WL & Cavalcanti TB (2012) Vascular flora of the Tocantins River Middle Basin Brazil. Check List 8: 852-885.) e Heterocondylus pumilus (Gardner) R.M.King & H.Rob. (Almeida 2008Almeida GSS (2008) Asteraceae Dumort. nos campos rupestres do Parque Estadual do Itacolomi Minas Gerais Brasil. Tese de Doutorado. Universidade Federal de Viçosa, Viçosa. 365p.; Reis 2013Reis GH (2013) Avaliação de diversidade de Asteraceae dos campos de cerrados rupestres das Serras da Bocaina e de Carrancas, Minas Gerais, Brasil. Dissertação de Mestrado. Universidade Federal de Lavras, Lavras. 96p.). Chromolaena ivifolia (L.) R.M.King & H.Rob. não foi encontrada em nenhum dos estudos e duas espécies foram registradas somente em um estudo cada: Aldama squalida (S.Moore) E.E.Schill. & Panero foi reportada somente em IBGE (2004)IBGE - Instituto Brasileiro de Geografia e Estatística (2004) Reserva Ecológica do IBGE: Ambiente e plantas vasculares. IBGE, Brasília. 73p. e Pterocaulon lanatum Kuntze foi citada apenas em Hattori & Nakajima (2011)Hattori EKO & Nakajima JN (2011) A família Asteraceae na Reserva Ecológica do Panga Uberlândia Minas Gerais Brasil. Hoehnea 38: 165-214.. Apesar de terem sido registradas em poucos ou em nenhum estudo, estas espécies são de ampla valência ecológica no Cerrado e/ou outros domínios (BFG 2018).
Por outro lado, Disynaphia senecionidea (Baker) R.M.King & H.Rob. foi citada em apenas três estudos (IBGE 2004IBGE - Instituto Brasileiro de Geografia e Estatística (2004) Reserva Ecológica do IBGE: Ambiente e plantas vasculares. IBGE, Brasília. 73p.; Almeida 2008Almeida GSS (2008) Asteraceae Dumort. nos campos rupestres do Parque Estadual do Itacolomi Minas Gerais Brasil. Tese de Doutorado. Universidade Federal de Viçosa, Viçosa. 365p.; Hattori & Nakajima 2011Hattori EKO & Nakajima JN (2011) A família Asteraceae na Reserva Ecológica do Panga Uberlândia Minas Gerais Brasil. Hoehnea 38: 165-214.), pois trata-se de uma espécies mais restritiva (BGF 2018). Assim, o fato desta espécie não ter sido ou ser relatada em poucos inventários florísticos do Cerrado sugere que é uma espécie incomum, provavelmente com populações reduzidas. Como não há informações suficientes na literatura sobre sua ocorrência, não se sabe se está ameaçada.
Este estudo é o primeiro realizado para a família Asteraceae em campo de murundus de Goiás e considerando que a ocorrência de poucas espécies era conhecida nesta fitofisionomia, constitui-se em uma importante contribuição ao ampliar as informações sobre o hábitat das espécies. Além disso, evidencia a carência de estudos florísticos no estrato herbáceo-subarbustivo em fisionomias pouco estudadas, como campo de murundus. A investigação destas fisionomias é necessária para ampliação do conhecimento da biodiversidade, pois podem funcionar como importante reservatório de espécies pouco conhecidas ou endêmicas e para táxons novos para a ciência. Assim, a conservação dos campos de murundus é extremamente relevante para o aumento do conhecimento e para a manutenção da biodiversidade local, regional e mundial.
Agradecimentos
Ao CNPq e FAPEG, no âmbito do Projeto PELD Jataí - Pesquisas Ecológicas de Longa Duração (Processo Nº2012/10267001108) e à FAPEG (Processo Nº2009/10267000382), o apoio financeiro; ao CNPq, a bolsa Produtividade em Pesquisa a Frederico Augusto Guimarães Guilherme.
Referências
- Almeida AM, Fonseca CR, Prado PI, Almeida-Neto M, Diniz S, Kubota U, Braun MR, Raimundo RG, Anjos LA, Mendonça TG, Futada SM & Lewinsohn TM (2005) Diversidade de Asteraceae em Cerrado de São Paulo. Biota Neotropica 5: 1-17.
- Almeida GSS (2008) Asteraceae Dumort. nos campos rupestres do Parque Estadual do Itacolomi Minas Gerais Brasil. Tese de Doutorado. Universidade Federal de Viçosa, Viçosa. 365p.
- Araújo GM, Barbosa AA, Arantes AA & Amaral AF (2002) Composição florística de veredas no Município de Uberlândia MG. Revista Brasileira de Botânica 25: 475-493.
- Araújo-Neto MD, Furley PA, Haridasan M & Johnson CE (1986) The Murundus of the Cerrado region of Central Brazil. Journal of Tropical Ecology 2: 17-35.
- Baker JG (1873) Compositae I: Vernoniaceae. In: Martius CFP & Eichler AG (eds.) Flora brasiliensis Monachii, Lipsiae. Vol. 6. Pars 2. Pp. 1-180.
- Baker JG (1876) Compositae II: Eupatoriaceae. In: Martius CFP & Eichler, AG (eds.) Flora brasiliensis Monachii, Lipsiae. Vol. 6. Pars 2. Pp. 181-376.
- Baker JG (1882) Compositae III: Asteroideae & Inuloideae. In: Martius CFP & Eichler AG (eds.) Flora brasiliensis Monachii, Lipsiae. Vol. 6. Pars 2. Pp. 1-134.
- Baker JG (1884) Compositae IV: Helianthoideae - Mutisiaceae. In: Martius CFP & Eichler AG (eds.) Flora brasiliensis Monachii. Vol. 6. Pars 3. Pp. 135-398.
- Barroso GM, Peixoto AL, Costa CG, Ichaso CLF, Guimarães EF & Lima HC (1986) Sistemática de angiospermas do Brasil. Vol. 3. Imprensa Universitária da Universidade Federal de Viçosa, Viçosa. 326 p.
- Batalha MA & Mantovani W (2001) Floristic composition of the Cerrado in the Pé-de-Gigante reserve (Santa Rita do Passa Quatro Southeastern Brazil). Acta Botanica Brasilica 15: 289-32.
- Bernacci LCB & Leitão-Filho HF (1996) Flora fanerogâmica da fazenda São Vicente Campinas-SP. Revista Brasileira de Botânica 19: 149-164.
- BFG - The Brazil Flora Group (2015) Growing knowledge: an overview of seed plant diversity in Brazil. Rodriguésia 66: 1085-1113.
- Brandão M, Gavilanes ML, Laca-Buendia JP, Cunha LHS & Macedo JF (1989) Flora da Serra de Itabirito, Minas Gerais - Primeira contribuição. Acta Botanica Brasilica 3: 237-251.
- Cabrera AL (1974) Compositae. In: Burkart A (ed.) Flora ilustrada de Entre Rios 6: 106-540.
- Cabrera AL (1978) Compositae. In: Cabrera AL (ed.) Flora de la Provincia de Jujuy - Republica Argentina 10: 1-726.
- Castro-Júnior PR (2002) Dinâmica da água em campos de murundus do Planalto dos Parecis. Tese de doutorado. Universidade de São Paulo, São Paulo. 193p.
- Ferreira SC, Carvalho-Okano RM & Nakajima JN (2009) A família Asteraceae em um fragmento Florestal, Viçosa, Minas Gerais, Brasil. Rodriguésia 60: 903−942.
- Filgueiras TS, Nogueira PE, Brochado AL & Guala GF (1994) Caminhamento: um método expedito para levantamentos florísticos qualitativos. Cadernos de Geociências 12: 39-43.
- Flora do Brasil 2020 em construção. Jardim Botânico do Rio de Janeiro. Disponível em <http://floradobrasil.jbrj.gov.br>. Acesso em 25 fevereiro 2018.
» http://floradobrasil.jbrj.gov.br - Florescer (2014) Plataforma Florescer. Disponível em <http://www.florescer.unb.br/bol/>. Acesso em 30 novembro 2014.
» http://www.florescer.unb.br/bol/ - Funk VA, Susanna A, Stuessy TF & Robinson H (2009) Classication of Compositae. In: Funk VA, Susanna A, Stuessy TF & Bayer RJ (eds.) Systematics, evolution, and biogeography of Compositae. IAPT, Vienna. Pp. 171-176.
- Furley PA (1986) Classification and distribution of murundus in the Cerrado of central Brazil. Journal of Biogeography 13: 265-268.
- Gomes Filho RR, Silva JH, Paulino HB, Carneiro MAC & Costa CAG (2011) Velocidade de infiltração da água num plintossolo háplico de campo de murundu sob um cronossequência de interferência antrópica. Revista Brasileira de Agricultura Irrigada 5: 245-253.
- Hattori EKO & Nakajima JN (2008) A família Asteraceae na Estação de Pesquisa e Desenvolvimento Ambiental Galheiro Perdizes Minas Gerais Brasil. Rodriguésia 59: 687-749.
- Hattori EKO & Nakajima JN (2011) A família Asteraceae na Reserva Ecológica do Panga Uberlândia Minas Gerais Brasil. Hoehnea 38: 165-214.
- IBGE - Instituto Brasileiro de Geografia e Estatística (2004) Reserva Ecológica do IBGE: Ambiente e plantas vasculares. IBGE, Brasília. 73p.
- Giulietti AM, Menezes NL, Pirani JR & Wanderley MGL (1987) Flora da Serra do Cipó, Minas Gerais: caracterização e lista de espécies. Boletim de Botânica, Universidade de São Paulo 9: 1-151.
- Mantovani W & Martins FR (1993) Florística da Reserva Biológica de Moji-Guaçu SP. Revista Brasileira Botanica 7: 33-60.
- Maricato HS, Pereira FC, Souza LF, Gomes DC & Guilherme FAG (2017) Aspectos físicos e estrutura da vegetação lenhosa em três campos de murundus no sudoeste goiano. Revista Brasileira de Biociências 15: 169-177.
- Marimon BS & Lima ES (2001) Caracterização fitofisionômica e levantamento florístico preliminar no pantanal dos rios Mortes-Araguaia. Acta Botanica Brasilica 15: 213-229.
- Marimon BS, Marimon-Junior BH, Mews HA, Jancoski HS, Franczak DD, Lima HS, Lenza E, Rossete AN & Moresco MC (2012) Florística de campos de murundus do Pantanal do Araguaia. Acta Botanica Brasilica 26: 181-196.
- Medeiros MB, Walter BMT, Silva GP, Gomes BG, Lima ILP, Silva SR, Moser P, Oliveira WL & Cavalcanti TB (2012) Vascular flora of the Tocantins River Middle Basin Brazil. Check List 8: 852-885.
- Mendonça RC, Felfili JM, Walter BMT, Silva Jr. MC, Rezende AV, Filgueiras TS, Nogueira PE & Fagg CW (2008) Flora vascular do bioma Cerrado: checklist com 12.356 espécies. In: Sano SM, Almeida SP & Ribeiro JF (eds.) Cerrado: ecologia e flora. Embrapa Cerrados, Planaltina. Pp. 421-1279.
- Moreira GL & Teles AM (2014) A tribo Vernonieae (Asteraceae) na Serra Dourada, Goiás, Brasil. Iheringia, Série Botânica 69: 357-385.
- Munhoz CBR & Felfili JM (2007) Florística do estrato herbáceo-subarbustivo de um campo limpo úmido em Brasília Brasil. Biota Neotropica 7: 207-215.
- Munhoz CBR & Proença C (1998) Composição florística no município de Alto Paraíso de Goiás na Chapada dos Veadeiros. Boletim do Herbário Ezechias Paulo Heringer 3: 102-150.
- Nakajima JN & Semir J (2001) Asteraceae do parque Nacional da Serra da Canastra Minas Gerais Brasil. Revista Brasileira de Botânica 24: 471-478.
- Oliveira-Filho AT (1992a) Floodplain ‘murundus’ of Central Brazil: evidence for the termite-origin hypothesis. Journal of Tropical Ecology 8: 1-19.
- Oliveira-Filho AT (1992b) The vegetation of Brazilian “murundus”: the island-efect on the plant community. Journal of Tropical Ecology 8: 465-486.
- Oliveira Filho AT & Martins FR (1991) A comparative study of five cerrado areas in southern Mato Grosso Brazil. Edinburgh Journal of Botany 48: 37-332.
- Pinto JRR, Mews HA, Jancoski HS, Marimon BS & Bomfim BO (2014) Woody vegetation dynamics in a floodplain campo de murundus in central Brazil. Acta Botanica Brasilica 28: 519-526.
- Pivello VR, Carvalho VMC, Lopes PF, Peccinini AA & Rosso S (1999a) Abundance and distribution of native and alien grasses in a “cerrado” (Brazilian savanna) Biological Reserve. Biotropica 31: 71-82.
- Pivello VR, Shida CN & Meirelles ST (1999b) Alien grasses in Brazilian savannas: a threat to the biodiversity. Biodiversity and Conservation 8: 1281-1294.
- Ratter JA, Ribeiro JF & Bridgewater S (1997) The Brazilian Cerrado vegetation and threats to its biodiversity. Annal of Botany 8: 223-230.
- Reis GH (2013) Avaliação de diversidade de Asteraceae dos campos de cerrados rupestres das Serras da Bocaina e de Carrancas, Minas Gerais, Brasil. Dissertação de Mestrado. Universidade Federal de Lavras, Lavras. 96p.
- Resende ILM, Araújo GMA, Oliveira APA, Oliveira AP & Ávila Júnior RS (2004) A comunidade vegetal e as características abióticas de um campo de murundu em Uberlândia MG. Acta Botanica Brasilica 18: 9-17.
- Ribeiro JF & Walter BMT (2008) As principais fitofisionomias do Bioma Cerrado. In: Sano SM, Almeida SP & Ribeiro JF (eds.) Cerrado: ecologia e flora. Embrapa Cerrados, Planaltina. Pp. 151-212.
- Ribeiro RN & Teles AM (2015) Eupatorieae (Asteraceae) no Parque Estadual da Serra Dourada, Goiás, Brasil. Rodriguésia 66: 887-903.
- Roveratti J (2008) Flora vascular do cerrado sensu stricto do Parque Nacional de Brasília Distrito Federal Brasil e chave para identificação das espécies. Dissertação de Mestrado. Universidade de Brasília, Brasília. 93p.
- Schneider MO & Silva DB (1991) Estrutura pedológica e dinâmica hídrica do “covoal” do Córrego da Fortaleza. Sociedade & Natureza 3: 75-89.
- Silva JG (2010) Índice de qualidade de um Plintossolo Argilúvico para fins agrícolas no Cerrado do Sudoeste de Goiás. Dissertação de Mestrado. Universidade Federal de Goiás, Jataí. 59p.
- Silva FAM, Assad ED, Evangelista BA (2008) Caracterização climática do bioma Cerrado. In: Sano SM, Almeida SP & Ribeiro JF (eds.) Cerrado: ecologia e flora. Embrapa, Planaltina. Pp. 69-88.
- Souza VC & Lorenzi H (2012) Botânica sistemática: guia ilustrado para identificação das famílias de angiospermas da flora brasileira baseado em APG III. 3ª ed. Instituto Plantarum, Nova Odessa. 768p.
- Teles AM & Stehmann JR (2016) A tribo Senecioneae (Asteraceae) em Minas Gerais, Brasil. Rodriguésia 67: 455-487.
Editado por
Datas de Publicação
-
Publicação nesta coleção
25 Abr 2019 -
Data do Fascículo
2019
Histórico
-
Recebido
13 Fev 2017 -
Aceito
01 Mar 2018