Resumos
INTRODUÇÃO: O insucesso do tratamento clínico do diabete melito tipo 2 (DM2) aumentou o interesse em cirurgia metabólica, sendo considerada alternativa promissora no controle de diabéticos com ou sem obesidade. Todavia, ainda não há seguimento em longo prazo para se avaliar a duração da remissão da doença, cuja recidiva pode estar associada ao reganho de peso. OBJETIVOS: 1) Descrever os resultados de pacientes com DM2 e IMC <30 e <35 kg/m², submetidos aos seguintes tipos de operações metabólicas: interposição ileal e gastrectomia vertical, derivação gástrica em Y-de-Roux (DGYR), banda gástrica ajustável, exclusão duodeno-jejunal e bypass duodenojejunal; 2) avaliar a possível ocorrência de recidiva do diabete após reganho de peso em longo prazo. MÉTODO: Foi realizada revisão expositiva e histórica da literatura sobre cirurgia metabólica em pacientes com DM2 e IMC <30 e <35 kg/m², e revisão sistemática sobre a associação entre recidiva da doença e reganho de peso após cirurgia bariátrica. RESULTADO: Após análise de 188 artigos publicados no Medline até 2010, foram selecionados três estudos, com 269 pacientes submetidos à DGYR, com IMC pré-operatório entre 37 e 60 kg/m² e com seguimento de três a 16 anos. CONCLUSÕES: 1) Dois estudos mostraram que o reganho de peso está associado à recidiva do diabete, enquanto o terceiro não confirma este fato, na comparação entre o grupo com e sem reganho; 2) a cirurgia metabólica vem apresentando adequado controle do diabete em obesos grau I; todavia, o grupo não obeso ainda aguarda avaliação em longo prazo, considerando o risco de recidiva associado ao reganho de peso.
Cirurgia bariátrica; Diabete melito; Recidiva; Ganho de peso
INTRODUCTION: The poor success of clinical treatment of Type 2 Diabetes Mellitus (T2DM2) increased interest in metabolic surgery, which has been considered a promising alternative for the control of obese or non-obese diabetics. However, there is still no long-term follow-up to evaluate the duration of diabetes remission, and if weight regain would be associated to recurrence. AIM: 1) To describe the results of diabetic patients with a BMI < 30 and < 35 kg/m² submitted to the following types of metabolic surgery: ileal interposition and sleeve gastrectomy, Roux-en-Y gastric bypass (RYGB), adjustable gastric banding, duodeno-jejunal exclusion and duodeno-jejunal bypass; 2) to evaluate the possible relapse of diabetes after occurrence of weight regain on long-term after bariatric surgery. METHOD: An expositive and historical literature review about metabolic surgery in diabetic patients with BMI < 30 and < 35 kg/m² was conducted, and systematic review of the association between disease relapse and weight regain after bariatric surgery. RESULTS: After analysis of 188 published papers on Medline until 2010, three papers were selected, which included 269 patients who underwent RYGB. Pre-operatory BMI was between 37 and 60 kg/m² and follow-up of three to 16 years. CONCLUSIONS: 1) Two studies showed association between weight regain and recurrence of type 2 diabetes, while the third did not show this association when comparing groups with and without weight regain; 2) metabolic surgery has shown adequate control of T2DM2 in class I obese subjects; however, the non-obese group still need a long-term evaluation, considering the risk of diabetes recurrence when after weight regain.
Bariatric surgery; Diabetes Mellitus; Recurrence; Weight regain
ARTIGO DE REVISÃO
Cirurgia metabólica, reganho de peso e recidiva do diabete
Josemberg M. CamposI; Daniel C. LinsI,II; Lyz B. SilvaI; José Guido C. Araujo-JuniorI; Jorge L. M. ZeveIII; Álvaro A. B. FerrazI
ITrabalho realizado no Serviço de Cirurgia Geral, Universidade Federal de Pernambuco, Recife, PE
IIDepartamento de Endocrinologia, Hospital Oswaldo Cruz, Faculdade de Ciências Médicas, Universidade de Pernambuco, Recife, PE
IIIFaculdade de Medicina, Universidade Federal do Tocantins, Palmas, TO, Brasil
Correspondência Correspondência: Josemberg M. Campos E-mail: josembergcampos@gmail.com
RESUMO
INTRODUÇÃO: O insucesso do tratamento clínico do diabete melito tipo 2 (DM2) aumentou o interesse em cirurgia metabólica, sendo considerada alternativa promissora no controle de diabéticos com ou sem obesidade. Todavia, ainda não há seguimento em longo prazo para se avaliar a duração da remissão da doença, cuja recidiva pode estar associada ao reganho de peso.
OBJETIVOS: 1) Descrever os resultados de pacientes com DM2 e IMC <30 e <35 kg/m2, submetidos aos seguintes tipos de operações metabólicas: interposição ileal e gastrectomia vertical, derivação gástrica em Y-de-Roux (DGYR), banda gástrica ajustável, exclusão duodeno-jejunal e bypass duodenojejunal; 2) avaliar a possível ocorrência de recidiva do diabete após reganho de peso em longo prazo.
MÉTODO: Foi realizada revisão expositiva e histórica da literatura sobre cirurgia metabólica em pacientes com DM2 e IMC <30 e <35 kg/m2, e revisão sistemática sobre a associação entre recidiva da doença e reganho de peso após cirurgia bariátrica.
RESULTADO: Após análise de 188 artigos publicados no Medline até 2010, foram selecionados três estudos, com 269 pacientes submetidos à DGYR, com IMC pré-operatório entre 37 e 60 kg/m2 e com seguimento de três a 16 anos.
CONCLUSÕES: 1) Dois estudos mostraram que o reganho de peso está associado à recidiva do diabete, enquanto o terceiro não confirma este fato, na comparação entre o grupo com e sem reganho; 2) a cirurgia metabólica vem apresentando adequado controle do diabete em obesos grau I; todavia, o grupo não obeso ainda aguarda avaliação em longo prazo, considerando o risco de recidiva associado ao reganho de peso.
Descritores: Cirurgia bariátrica. Diabete melito. Recidiva. Ganho de peso.
INTRODUÇÃO
Há projeção de que o número de indivíduos diagnosticados com diabete melito tipo 2 (DM2) irá aumentar em 198%14, podendo levar à complicações crônicas. O DM2 é mal controlado apenas com tratamento clínico e baseado na mudança de hábitos de vida e no uso de alguns medicamentos. O adequado controle glicêmico obtido após cirurgia bariátrica tem aumentado o interesse no desenvolvimento de novas técnicas; também há a possibilidade de se realizar o procedimento em pacientes que não atenderiam aos critérios de inclusão tradicionais12, 15, 17. A cirurgia tem sido proposta como opção para pacientes com obesidade grau I ou não-obesos com DM2 mal controlada.
Aproximadamente 84% dos diabéticos chegam à completa remissão após a realização da derivação gástrica em Y-de-Roux (DGYR), antes mesmo de haver perda de peso significativa.13 Há várias teorias buscando explicar os mecanismos responsáveis por este efeito, as quais serão exploradas adiante.
Apesar de haver muitos dados publicados sobre remissão do DM2 após cirurgia bariátrica, é disponível quantidade limitada de informações sobre efeitos em longo prazo, recidiva ou piora da doença após determinado período, além dos fatores associados à recidiva.
Objetiva-se apresentar uma revisão da literatura sobre cirurgia metabólica em pacientes com índice de massa corpórea (IMC) menor que 35 kg/m2, discutindo a possibilidade de se expandir as indicações da cirurgia, com foco na falta de informação de seguimento em longo prazo e os efeitos que o reganho de peso teria no DM2. Ainda apresenta-se revisão sistemática sobre a possível recidiva do DM2 associada ao reganho de peso após cirurgia bariátrica em seguimento de longo prazo, independente do IMC pré-operatório.
MÉTODOS
Foi realizada revisão expositiva e histórica da literatura sobre cirurgia metabólica e controle do diabete, em pacientes com IMC menor que 30 e 35 kg/m2. Visando executar revisão sistemática da literatura sobre recidiva da DM2 e reganho de peso, realizou-se busca simples no Medline utilizando a seguinte estratégia de busca: "bariatric surgery" or "gastric bypass" and "diabetes" and "follow-up studies", limitando para estudos em humanos, e publicados até o ano de 2011. O objetivo foi incluir artigos que reportassem e analisassem taxas de recorrência e de piora em diabéticos que haviam atingido remissão após cirurgia bariátrica, em seguimento de longo prazo, independente do IMC pré-operatório. A busca resultou em 188 estudos, e após leitura dos títulos e resumos, 182 foram excluídos. Os seis restantes tiveram seus textos completos buscados, com quatro deles sendo excluídos após leitura integral por não reportarem recorrência ou piora do diabetes. Os dois artigos incluídos serão analisados no presente estudo (Figura 1). Foram incluídos ainda dados de estudo de uma das instituições envolvidas (Serviço de Cirurgia Geral - UFPE), ainda não publicados, onde foi feita comparação da remissão do diabete entre um grupo que manteve a perda de peso e outro que reganhou o peso perdido.
Mecanismos cirúrgicos da resolução do DM2
O controle pós-operatório do diabetes é consequência direta do rearranjo na anatomia gastrointestinal, e não meramente da redução na ingestão calórica e no peso. Algumas teorias têm sido criadas para explicar os mecanismos por trás da remissão do diabetes após cirurgia bariátrica.
Hipótese da ingestão alimentar mínima e perda de peso
Considera que o controle glicêmico melhora em curto período de tempo após a operação devido à restrição de ingestão do período pós-operatório, e mantém-se quando a alimentação regular é retomada devido aos efeitos sensibilizadores de insulina da perda de peso dinâmica. Há remissão pós-operatória da DM2 rápida, e se a restrição calórica fosse o fator principal, ocorreria remissão rápida do diabete após todos os procedimentos bariátricos, o que não se mostra verdade. Esta hipótese falha em explicar a superioridade do controle glicêmico atingido após DGYR, comparado com perda de peso equivalente e advinda de dieta ou cirurgia bariátrica puramente restritiva13,21.
Hipótese do intestino distal
Sugere que a chegada mais rápida de alimentos digeridos ao final do trato gastrintestinal melhora o metabolismo de carboidratos através de aumento na secreção do glucagon-like-peptide (GLP-1) e outros peptídeos anorexigênicos. Tal teoria é baseada em experimentos como a interposição ileal, que consiste na transposição de um segmento de íleo distal para o jejuno sem ressecção gástrica ou intestinal. Em ratos, a interposição tem demonstrado ocorrência de aumento na secreção de GLP-1 e do peptídeo YY (PYY), consequentemente melhorando o controle glicêmico.4
Hipótese do intestino proximal
Sugere que o alimento desviado do duodeno e jejuno proximal evita a secreção de substâncias ainda não identificadas que promovem resistência insulínica e DM2. Rubino et al. submeteram ratos Goto-Kakizaki à derivação duodenojejunal e anastomose gastrojejunal. Tal técnica desvia a mesma porção do intestino que duodenojejunal, mas permite a passagem de alimento no intestino proximal. Os ratos submetidos à duodenojejunal alcançaram melhora na tolerância à glicose, enquanto os da gastrojejunal não demonstraram melhora no perfil glicêmico.19
Múltiplos mecanismos contribuem para a remissão do diabete após bypass intestinal. A rápida chegada de nutrientes ao intestino distal intensifica a secreção de GLP-1 e PYY, enquanto a exclusão do duodeno exerce outros efeitos anti-diabéticos.18
Cirurgia metabólica e IMC < 35 kg/m²
A eficácia da cirurgia metabólica em levar à melhoria e até a remissão da DM2 através de mecanismos que vão além da perda de peso levantou a questão de como diabéticos não obesos responderiam a tratamento cirúrgico. O primeiro estudo provando os efeitos anti-diabéticos do bypass gastrintestinal foi realizado por Rubino et al., envolvendo ratos Goto-Kakizaki diabéticos não obesos que foram submetidos a derivação duodenojejunal e alcançaram melhora na tolerância a glicose.20
Baseados na teoria do intestino distal, De Paula et al. realizaram uma combinação de interposição ileal e gastrectomia vertical no tratamento de um grupo de diabéticos com IMC<35 kg/m2. Houve descontinuação no uso de medicações hipoglicemiantes orais e insulina em 87% dos indivíduos no período pós-operatório. No entanto, a eficácia e a segurança da técnica em longo prazo continuam desconhecidos.7
Em 2006, Cohen et al. publicaram uma série de casos envolvendo 37 diabéticos não obesos mórbidos com comorbidades severas submetidos a DGYR e seguidos por 48 meses. A remissão de todas as comorbidades ocorreu em 36 pacientes e a perda de excesso de peso média foi de 81%.3 A DGYR aparentemente une os dois supostos mecanismos do controle glicêmico (intestino proximal e distal) na mesma operação.
Em outro estudo envolvendo amostra pequena de pacientes diabéticos com IMC entre 30 e 35 kg/m2, o tratamento com banda gástrica ajustável foi estatisticamente mais eficaz na remissão da DM2 do que o tratamento clínico. Este grupo perdeu mais peso e alcançou 73% de normalização de glicemia, comparado a 13% no grupo do tratamento clínico, em seguimento de dois anos.9
Entre a experiência dos autores deste trabalho, De Sá et al. analisaram 27 pacientes submetidos à DGYR para o tratamento do DM2 descontrolado, com seguimento médio de 20 meses; houve redução de 23% no peso médio e IMC. A perda de excesso de peso foi de 94.5%, e o menor IMC foi 20,3 kg/m2. Vinte pacientes (74%) descontinuaram o uso de todas as medicações hipoglicemiantes. Treze (48%) alcançaram remissão do DM2 e 20 (74%) alcançaram controle glicêmico sem medicações. Todos exibiram melhora nos níveis glicêmicos quando comparados ao período pré-operatório. O tipo de medicação utilizado no período pré-operatório ou peso prévio não afetou a remissão do diabete e controle glicêmico.5
Choi et al. compararam 66 pacientes com IMC entre 30-35 kg/m2 e comorbidades ou com IMC 35-40 kg/m2 sem comorbidades com 438 pacientes com critérios de inclusão tradicionais que haviam sido submetidos à banda gástrica ajustável por via laparoscópica. Os resultados evidenciaram que a perda de peso em curto prazo, complicações e resolução de comorbidades nas duas populações foram similares, demonstrando que a banda gástrica ajustável é segura e eficaz para pacientes com IMC mais baixos.2
Um artigo de revisão analisou 16 estudos envolvendo um total de 343 diabéticos com IMC<35 kg/m2 submetidos a algum tipo de cirurgia bariátrica com o intuito de tratar o DM2. Dos 343 indivíduos, 85,3% conseguiram manter glicemias de jejum próximas ao normal e hemoglobina glicada normais sem uso de medicações. A redução do IMC e resolução do DM2 foram mais pronunciadas em procedimentos disabsortivos/restritivos, e em pacientes com IMC de 3035 kg/m2, quando comparados aqueles com IMC<30 kg/m2. Houve baixa taxa de complicação e mortalidade operatória (0,29%). A maioria dos pacientes com baixo IMC alcançaram resolução laboratorial e clínica do DM2 sem redução inapropriada do peso. No entanto, não foi possível realizar metanálise devido ao limitado número de estudos e indivíduos envolvidos e à falta de uniformidade nos dados reportados.10
Cirurgia metabólica e IMC < 30 kg/m2
Em humanos, Cohen et al. demonstraram que a derivação duodenojejunal normalizou a glicemia em dois pacientes no período pós-operatório precoce.3 Geloneze et al. selecionaram 12 pacientes para serem submetidos à exclusão duodenojejunal aberta, e compará-los a um grupo controle semelhante em tratamento clínico padrão. Todos tinham sobrepeso, e eram diabéticos em uso de insulina. Após 24 semanas, dois dos 12 continuavam em terapia insulínica, enquanto todo o grupo controle ainda necessitava de insulina. O grupo controle apresentou melhora devido à otimização da terapia médica.11
Ramos et al. utilizaram o mecanismo da derivação duodenojejunal em diabéticos com IMC<30 kg/m2 e demonstraram resolução do DM2 em 90%. No período pré-operatório a glicemia de jejum e hemoglobina glicada eram de 171 mg/dl e 8,8% respectivamente, e diminuíram para 96,3 mg/dl e 6,8% seis meses após a operação. Houve aumento de 25% no peptídeo-C após esse procedimento.16
Um grupo de 69 diabéticos não obesos foi submetido à interposição ileal laparoscópica associada à gastrectomia vertical e seguidos por De Paula et al. Cinco (7,3%) tiveram complicações precoces graves, e não houve mortalidade. O seguimento médio foi de 21,7 meses após o qual 95,7% dos pacientes alcançaram controle glicêmico adequado sem medicações hipoglicemiantes, e a hemoglobina glicada média diminuiu de 8,7±2,1% para 5,9±0,9%. A remissão foi mais frequente naqueles com menos de cinco anos de história de DM2, e para aqueles em uso pré-operatório de agentes orais. É importante perceber que o controle glicêmico não foi relacionado à quantidade de peso perdido. O IMC pós-operatório médio foi de 21,8±4,1 kg/m2, 12 pacientes (17,4%) chegaram ao baixo peso, e a albumina sérica era normal em todos, sem desnutrição detectada (Tabela 1).6
Revisão sistemática
Seguimento em longo prazo, reganho de peso e recidiva do diabete
Há quantidade razoável de publicações sobre cirurgia bariátrica e seus efeitos sobre o diabete, mas os dados de seguimento em longo prazo ainda são muito limitados, deixando não respondidas questões sobre se a operação realmente leva à remissão do diabete ou se a doença poderá re-emergir após certo período de tempo.
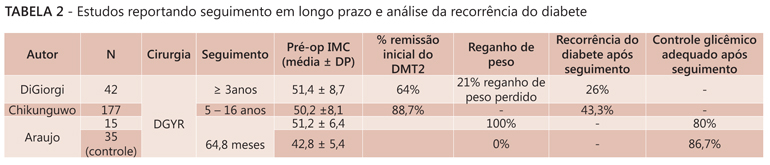
Di Giorgi et al. realizaram um estudo retrospectivo de 42 pacientes pós DGYR com seguimento de pelo menos três anos, analisando perda de peso e status do DM2. O IMC médio pré-operatório era de 51,4 kg/m2, 54% utilizavam medicações orais e 35% insulina. Dentro dos primeiros seis meses da operação, todos tiveram melhora do DM2, com 64% atingindo resolução completa. No entanto, 22% falharam em atingir perda de peso adequada e o grupo inteirou reganhou uma média de 21% do peso que havia perdido. Do grupo com resolução inicial do DM2 após a operação, ocorreu recidiva em 26%. Daqueles que apresentaram apenas melhora inicial do DM2 após o DGYR, 20% pioraram com o passar do tempo. Aqueles com recidiva ou piora do diabetes tinham IMC pré-operatório menor quando comparados com aqueles nos quais o diabete permaneceu em remissão ou com alguma melhora (47,9 versus 52,5 kg/m2). A perda de excesso de peso foi menor e a taxa de falha e porcentagem de reganho de peso perdido foram maiores para aqueles em que ocorreu recorrência ou piora do DM2 apesar do IMC inicial menor.8
Chikunguwo et al. estudaram retrospectivamente 177 pacientes com DM2 que haviam sido submetidos à DGYR de 1993 a 2003. Destes, 30 eram homens (17%) e 147 mulheres (83%). O seguimento variou de 516 anos, com média de 8,6 anos. Dos 177 indivíduos, 157 (88,7%) alcançaram remissão completa do DM2 em algum ponto no curso pós-operatório. A diferença no percentual de perda de excesso de peso entre aqueles que atingiram remissão e aqueles que não atingiram foi significante. Dos 157 pacientes com remissão inicial do DM2, 68 (43,4%) subsequentemente desenvolveram recorrência da doença, o que foi correlacionado com reganho do peso perdido. A remissão duradoura foi bem correlacionada com o tipo de tratamento do DM2 utilizado no período pré-operatório. Dos 76 que tomavam hipoglicemiantes orais e chegaram à remissão, apenas 26 (34,3%) apresentaram recidiva, e dos 47 que utilizavam insulina e alcançaram remissão, houve recidiva em 34 (72%). A remissão do DM2 foi mais duradoura em homens (80%) do que em mulheres (52,3%), e pacientes mais idosos apresentaram remissão menos duradoura. A análise mostrou que o percentual de perda de peso, gênero, idade e severidade do diabete foram fatores preditores independentes da recorrência da doença. Os preditores mais fortes foram estágio da doença (controle com medicações orais versus controle com insulina) e gênero feminino (Tabela 2)1.
No primeiro estudo descrito, por Di Giorgi et al., IMC mais baixo foi considerado como um preditor de recidiva do diabete. Isto reforça o fato que pessoas que desenvolvem diabete em um IMC mais baixo têm forma mais complicada da doença, sendo então mais susceptíveis à recidiva. Se essa hipótese é verdadeira, o tratamento cirúrgico do diabete em pacientes com IMC mais baixo pode ser menos bem sucedido do que para aqueles que desenvolveram diabete com maior IMC.8
Ambos os estudos concluíram que reganho de peso foi fator que afetou negativamente a remissão sustentável do diabete. Todavia, não é claro se a recidiva do diabete ocorre por causa do reganho de peso em si ou pela ingestão calórica aumentada, que geralmente está associada. No estudo de Chikunguwo et al. houve exceções; alguns pacientes não alcançaram remissão apesar de um grande percentual de perda de excesso de peso. Seus resultados sugerem que talvez a remissão precoce do DM2, que é independente da perda de peso, é mediada através de mecanismo diferente do que aquele que atua na remissão em longo prazo1,8.
Também relatado em ambos os estudos foi o fato de que o grupo que utilizava apenas medicações orais no período pré-operatório apresentou melhor taxa e duração da remissão do que o grupo com insulina. Tal fato indica que a intervenção na doença diabética precoce seria mais benéfica, e a necessidade de terapia insulínica poderia identificar aqueles pacientes nos quais a perda de peso seria insuficiente para compensar a capacidade secretória de insulina diminuída1,8.
Um grupo de 45 indivíduos do ambulatório de Cirurgia Geral da UFPE, todos diabéticos e obesos (obesidade grau II ou III), foram submetidos à DGYR. O grupo foi analisado retrospectivamente e prospectivamente. Todos perderam peso e alcançaram IMC menor que 35, mas em algum ponto do tempo de seguimento, houve reganho de peso em uma parte da amostra. O grupo foi então dividido em um grupo controle que incluiu pacientes que mantiveram perda de peso (n=30) e um grupo com aqueles que reganharam peso (n=15). O controle glicêmico foi analisado em ambos os grupos e não houve diferença significativa na glicemia de jejum, teste de tolerância oral a glicose, hemoglobina glicada e resolução do diabete. A remissão completa do diabete foi alcançada em 73,3% no grupo do reganho de peso e em 80% no controle (p>0,05). O estudo concluiu que reganho de peso não influencia significativamente a resolução do DM2 após a DGYR em seguimento médio de 64,8 meses, pacientes com ou sem reganho de peso tiveram taxa de recorrência do diabete similar. No entanto, para que este estudo possa ser generalizável, o número de indivíduos envolvidos deveria ser aumentado e o período de seguimento maior (Tabela 3).
Uma limitação dos artigos é que há falha em relatar se todos os pacientes foram corretamente diagnosticados com DM2. Há chance de que alguns deles, especialmente os com IMC mais baixo, foram erroneamente diagnosticados com DM2, quando na verdade eram portadores de diabete tipo 1. Tais pacientes teriam pior resposta à cirurgia metabólica, gerando um viés. Também, não é certo se os grupos envolvidos nas diferentes pesquisas estão em estágio similar da doença, e a falta de homogeneidade nos estudos e entre os estudos gera dificuldade na análise e na comparação dos resultados.
CONCLUSÕES
IMC apenas não é um bom parâmetro para definir a indicação operatória em diabéticos mal controlados. Ainda não há evidência científica de um ponto de corte no IMC para selecionar o grupo que se beneficiará do procedimento cirúrgico. Estudos futuros comparando cirurgia com tratamento clínico são necessários para realmente demonstrar a redução na mortalidade cardiovascular com tais procedimentos. Cirurigia metabólica realizada em pacientes com IMC<30kg/m2, visando o tratamento do diabete, tem-se mostrado método seguro e eficaz na análise em curto prazo. Como mostrado nesta revisão, não há dados publicados suficientes no seguimento em longo prazo, mesmo em obesos, e ainda há controvérsia nos fatores que poderiam estar associados à remissão durável da doença. Devido à esta falta de informação, futuros estudos e discussão do assunto são necessárias para se determinar a verdadeira posição deste procedimento como forma de tratamento para diabéticos não obesos.
Fonte de financiamento: não há
Conflito de interesses: não há
Recebido para publicação: 13/11/2012
Aceito para publicação: 22/01/2013
- 1.Chikunguwo S M, Wolfe L G, Dodson P, et al. Analysis of factors associated with durable remission of diabetes after Roux-en-Y gastric bypass. Surg Obes Relat Dis. 2010 May-Jun;6(3):254-9.
- 2.Choi J, Digiorgi M, Milone L, et al. Outcomes of laparoscopic adjustable gastric banding in patients with low body mass index. Surg Obes Relat Dis. 2010 Jul-Aug;6(4):367-71.
- 3.Cohen R V, Schiavon C A, Pinheiro J S, et al. Duodenal-jejunal bypass for the treatment of type 2 diabetes in patients with body mass index of 22-34 kg/m2: a report of 2 cases. Surg Obes Relat Dis. 2007 Mar-Apr;3(2):195-7.
- 4.Cummings D E, Overduin J, Foster-Schubert K E, et al. Role of the bypassed proximal intestine in the anti-diabetic effects of bariatric surgery. Surg Obes Relat Dis. 2007 Mar-Apr;3(2):109-15.
- 5.de Sa V C, Ferraz A A, Campos J M, et al. Gastric bypass in the treatment of type 2 diabetes in patients with a BMI of 30 to 35 kg/m2. Obes Surg. 2011 Mar;21(3):283-7.
- 6.DePaula A L, Macedo A L, Mota B R, et al. Laparoscopic ileal interposition associated to a diverted sleeve gastrectomy is an effective operation for the treatment of type 2 diabetes mellitus patients with BMI 21-29. Surg Endosc. 2009 Jun;23(6):1313-20.
- 7.DePaula A L, Macedo A L, Rassi N, et al. Laparoscopic treatment of type 2 diabetes mellitus for patients with a body mass index less than 35. Surg Endosc. 2008 Mar;22(3):706-16.
- 8.DiGiorgi M, Rosen D J, Choi J J, et al. Re-emergence of diabetes after gastric bypass in patients with mid- to long-term follow-up. Surg Obes Relat Dis. 2010 May-Jun;6(3):249-53.
- 9.Dixon J B, O'Brien P E, Playfair J, et al. Adjustable gastric banding and conventional therapy for type 2 diabetes: a randomized controlled trial. JAMA. 2008 Jan 23;299(3):316-23.
- 10.Fried M, Ribaric G, Buchwald J N, et al. Metabolic surgery for the treatment of type 2 diabetes in patients with BMI <35 kg/m2: an integrative review of early studies. Obes Surg. 2010 Jun;20(6):776-90.
- 11.Geloneze B, Geloneze S R, Fiori C, et al. Surgery for nonobese type 2 diabetic patients: an interventional study with duodenal-jejunal exclusion. Obes Surg. 2009 Aug;19(8):1077-83.
- 12.Gokcel A, Karakose H, Ertorer E M, et al. Effects of sibutramine in obese female subjects with type 2 diabetes and poor blood glucose control. Diabetes Care. 2001 Nov;24(11):1957-60.
- 13.Gumbs A A, Modlin I M and Ballantyne G H. Changes in insulin resistance following bariatric surgery: role of caloric restriction and weight loss. Obes Surg. 2005 Apr;15(4):462-73.
- 14.Narayan K M, Boyle J P, Geiss L S, et al. Impact of recent increase in incidence on future diabetes burden: U.S., 2005-2050. Diabetes Care. 2006 Sep;29(9):2114-6.
- 15.Norris S L, Zhang X, Avenell A, et al. Efficacy of pharmacotherapy for weight loss in adults with type 2 diabetes mellitus: a meta-analysis. Arch Intern Med. 2004 Jul 12;164(13):1395-404.
- 16.Ramos A C, Galvao Neto M P, de Souza Y M, et al. Laparoscopic duodenal-jejunal exclusion in the treatment of type 2 diabetes mellitus in patients with BMI<30 kg/m2 (LBMI). Obes Surg. 2009 Mar;19(3):307-12.
- 17.Redmon J B, Reck K P, Raatz S K, et al. Two-year outcome of a combination of weight loss therapies for type 2 diabetes. Diabetes Care. 2005 Jun;28(6):1311-5.
- 18.Rubino F. Is type 2 diabetes an operable intestinal disease? A provocative yet reasonable hypothesis. Diabetes Care. 2008 Feb;31 Suppl 2:S290-6.
- 19.Rubino F, Forgione A, Cummings D E, et al. The mechanism of diabetes control after gastrointestinal bypass surgery reveals a role of the proximal small intestine in the pathophysiology of type 2 diabetes. Ann Surg. 2006 Nov;244(5):741-9.
- 20.Rubino F and Marescaux J. Effect of duodenal-jejunal exclusion in a non-obese animal model of type 2 diabetes: a new perspective for an old disease. Ann Surg. 2004 Jan;239(1):1-11.
- 21.Thaler J P and Cummings D E. Minireview: Hormonal and metabolic mechanisms of diabetes remission after gastrointestinal surgery. Endocrinology. 2009 Jun;150(6):2518-25.
Datas de Publicação
-
Publicação nesta coleção
24 Jan 2014 -
Data do Fascículo
2013
Histórico
-
Recebido
13 Nov 2012 -
Aceito
22 Jan 2013