Resumos
Os dispositivos biorreabsorvíveis são alternativas para fixação interna das fraturas. Durante o tratamento estes dispositivos mantêm a fixação e degradam-se gradualmente não necessitando de uma cirurgia de remoção, reduzindo o custo de tratamento quando comparadas aos dispositivos metálicos. O objetivo desse trabalho foi estudar a interação polímero/tecido utilizando pinos de PLGA e PDS após implantes em coelhos Nova Zelândia. Separou-se os animais em 3 grupos os quais foram sacrificados após 3, 6 e 12 semanas de implantação e o material obtido foi submetido à análise histológica. As análises histológicas com implantes de PLGA mostraram após 3 semanas a formação de um tecido com características mesenquimatosas e com 12 semanas a formação de uma estrutura óssea madura. Já nos implantes de PDS de 3 semanas houve uma maior invasão de tecido mesenquimal comparado ao PLGA e após 12 semanas, ocorreu uma degradação avançada, com tecido proliferativo mesenquimal e ósseo. Assim, concluiu-se que ocorreram resultados positivos à resposta tecidual/implante e foi relevante a observação da ausência de células responsáveis pela resposta inflamatória. As análises demonstraram que o copolímero de PLGA apresentou propriedades osteoindutivas mais adequadas que os de PDS, apresentando biocompatibilidade aceitável para aplicação ortopédica.
Poli (ácido lático-co-ácido glicólico); poli(p-dioxanona); osteoindução
Bioresorbable devices are alternatives for internal fixation. During the treatment, those devices maintain the fixation, degrade gradually and eliminate the need for a remove surgery, decreasing the treatment cost when compared with metallic devices. The aim of this work was to study the interaction polymer/tissue interaction using pins of PLGA and PDS implanted in New Zealand rabbits. The animals were separated in 3 groups which were sacrificed after 3, 6 and 12 weeks after implantation, and the obtained material was submitted to histological analysis. Histological analysis with PLGA implants showed after 3 weeks, the growth of a tissue with mesenchimal characteristics, after 3 weeks, with formation of mature bone aready after 12 weeks. PDS implants after 3 weeks showed a bigger invasion of mesenchimal tissue compared to PLGA and after 12 weeks an advanced degradation occurred, with proliferation of mesenchimal and bone tissue formation. It is concluded that the results are highly positive, with the relevant absence of cells responsible for inflammatory response. Analysis showed that the copolymer PLGA has better ostoinductive properties than PDS, showing biocompatibility acceptable for orthopedics application.
Poly(lactic-co-glycolic acid); poly(p-dioxanone); osteoinduction
ARTIGO TÉCNICO CIENTÍFICO
Estudo da interação polímero/cartilagem/osso utilizando poli (ácido lático-co-ácido glicólico) e poli (p-dioxanona) em condilo femural de coelhos
Study of polymer/cartilage/bone interaction using poly(lactic acid-co-glycolic acid) and poly (p-dioxanona) in femoral condyle of rabbits
Maisa M. Sakata; Maria do Carmo Alberto-Rincon; Eliana A. R. Duek
Laboratório de Biomateriais, CCMB, PUC, SP
Endereço para correspondência Endereço para correspondência Eliana A. R. Duek Laboratório de Biomateriais, CCMB, PUC Praça Dr. José Ermírio de Moraes 290 CEP: 18030-230, Sorocaba, SP E-mail: eliduek@fem.unicamp.br
RESUMO
Os dispositivos biorreabsorvíveis são alternativas para fixação interna das fraturas. Durante o tratamento estes dispositivos mantêm a fixação e degradam-se gradualmente não necessitando de uma cirurgia de remoção, reduzindo o custo de tratamento quando comparadas aos dispositivos metálicos. O objetivo desse trabalho foi estudar a interação polímero/tecido utilizando pinos de PLGA e PDS após implantes em coelhos Nova Zelândia. Separou-se os animais em 3 grupos os quais foram sacrificados após 3, 6 e 12 semanas de implantação e o material obtido foi submetido à análise histológica. As análises histológicas com implantes de PLGA mostraram após 3 semanas a formação de um tecido com características mesenquimatosas e com 12 semanas a formação de uma estrutura óssea madura. Já nos implantes de PDS de 3 semanas houve uma maior invasão de tecido mesenquimal comparado ao PLGA e após 12 semanas, ocorreu uma degradação avançada, com tecido proliferativo mesenquimal e ósseo. Assim, concluiu-se que ocorreram resultados positivos à resposta tecidual/implante e foi relevante a observação da ausência de células responsáveis pela resposta inflamatória. As análises demonstraram que o copolímero de PLGA apresentou propriedades osteoindutivas mais adequadas que os de PDS, apresentando biocompatibilidade aceitável para aplicação ortopédica.
Palavras-chave: Poli (ácido lático-co-ácido glicólico), poli(p-dioxanona), osteoindução.
ABSTRACT
Bioresorbable devices are alternatives for internal fixation. During the treatment, those devices maintain the fixation, degrade gradually and eliminate the need for a remove surgery, decreasing the treatment cost when compared with metallic devices. The aim of this work was to study the interaction polymer/tissue interaction using pins of PLGA and PDS implanted in New Zealand rabbits. The animals were separated in 3 groups which were sacrificed after 3, 6 and 12 weeks after implantation, and the obtained material was submitted to histological analysis. Histological analysis with PLGA implants showed after 3 weeks, the growth of a tissue with mesenchimal characteristics, after 3 weeks, with formation of mature bone aready after 12 weeks. PDS implants after 3 weeks showed a bigger invasion of mesenchimal tissue compared to PLGA and after 12 weeks an advanced degradation occurred, with proliferation of mesenchimal and bone tissue formation. It is concluded that the results are highly positive, with the relevant absence of cells responsible for inflammatory response. Analysis showed that the copolymer PLGA has better ostoinductive properties than PDS, showing biocompatibility acceptable for orthopedics application.
Keywords: Poly(lactic-co-glycolic acid)), poly(p-dioxanone), osteoinduction.
Introdução
Os defeitos ósseos podem ocorrer do resultado de uma anormalidade congênita, trauma ou doença[1]. O tecido ósseo é continuamente reposto e remodelado de acordo com a tensão aplicada pelos osteoblastos e osteoclastos, sendo capaz de se auto-reparar após ferimentos. Porém, quando esses ferimentos causam grandes defeitos, o osso é incapaz de repará-los, formando um tecido fibroso, perdendo a sua função mecânica[1-3].
É um fenômeno bem conhecido que, se essas lesões são limitadas na substância do próprio tecido da cartilagem articular (espessura parcial ou defeitos superficiais) elas não cicatrizam espontaneamente. Se, porém, elas penetrarem na camada subjacente do osso subcondral (defeitos em toda a espessura), ocorre então, como resultado, uma reação espontânea de reparo limitada, com células dessa resposta originadas da medula óssea e espaços vasculares[4].
A regeneração óssea requer 4 componentes: um sinal morfogenético, células hospedeiras que respondem ao sinal, um carreador apropriado deste sinal que o possa entregar aos locais específicos e sirva assim como um suporte para o crescimento das células responsivas do hospedeiro e um leito viável e bem vascularizado [5].
O processo de regeneração óssea envolve o crescimento de células tipo cartilaginosas, que são formadas na superfície externa do ferimento, geralmente durante os primeiros dias após o ferimento ter ocorrido. Entre a terceira e quarta semana, a lacuna entre as células tipo cartilaginosas do novo osso é invadida por tecido embrionário, o qual forma uma ponte de tecido conjuntivo. Entre a sexta e oitava semana, ocorre a calcificação, onde o sistema vascular penetra na fibrocartilagem, absorvendo-a, enquanto a área é reposta por fibras ósseas. Finalmente, entre dois meses a dois anos, a nova fibra óssea formada é gradualmente trocada por osso rígido e, eventualmente, osso normal[3].
Apesar das fixações metálicas utilizadas nos tratamentos de fraturas ósseas serem um procedimento bem sucedido, o osso cortical e o metal possuem propriedades mecânicas bem diferentes. A elasticidade constante do osso é apenas 1/10 daquela do implante metálico, enquanto a força de tensão é dez vezes menor, levando a uma relativa osteoporose causada pela ausência funcional normal. Ocorrem também reações alérgicas contra os diferentes componentes metálicos ou o desenvolvimento de malignomas no local do implante[6-8]. Além disso, a remoção de implantes metálicos pode resultar num enfraquecimento do osso com perigo de fratura[6].
Por isso, nas duas últimas décadas, dispositivos biorreabsorvíveis têm sido utilizados e experimentados em vários aspectos das cirurgias ortopédicas, incluindo fixações de fraturas, reposição óssea, reparo da cartilagem, reparo do menisco e fixação de ligamentos[9]. Esses materiais biorreabsorvíveis têm sido utilizados na forma de parafusos, pinos e placas nas aplicações ortopédicas e cirurgias orais em humanos e animais[10]. Suas propriedades mecânicas podem ser alteradas para prover rigidez suficiente para a cura do osso, degradando numa certa velocidade que permita uma transferência gradual da tensão do implante do osso que está sendo regenerado, prevenindo assim o acúmulo de tensão no tecido[10,2,11].
Kulkarni foi o primeiro a descrever implantes de fraturas feitos de polímeros biorreabsorvíveis[12]. Desde então, foi testada uma grande variedade de materiais biorreabsorvíveis in vitro e in vivo. Inicialmente os implantes foram preparados moldando-se os polímeros em folhas ou películas, que permitiram investigações básicas no comportamento biológico das composições no tecido ósseo, mas os dispositivos não eram apropriados para fixação de fraturas, mostrando que as propriedades mecânicas dos polímeros sofrem uma variação considerável. A cristalinidade, a quantidade de monômeros livres e a taticidade são outros fatores que influenciam as propriedades mecânicas do material biodegradável. Apesar de muitos compostos macromoleculares serem biorreabsorvíveis, apenas alguns possuem as propriedades adequadas para serem dispositivos de fixação interna óssea[13]. Os mais freqüentes e investigados poli (a-hidroxi esters) têm sido poli (L-ácido lático) (PLLA), poli (ácido glicólico) (PGA) e poli (ácido lático-co-ácido glicólico) (PLGA). Esses três materiais, juntamente com o poli (pdioxanona), (PDS), têm uma longa história no uso de suturas cirúrgicas degradáveis e são aprovados para uso em humanos pela Food and Drug Administration[14,15].
A velocidade de degradação e o grau de reação de corpo estranho são determinados pela massa molar inicial e pela composição química do material. Clinicamente, a absorção dos polímeros PGA e PLA e seus copolímeros são freqüentemente acompanhados pela reação local de corpo estranho, especialmente se a velocidade de degradação é alta ou se os polímeros não são absorvidos completamente[10].
A degradação do polímero determina o tipo e a intensidade da resposta inflamatória. O surgimento de partículas monoméricas e poliméricas liberadas durante a degradação do polímero in vivo está diretamente relacionada ao tipo da resposta inflamatória. Este processo pode ser oriundo de produtos tóxicos provenientes da degradação ou pela mudança de rugosidade superficial e forma de implante durante a liberação de fragmentos. Além disso, a própria fagocitose destes atua como fator importante na modulação da resposta inflamatória. Ela modifica o processo funcional do macrófago, que é o pivô na resposta inflamatória tecidual e na ação de corpo estranho. Além disso, os fragmentos fagocitados podem acarretar morte celular e a liberação do conteúdo destas células mortas podem levar a uma resposta inflamatória aguda[ 16 ].
Os dispositivos de fixação biorreabsorvíveis têm sido utilizados clinicamente apenas por 18 anos. O número cumulativo de cirurgias com implantes biorreabsorvíveis em ortopedia têm excedido 300.000. O número de aplicações cirúrgicas continuará a crescer em ortopedia e também em outras especialidades cirúrgicas e, por essa razão, no futuro, terão um significado maior nas técnicas cirúrgicas modernas[13].
O objetivo desse trabalho foi estudar a interação polímero/cartilagem/osso, utilizando pinos de poli (ácido lático-co-ácido glicólico), PLGA, e poli (p-dioxanona), PDS, implantados em côndilo femural de coelhos Nova Zelândia.
Experimental
Preparação dos Pinos
Foram preparados por fusão, pinos de PLGA (PURAC, Groningen, The Netherlands) e PDS (Johnson & Johnson Orthopedics ), em uma mini injetora Mini Max Molder modelo LMM - 2017, utilizando um molde com dimensões internas de 2,0 mm de diâmetro e 70 mm de comprimento. Quantidades estabelecidas dos materiais foram colocadas dentro da panelinha da mini injetora, e aquecidas a 200 °C por 50 s sem cisalhamento, seguido de 1min com cisalhamento (velocidade de cisalhamento constante, de 5 rpm). O molde foi envolto por uma camisa para mantê-lo aquecido a 120 °C. Após esse procedimento a mistura foi injetada no molde, deixado esfriar a temperatura ambiente. Depois de retirado do molde, os pinos foram armazenados no dessecador, sob vácuo.
Implante do material
Neste trabalho foram utilizados coelhos Nova Zelândia, brancos, de ambos os sexos, adultos jovens, com idade aproximada de três meses, pesando 2-3,5 Kg, provenientes do Biotério do CCMB/PUC/SP. Esses animais permaneceram em gaiolas de arame no Biotério recebendo ração comercial e água "ad libitum", durante todo o período de implante .
O procedimento cirúrgico consistiu na artrotomia de ambos os joelhos, osteotomia dos côndilos femurais mediais, direito e esquerdo, nos planos axiais e fixações dos segmentos osteocondrais resultantes com pino de PDS, em joelho direito, e de PLGA, em joelho esquerdo .
Após o implante do material os animais receberam uma dose de antibiótico e permaneceram em gaiolas individuais, sem imobilização. Os animais, seis coelhos por grupo, foram sacrificados após 3, 6, 12 semanas de implantação e o material foi submetido à análise histológica.
Processamento do material
As amostras foram preparadas para análise histológica de acordo com as técnicas utilizadas para Microscopia de Luz, utilizando-se parafina como meio de inclusão.
O processamento consistiu inicialmente na retirada cirúrgica do material em data pré-determinada e fixação imediata em líquido Bouin, contendo ácido pícrico, formol e ácido acético, por um período de 24 horas à temperatura ambiente. Após a fixação, iniciou-se o processo de descalcificação em ácido fórmico (15%) e formol (5%). Após a descalcificação, iniciou-se o processo de inclusão para a preparação dos cortes histológicos onde utilizou-se como corantes a hematoxilina-eosina e o picrossírius.
Resultados e Discussão
Aspectos clínico e radiológico
Todos os animais sobreviveram até a data prevista do sacrifício. Eles mantiveram suas funções e atividades normais permanecendo em gaiolas individuais, sem imobilização. Não houve infecções pós-operatórias e nem evidências de reação de corpo estranho. Durante o pós-operatório foi observada clinicamente uma excelente recuperação dos coelhos, com deambulação precoce, limitada pela marcha antálgica em média por três dias, sendo normal após este período.
Os exames radiológicos com incidências antero-posterior e lateral dos côndilos femorais revelaram progressiva degradação dos polímeros, acompanhada de consolidação na área de osteotomia, sem diferença visual importante tanto nos casos com implantes de PDS como nos de PLGA .
Aspecto Histológico
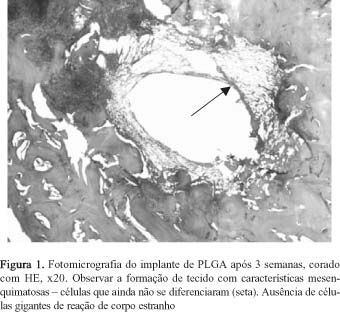
A análise histológica dos implantes de PLGA após 3 semanas demonstrou a formação de um tecido com características mesenquimatosas. Esse tipo de tecido é composto por células com longos prolongamentos, células blásticas, poucas fibras colágenas e abundante substância fundamental amorfa (Figura 1). Não foram evidenciadas células gigantes de reação a corpo estranho, mostrando assim uma ótima biocompatibilidade do polímero já que a biocompatibilidade dos dispositivos é fortemente influenciada pelo comportamento da degradação do material utilizado e é essa degradação que determina o tipo e a intensidade da resposta inflamatória[16].
Na interface osso/tecido neoformado, verifica-se a presença de vasos sanguíneos de pequeno calibre que emitem capilares em direção ao tecido em formação, os quais são necessários para nutrir o novo tecido caracterizando resposta adequada da regeneração tecidual.
Conforme Burg[5] a proliferação osteoblástica é sensível à superfície topográfica e à estímulos mecânicos. O tamanho da partícula, formato e relevo de superfície afetam a adesão celular, proliferação e fenótipo. Essas características da superfície são particularmente interessantes quando se considera o material biorreabsorvível dinâmico, o qual sempre apresentará uma nova superfície de contato. Todos os animais apresentaram uma regeneração espontânea da cartilagem limitada, com células dessa resposta originadas da medula óssea e espaços vasculares[4].
Na análise histológica dos implantes de PDS após 3 semanas, observou-se a formação de tecido com características mesenquimatosas como nos implantes de PLGA, porém, houve uma degradação acelerada do material, que foi caracterizada por uma camada bem maior de tecido mesenquimal em relação ao outro polímero (Figura 2). O polidioxanona demonstrou ausência de efeitos tóxicos quando implantados, assim como foi descrito por Grimaldi[ 17].
Nos implantes realizados, os polímeros biorreabsorvíveis conseguiram satisfazer vários requisitos biológicos e técnicas para serem aceitos. Assim como as definições feitas por Gogolewski[18], os polímeros não induziram reação inflamatória de corpo estranho, não foram carcinogênicos, mutagênicos ou teratogênicos, não causaram alergias, hipersensibilidade ou toxicidade, nem ativaram o sistema de complemento, tendo uma importância clínica relevante.
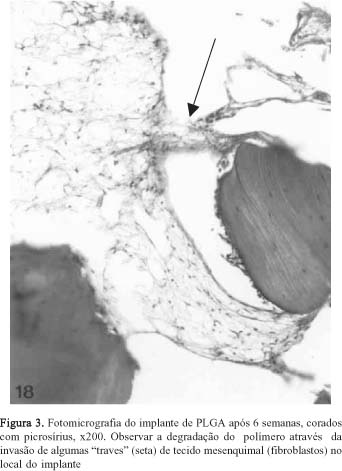
Após 6 semanas, foi possível verificar a degradação do implante de PLGA através da invasão de algumas "traves" de tecido mesenquimal no local de degradação do implante. (Figura 3). Observou-se também uma maior quantidade de tecido conjuntivo frouxo ao redor do polímero, com delicadas fibras colágenas, substância fundamental amorfa e a presença de fibroblastos (principais células responsáveis pela formação da matriz óssea).
Já nos implantes de PDS após 6 semanas, a análise histológica revelou uma maior invasão de tecido conjuntivo frouxo, ocupando uma posição mais periférica e no centro apresenta-se mais denso, com a presença de vasos sanguíneos, mostrando a boa propriedade osteocondutiva do PDS (Figura 4). De acordo com Burg[5], a osteocondução auxilia o crescimento dos capilares e das células do hospedeiro em uma estrutura tridimensional para dar forma ao osso.
Nos resultados obtidos dos implantes de PLGA de 12 semanas é possível afirmar que o local onde estava o polímero foi substituído por tecido mesenquimal proliferativo, que se tornou tecido ósseo primário e agora, apresenta-se como estrutura óssea madura com Sistema de Havers formado (Figura 5).
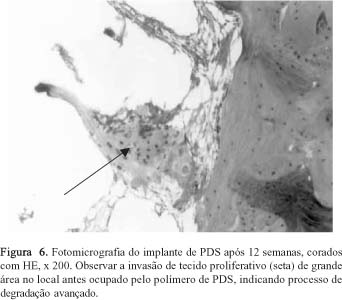
No implante com PDS de 12 semanas, verifica-se uma invasão de tecido proliferativo mesenquimal e ósseo na grande área no local antes ocupado pelo polímero, indicando processo de degradação avançado, sem indícios de células de resposta inflamatória, porém não apresentou ainda a formação de uma estrutura óssea madura como nos implantes de PLGA (Figura 6).
Conforme observado por Rokkanen[13], o grau de restauração final da arquitetura original do tecido dentro do espaço ocupado pelo implante varia por razões ainda não inteiramente conhecidas. A degradação destes polímeros ocorre principalmente por hidrólise e, em pouca extensão, com a ação enzimática não específica. Os produtos da degradação do poli (ácido glicólico) e da polidioxanona são excretados pelos rins. Através da hidrólise as moléculas de poli (ácido lático) são degradadas, in vivo, em ácido lático e as de poli (ácido glicólico) em glicinas; estes produtos entram no ciclo do ácido tricarboxílico da respiração e são excretados na forma de água e dióxido de carbono[9].
Não foram detectadas reações inflamatórias que pudessem comprometer os implantes e suas degradações. De acordo com os resultados de Gogolewski[ 18], a reação óssea aos polilácticos é em geral boa se os implantes são devidamente confeccionados e quando a técnica cirúrgica é adequada.
Conclusões
Com os dados obtidos pôde-se concluir que ocorreram resultados positivos na interação tecido/implante tanto nos implantes de PLGA como nos de PDS. Ambos apresentaram a formação de um neotecido com características mesenquimatosas e ausência de resposta inflamatória, caracterizando a biocompatibilidade dos polímeros.
Nos implantes de pinos de PDS houve uma permeabilidade de tecido mesenquimal mais rápida que nos implantes de pinos de PLGA. Pôde ser observado nos implantes de PDS, uma rápida degradação e o crescimento de capilares sanguíneos, mostrando assim a propriedade osteocondutiva que esse polímero apresenta.
Já os implantes de PLGA demonstraram com 12 semanas uma boa propriedade osteoindutiva, uma vez que o tecido mesenquimal infiltrado no polímero degradado, diferenciou-se em osteoblastos e osteócitos, e estes foram os responsáveis, juntos com os osteoclastos, pela formação do tecido ósseo maduro ou sistema de Havers.
Apesar de ambos apresentarem propriedades osteocondutivas satisfatórias, concluímos que o copolímero PLGA estudado apresenta propriedades osteoindutivas mais adequadas, com biocompatibilidade aceitável para aplicações ortopédicas.
Enviado: 08/12/03
Reenviado: 13/04/04
Aprovado: 18/04/04
- 1. Seal, B.L.; Otero, T.C.; Panitch, A. - Materials Science and Engineering, 34, p.147-230 (2001).
- 2. Salernitano, E. & Migliaresf, C. - J. of Applied Biomat. & Biomech. , 1, p. 3-18 (2003).
- 3. Arnold, J.S. & Adam, J.A. - Mathematical and Computer Modelling, 30, p.47-60 (1999).
- 4. Huziker, E.B.- Clinical Orthopaedics and Related Research, 367, p.S135-S146 (1999)
- 5. Burg, K.J.L; Porter, S. & Kellam, J.F.- Biomaterials, 21, p.2347-2359 (2000).
- 6. Chandra, R. & Rustgi, R. - Prog. Polym. Sci., 23, p.1273-1335 (1998).
- 7. Ignatius, A.A. & Claes, L.E. - Biomaterials, 17, p.831-839 (1996).
- 8. Bos, R.R.M., Rozema, F.R., Boering, G. & Nijenhuis, A.J.- Biomaterials, 12, p.32-36 (2001).
- 9. An, Y.H.; Woolf, S.K. & Friedman, R.J. - Biomaterials, 21, p.2635-2652 (2000).
- 10. An, Y.H.; Friedman, R.J.; Power, D.L.; Draughn, R.A. & Latour, R.A.- Clin. Orthop. And Related Research, 355, p.300-311 (1998).
- 11. Bergsma, J.E.; Bruijn, W.C.; Rozema F.R.; Bos, R.R.M. & Boering, G. - Biomaterials, 16, p.25-31 (1995).
- 12. Elst, M. van der; Dijkema, A.R.A.; Klein, C.P.A.; Patka, P. & Haarman, H.J. Th.M. - Biomaterials, 16, p.103-106 (1995).
- 13. Rokkanen, P.U.; Böstman, O.; Hirvensalo, E.; Mäkelä, E.A.; Partio, E.K.; Pätiälä, H.; Vainionpää, S.; Vihtonen, K & Töimälä, P. - Biomaterials, 21,p.2607-2613 (2000).
- 14. Manninen, M.J. & Pohjonen, T. - Biomaterials, 14, p.305-312 (1993).
- 15. Yaszemski, M.J.; Payne, R.G.; Hayes, W.C.; Langer, R. & Mikos, A.G.- Biomaterials, 17, p.175-185 (1996).
- 16. .Lam, K.H et al - J. Biom. Mat. Res., 27, p.1569-1577 (1993).
- 17. Grimaldi, M. et al - J. of Mat. Sci.: Mat. In Med., 31, p.6155-6162 (1996).
- 18. Gogolewski, S. - Int. J. Care Injuried, 31, p. S-D28-32 (2000).
Datas de Publicação
-
Publicação nesta coleção
29 Set 2004 -
Data do Fascículo
Set 2004
Histórico
-
Aceito
18 Abr 2004 -
Recebido
08 Dez 2003