Resumos
A hanseníase, doença crônica, granulomatosa, infecto-contagiosa, transmitida pelo Mycobacterium leprae, ainda se mantém prevalente nos dias atuais, principalmente em países subdesenvolvidos e a sua forma paucibacilar com lesão única, vem sendo tratada através da administração de rifampicina (600mg), ofloxacina (400mg) e minociclina (100mg), em dose única (esquema ROM). Assim, o objetivo deste trabalho foi investigar a correlação dose/concentração plasmática versus alterações bioquímicas na administração da rifampicina, ofloxacina e minociclina a ratos machos Wistar, em regime de dose única em mono e politerapia. Concluímos que a rifampicina e a ofloxacina sofreram um aumento na concentração plasmática quando administrados em politerapia, enquanto que a minociclina sofreu uma redução, provavelmente por interferências na biotransformação e excreção. Constatamos através das análises bioquímicas que a rifampicina provavelmente é a responsável por alterações hepáticas e renais, e que as interações medicamentosas envolvendo o fármaco exigem estudos individualizados principalmente quando o fármaco é usado associado a ofloxacina e minociclina.
Esquema ROM; Concentração plasmática; Alterações hepáticas e renais
Leprosy, a chronic granulomatous infectocontagious disease transmitted by Mycobacterium leprae, continues to be prevalent today, especially in underdeveloped countries and its paucibacillary form with a single lesion is being treated with rifampicin (600mg), ofloxacin (400mg) and minocycline (100mg) administered as a single dose (ROM scheme). Thus, the objective of the present study was to investigate the dose/plasma concentration correlation versus biochemical changes occurring in male Wistar rats receiving a single dose of rifampicin, ofloxacin and minocycline in mono- and polytherapy. Rifampicin and ofloxacin showed an increased concentration in plasma when administered in polytherapy, whereas minocycline was reduced, probably due to interference with its biotransformation and excretion. Biochemical analyses showed that rifampicin is probably responsible for hepatic and renal changes and that the medicamentous interactions involving the drug require individualized studies, especially when the drug is associated with ofloxacin and minocycline therapy.
ROM scheme; Plasma concentration; Hepatic and renal changes
ARTIGO ARTICLE
Correlação entre dose/concentração plasmática e avaliação de alterações hepáticas e renais em ratos Wistar tratados com o esquema ROM
Correlation between dose/plasma concentration and assessment of hepatic and renal changes in Wistar rats treated with the ROM scheme
Wilson Roberto Malfará; Sérgio Akira Uyemura; Regina Helena Costa Queiroz
Departamento de Análises Clínicas, Toxicológicas e Bromatológicas da Faculdade de Ciências Farmacêuticas de Ribeirão Preto da Universidade de São Paulo, Ribeirão Preto, SP
Endereço para correspondência Endereço para correspondência Dr. Wilson Roberto Malfará Avenida do Café s/n, Monte Alegre 14040-903 Ribeirão Preto, SP Tel: 16 602-4259/4703, Fax: 16 633-1936 e-mail: wilsonmalfara@yahoo.com.br, wrfara@fcfrp.usp.br
RESUMO
A hanseníase, doença crônica, granulomatosa, infecto-contagiosa, transmitida pelo Mycobacterium leprae, ainda se mantém prevalente nos dias atuais, principalmente em países subdesenvolvidos e a sua forma paucibacilar com lesão única, vem sendo tratada através da administração de rifampicina (600mg), ofloxacina (400mg) e minociclina (100mg), em dose única (esquema ROM). Assim, o objetivo deste trabalho foi investigar a correlação dose/concentração plasmática versus alterações bioquímicas na administração da rifampicina, ofloxacina e minociclina a ratos machos Wistar, em regime de dose única em mono e politerapia. Concluímos que a rifampicina e a ofloxacina sofreram um aumento na concentração plasmática quando administrados em politerapia, enquanto que a minociclina sofreu uma redução, provavelmente por interferências na biotransformação e excreção. Constatamos através das análises bioquímicas que a rifampicina provavelmente é a responsável por alterações hepáticas e renais, e que as interações medicamentosas envolvendo o fármaco exigem estudos individualizados principalmente quando o fármaco é usado associado a ofloxacina e minociclina.
Palavras-chaves: Esquema ROM. Concentração plasmática. Alterações hepáticas e renais.
ABSTRACT
Leprosy, a chronic granulomatous infectocontagious disease transmitted by Mycobacterium leprae, continues to be prevalent today, especially in underdeveloped countries and its paucibacillary form with a single lesion is being treated with rifampicin (600mg), ofloxacin (400mg) and minocycline (100mg) administered as a single dose (ROM scheme). Thus, the objective of the present study was to investigate the dose/plasma concentration correlation versus biochemical changes occurring in male Wistar rats receiving a single dose of rifampicin, ofloxacin and minocycline in mono- and polytherapy. Rifampicin and ofloxacin showed an increased concentration in plasma when administered in polytherapy, whereas minocycline was reduced, probably due to interference with its biotransformation and excretion. Biochemical analyses showed that rifampicin is probably responsible for hepatic and renal changes and that the medicamentous interactions involving the drug require individualized studies, especially when the drug is associated with ofloxacin and minocycline therapy.
Key-words: ROM scheme. Plasma concentration. Hepatic and renal changes.
A hanseníase é uma doença infecto-contagiosa causada pelo Mycobacterium leprae, bacilo que atinge pele e nervos e causa sérias incapacidades físicas e sociais quanto mais tardio for o seu diagnóstico e tratamento. O contágio se dá através do contato entre indivíduos sadios e casos contagiantes da doença (multibacilares) sem tratamento. Estudos mostram que grande parte da população é resistente a doença, entretanto pode-se garantir que a doença encontra-se em expansão quando muitas pessoas são atingidas, em especial as crianças, e quando aparecem doentes com incapacidades físicas no momento do diagnóstico14.
O Brasil detém o segundo lugar no mundo, em número absoluto de casos (77.676 casos) e índice de detecção considerado muito alto (2,41/10.000 41.070 casos novos). Contudo, acredita-se que a eliminação possa ser alcançada até o ano de 2005, pois os estados que tem possibilidade de alcançar a meta em curto e médio prazos detectam 46% dos casos novos e concentram 80% da população brasileira14 22
Em 1999, a Área Técnica de Dermatologia Sanitária instituiu novo Comitê Assessor para a área de hanseníase, atualizando todas as normas técnicas, com indicação de novos Centros de Referência, além de instruções normativas que recomendam esquemas terapêuticos para pacientes multibacilares, que consiste em 12 doses mensais supervisionadas de rifampicina (RFP 600mg) associada a clofazimina (300mg), associado a doses diárias de dapsona (100mg) e clofazimina (50mg). Recentemente, como tratamento alternativo tem-se o esquema ROM (rifampicina+ofloxacina+minociclina), administrado em dose única a pacientes paucibacilares com lesão única, podendo ainda, ser utilizado para a doença na forma multibacilar, na impossibilidade do paciente utilizar a clofazimina7 14 15. Mesmo com a possibilidade de utilização do esquema ROM para multibacilares, no Brasil o esquema foi preconizado apenas para os casos paucibacilares com lesão única.
Mane et al12 concluíram eficácia com relação ao esquema ROM em pacientes pauci e multibacilares, evidenciada por uma diminuição significativa da atividade do M. leprae. Uma eficácia comprovada também foi observada com relação a presença de granulomas e bacilos, que foram significativamente reduzidos após a terapia4.
Apesar das constatações da efetividade do esquema ROM, não existem estudos em relação a possíveis alterações hepáticas e renais que a associação dos fármacos possa resultar, fato que pode contribuir principalmente onde a terapia é indicada como alternativa a pacientes impossibilitados de utilizar a clofazimina, sendo administrada durante 24 meses, sendo rifampicina (600mg) associada a ofloxacina (400mg) e a minociclina (100mg), em doses mensais supervisionadas15.
A rifampicina é um potente indutor do citocromo P450 hepático e intestinal e da Gly-P do sistema de transporte, o que resulta em numerosas interações medicamentosas clinicamente significativas, incluindo interações com ciclosporina, glicocorticóides, cetoconazol ou itraconazol, inibidores da protease relativos ao HIV, zidovudina, nifedipina e midazolam5.
Segundo Royer17, as fluoroquinolonas não demonstram efeitos adversos severos, estando estes, mais relacionados a reações de hiperssensibilidade, destacando-se alterações cutâneas, reações anafiláticas e falência renal.
Ruef e Blaser18 ressaltam como órgãos alvo para reações adversas a quinolonas o fígado e rins sendo porém, reações raras de observação. Aumento transitório na aspartato-aminotransferase e fosfatase alcalina podem ser observadas com todas as fluoroquinolonas, com relato de um caso de insuficiência renal aguda relacionada a ofloxacina, e aumento na creatinina e uréia em alguns pacientes. As fluoronoquinolonas são potentes inibidores de isoenzimas hepáticas do citocromo P450.
Krause9 descreve algumas reações irritativas gastrintestinais em pacientes que usam a minociclina e que as reações adversas são semelhantes às outras tetraciclinas, e faz um alerta quanto a necessidade de monitorização de enzimas hepáticas e renais. Como a minociclina é eliminada completamente pelo fígado e via biliar, o que pode acelerar a sua eliminação quando associada a agentes que induzem enzimas hepáticas.
Bocker et al1 constataram que a minociclina aumentou os níveis de aspartato amino-transferase (AST), uréia e bilirrubina em camundongos tratados com duas doses. Observaram ainda que, em animais tratados previamente com fenobarbital (indutor enzimático), os níveis dos três parâmetros foram ainda maiores.
Min et al13 relataram um caso de falência hepática aguda associada com minociclina administrada por via oral durante quatro semanas. Concluíram que a causa teve origem idiossincrática, onde se observou alterações hepáticas e prolongamento do tempo de protrombina (TP), sugerindo dano hepatocelular.
Lawrenson et al11 evidenciaram também casos de hepatotoxicidade associada ao uso de minociclina, relacionados a reações de hipersensibilidade, que ocorreram dentro de poucas semanas.
A interação entre fármacos representa um papel importante na terapia farmacológica, sejam essas interações de origens farmacodinâmicas ou farmacocinéticas, representando uma grande fonte de problemas clínicos10.
A modificação dos efeitos farmacológicos por interação entre fármacos pode ser no sentido de aumentar ou diminuir a eficácia terapêutica, da mesma maneira pode acentuar ou atenuar os efeitos indesejáveis. Podem aparecer também efeitos totalmente novos, diferentes dos observados com quaisquer dos fármacos utilizados isoladamente ou pode não ocorrer nenhuma modificação no efeito final, apesar da cinética e do metabolismo de um ou ambos terem sido alterados.
Assim, o presente trabalho objetiva investigar a correlação entre dose administrada versus concentração plasmática dos três fármacos componentes do esquema ROM, administrados a ratos machos Wistar, no esquema de dose única em monoterapia (fármacos isolados) e politerapia (fármacos associados esquema ROM), seguido de avaliação de possíveis alterações hepáticas e renais através da investigação de parâmetros bioquímicos.
MATERIAL E MÉTODOS
Animais. Foram utilizados 5 grupos (n=8) de ratos machos jovens, linhagem Wistar, que receberam intraperitonealmente os fármacos solubilizados em dimetilsulfóxido (DMSO), em regime de dose única (Grupo cont), grupo rfp100, que recebeu 500mL de rifampicina 100mg/kg em DMSO, grupo oflx80, que recebeu 200mL de ofloxacina 80mg/kg em DMSO, grupo mino20, que recebeu 200mL de minociclina 20mg/kg em DMSO e grupo rom, que recebeu 100mg/kg de rifampicina associada a 80mg/kg de ofloxacina e a 20mg/kg de minocilina em 900µL de DMSO. Duas horas após o tratamento, os animais foram anestesiados com éter etílico, e o sangue foi colhido da aorta e utilizado para determinação da concentração plasmática dos fármacos e para determinação dos parâmetros bioquímicos. Os animais foram eutanasiados logo em seguida da colheita do material.
Procedimentos analíticos.Análise da rifampicina, ofloxacina e da minociclina em plasma de ratos por cromatografia líquida de alta eficiência: os fármacos foram quantificados através de CLAE, onde desenvolveu-se e validou-se metodologias analíticas específicas aplicáveis para o estudo em questão.
Parâmetros bioquímicos. Os parâmetros bioquímicos analisados no presente trabalho foram quantificados por técnicas analíticas automatizadas utilizando o auto-analisador ABBA-VP, da marca Abbott e reagentes da marca Labtest®, sendo: bilirrubina total e direta pelo método colorimétrico, segundo Sims & Horn19, fosfatase alcalina (ALP) pelo método cinético-enzimático otimizado, aspartato-aminotransferase (AST) e alanina-aminotransferase (ALT) pelo método cinético-enzimático otimizado, gama-glutamiltransferase (GGT) pelo método cinético-enzimático, uréia pelo método cinético-enzimático, creatinina pelo método cinético-colorimétrico, proteínas totais pelo método colorimétrico do biureto6 e albumina pelo método colorimétrico do verde-bromocresol3 e amilase pelo método CNPG38.
Análise estatística. Os grupos tratados foram comparados a seus respectivos controles através de metodologia não-paramétrica para mais de duas amostras independentes (Teste de Kruskal-Wallis), e metodologia paramétrica através de comparação múltipla entre os grupos utilizando ANOVA (Tukey-Kramer). O nível de significância foi fixado em p < 0,05.
RESULTADOS
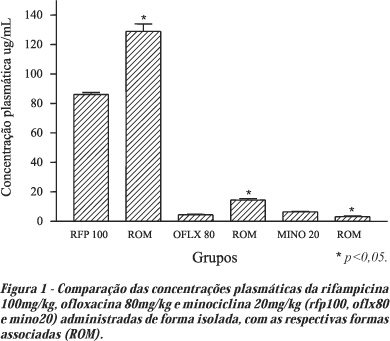
A Figura 1 ilustra a comparação da rifampicina 100mg/kg isolada (Grupo rfp100) com a mesma associada com ofloxacina e minociclina ( Grupo ROM), evidenciando um aumento significativo na concentração plasmática do fármaco no grupo ROM. O mesmo aumento foi observado com a ofloxacina 80mg/kg isolada comparada com a mesma associada a rifampicina e a minociclina. Contrariamente ao que ocorreu com a rifampicina e com a ofloxacina, observou-se com a minociclina isolada comparada com a associada com rifampicina e ofloxacina, uma redução dos níveis plasmáticos do fármaco.
A Tabela 1 representa os valores de todos os parâmetros analisados expressos como mediana, com seus respectivos valores mínimos e máximos, onde se observa diferenças estatisticamente significativas nos parâmetros representados nas Figuras 2 e 3.
A Figura 2 ilustra a comparação entre os parâmetros para avaliação de dano hepático, que ofereceram resultados estatisticamente significativos: bilirrubina direta (A), bilirrubina total (B), AST (C) e ALT (D), observando-se um aumento nos níveis séricos em todos os parâmetros quando se administrou a rifampicina e elevação de bilirrubina direta e total, no esquema associado.
A Figura 3 ilustra a comparação entre os parâmetros para avaliação de dano renal, que ofereceram resultados estatisticamente significativos: uréia (A) e creatinina (B), observando-se um aumento nos níveis séricos em ambos, quando se administrou a rifampicina.
DISCUSSÃO
A relação dose-efeito ou a relação concentração plasmática-efeito são elementos básicos na farmacologia experimental. Contudo, na farmacologia clínica a demonstração destas relações é difícil. Para alguns fármacos, a relação dose-efeito varia consideravelmente entre os pacientes e esta alta variabilidade é principalmente o resultado de uma pobre aderência do paciente ao regime de dosagem ou diferenças na farmacocinética, particularmente na absorção e eliminação. Portanto, em algumas terapias é importante ajustar a dose para se atingir o efeito terapêutico desejado sem correr o risco de toxicidade16.
No presente trabalho, tem-se especificamente o interferente variabilidade biológica inerente a qualquer ser vivo. A relação entre dose administrada e concentração plasmática, então, torna-se instrumento valioso para se eliminar interferentes que antecedem o efeito propriamente dito, ou seja, trabalha-se com a concentração efetivamente responsável pelo efeito ou alteração observados.
Para se correlacionar a dose administrada com concentração plasmática, usamos a cromatografia líquida de alta eficiência (CLAE).
Após a validação da metodologia, realizou-se a dosagem de concentração plasmática dos grupos que receberam rifampicina 100mg/Kg (rfp100), ofloxacina 80mg/kg (oflx80) e minociclina 20mg/kg (mino20) isolados, que foram comparados com os fármacos associados (ROM). Observa-se pela Figura 1 que as concentrações plasmáticas da rifampicina e da ofloxacina aumentaram e que inversamente, a concentração plasmática da minociclina diminuiu. Tal observação pode ser explicada pelas diferenças de velocidade nos processos farmacocinéticos e farmacodinâmicos ou até mesmo por uma interferência na biotransformação da mesma, ou seja, quando a rifampicina foi associada a ofloxacina e a minociclina, a sua concentração plasmática aumentou.
Diferenças interindividuais na oxidação de fármacos vêm sendo referenciadas como fonte de maior importância na variabilidade da farmacocinética de fármacos, pois esta oxidação é catalisada por enzimas do citocromo P450 (CYP450) e a atividade de metabolização de fármacos através CYP é determinada por fatores que variam de indivíduo para indivíduo, como a disposição genética, fatores ambientais e fatores constitucionais2. O envolvimento de isoformas específicas do CYP na biotransformação dos fármacos em questão, além de um provável envolvimento da glicoproteína-P (GLY-P), podem explicar os fatos observados. Logicamente estas são suposições que exigem maiores estudos para a conclusão completa da questão, mas isso também ressalta a grande importância da relação de efeito ou prováveis alterações, com a concentração plasmática e não com a dose administrada, o que facilita o entendimento de alguns processos eliminando interferências significativas.
Com relação as alterações hepáticas, observa-se um aumento nos níveis séricos de bilirrubinas direta e totais, AST e ALT nos animais que receberam a rifampicina isoladamente (rfp100), (Figura 2A, B, C e D), e aumento também nos níveis séricos de bilirrubinas direta e totais, quando administrou-se os três fármacos associados (rom), (Figura 2A e B). Acreditamos pelos resultados obtidos que a rifampicina é a provável responsável por essas alterações, como constatado por Sodhi et al20 21.
Da mesma forma, observa-se um aumento nos níveis séricos de uréia e creatinina, nos animais que receberam a rifampicina isolada (rfp100) comparando-a com o grupo controle (Figura 3A e B ).
Nos outros parâmetros avaliados (amilase, fosfatase alcalina, proteínas totais, albumina e gamaglutamil-transferase), não observamos alterações estatisticamente significativas (Tabela 1).
Assim, com tais constatações, concluímos que na administração do esquema ROM, tem-se uma elevação na concentração plasmática da rifampicina e da ofloxacina, diferindo da minociclina que sofreu uma redução dos seus níveis plasmáticos, devido provavelmente a uma interferência nos processos de biotransformação e excreção dos fármacos. Ainda, ratificando os dados da literatura20 21, concluímos que a rifampicina pode causar danos hepáticos e renais, o que na clínica pode ser de fundamental importância principalmente quando se administra o fármaco na associação com a ofloxacina e minociclina, e que as mesmas não demonstraram alterações significativas nos parâmetros hepáticos e renais avaliados, sugerindo que a probabilidade de tais fármacos induzirem alterações hepáticas e renais, pode estar relacionada a reações de hipersensibilidade, segundo Royer17 e Lawrenson et al11.
AGRADECIMENTOS
Agradecemos a Coordenação de Aperfeiçoamento de Pessoal de Nível Superior (CAPES), pelo apoio financeiro.
Recebido para publicação em 16/3/2004
Aceito em 15/12/2004
Financiamento: CAPES
- 1. Bocker HR, Peter R. Identification and determination of the two principal metabolites of minocycline in humans. Journal Chromatography Biom Applied 568:363-374, 1991.
- 2. Brosen K. Drug-metabolizing enzymes and therapeutic drug monitoring in psychiatry. Therapeutic Drug Monitoring 18: 393-396, 1996.
- 3. Doumas BT, Watson WA, Biggs HG. Albumin standart and the measurement of serum albumin with bromocresol green. Clinica Chimica Acta 31: 87-96, 1971.
- 4. Ebenezer GJ, Job CK. Histopathological activity in paucibacillary leprosy patients after ROM therapy. International Journal of Leprosy and other Mycobacterial Diseases 67: 409-413, 1999.
- 5. Finch CK, Chrisman CR, Baciewicz AM, Self TH. Rifampin and rifabutin drug interaction: an update. Archives of Internal Medicine 162: 985-992, 2002.
- 6. Gornall AG, Bardawill CJ, David MM. Determination of serum proteins by means of the biuret reaction. The Journal of biological chemistry 1977: 751-766, 1949.
- 7. Ishii N. Recent advances in the treatment of leprosy. Dermatology Online Journal l9:1-18, 2003.
- 8. Kaplan LA, Pesce AJ. Clinical chemistry: theory, analysis and correlation. 4th edition Saint Louis, 1996.
- 9. Krause M. Miscellaneous antibacterial drugs: sulfonamides and trimethoprim, tetracyclines, other antimicrobial drugs. In: Schaffner A. (ed) Meyler's Side Effects of drugs, 14th edition, Amsterdam, p. 906-911, 2000.
- 10. Kremers P. Can drug-drug interactions be predicted from in vitro studies? The Scientific World Journal 19:751-766, 2002.
- 11. Lawrenson RA, Seaman HE, Sundstrom A, Williams TJ, Farmer RD. Liver damage associated with minocycline use in acne: a systematic review of the published literature and pharmacovigilance data. Drug Saf 23:333-349, 2000.
- 12. Mane I, Cartel JL, Grosset JH. Field trial on efficacy of supervised monthly dose of 600 mg rifampicin, 400 mg ofloxacin and 100 mg minocyclin for the treatment of leprosy; first results. International Journal of Leprosy and other Mycobacterial Diseases 65:224-229, 1997.
- 13. Min DI, Burke PA, Lewis WD, Jenkins RL. Acute hepatic failure associated with oral minocycline: a case report. Pharmacotherapy 12:68-71, 1992.
-
14Ministério da Saúde. Portaria Nº 1073/GM de 26 de setembro de 2000. Publicada no Diário Oficial da União — 188-E — pg 18-Seção 1- 28 de setembro, 2000.
-
15Ministério da Saúde. Secretária de Políticas de Saúde.Departamento de Atenção Básica. Área Técnica de Dermatologia Sanitária. Normas Técnicas para Eliminação da Hanseníase no Brasil p. 1-45, 2001.
- 16. Rasmussen BB, BrÆsen K. Is Therapeutic Drug Monitoring a case for optimizing clinical outcome and avoiding interactions of selective serotonin reuptake inhibitors? Therapeutic Drug Monitoring 22:143-154, 2000.
- 17. Royer RJ. Adverse drug reactions with fluoroquinolones. Therapie 51: 414-416, 1996.
- 18. Ruef C, Blaser J. Miscellaneous antibacterial drugs: aminoglycosides, chloramphenicol and thiamphenicol, fluoroquinolones, glycopeptides. In: Schaffner A (ed) Meyler's Side Effects of drugs, 14th edition, Amsterdam, p. 852-856, 2000.
- 19. Sims FH, Horn C. Some observations on Powell's methods for the determination of serum bilirubin. American Journal of Clinical Pathology 29:412-417, 1958.
- 20. Sodhi CP, Rana S, Mehta S, Vaiphei K, Attari S, Mehta S. Study of oxidative-stress in isoniazid-rifampicin induced hepatic injury in young rats. Drug and Chemical Toxicology 20:255-269, 1997.
- 21. Sodhi CP, Rana S, Mehta S, Vaiphei K, Goel RC, Mehta SK. Study of oxidative-stress in rifampicin-induced hepatic injury in growing rats with and without protein-energy malnutrition. Human & Experimental Toxicology 17:315-321, 1997.
- 22. World Health Organization. Leprosy-Global Situation. Weekly epidemiological Record (on line), Disponível na Internet: http://www.who.int/wer 77:1-8, 2002.
Endereço para correspondência
Datas de Publicação
-
Publicação nesta coleção
30 Mar 2005 -
Data do Fascículo
Abr 2005
Histórico
-
Aceito
15 Dez 2004 -
Recebido
16 Mar 2004