Resumos
O hipotireoidismo congênito (HC) é o distúrbio endócrino congênito mais frequente, com incidência variando de 1:2.000 a 1:4.000 crianças nascidas vivas e uma das principais causas de retardo mental que pode ser prevenida. Os Programas de Triagem Neonatal para a doença permitem a identificação precoce dos afetados e seu tratamento de modo a evitar as complicações da falta do hormônio. A maioria dos casos de hipotireoidismo congênito é decorrente de disgenesias tireoidianas (85%), entre elas a ectopia, hipoplasia ou agenesia tireoidianas, e os demais resultam de defeitos de síntese hormonal. As crianças afetadas (> 95%) geralmente não apresentam sintomas sugestivos da doença ao nascimento. Os sintomas e sinais mais comuns são: icterícia neonatal prolongada, choro rouco, letargia, movimentos lentos, constipação, macroglossia, hérnia umbilical, fontanelas amplas, hipotonia e pele seca. Várias estratégias são utilizadas para a triagem do HC. No Brasil, esta é obrigatória por lei e geralmente é feita com a dosagem de TSH em sangue seco coletado do calcanhar. A idade recomendada para sua realização é após as 48 horas de vida até o quarto dia. A confirmação diagnóstica é obrigatória com as dosagens de TSH e T4 livre ou T4 total.
Hipotireoidismo congênito; triagem neonatal
Congenital hypothyroidism (CH) is the most common congenital endocrine disorder, with an incidence of 1:2,000 to 1:4,000 live births and it is a leading preventable mental retardation. Neonatal Screening Programs allow early identification of the disease and the adequate treatment of affected children can avoid the complications related to deprivation of the hormone. Most cases of primary congenital hypothyroidism (85%) are due to thyroid dysgenesis (ectopia, hypoplasia or agenesis) while the remaining result from defects in hormone synthesis. Affected children (> 95%) usually have no symptoms suggesting the disease at birth. The most frequent symptoms and signs are prolonged neonatal jaundice, hoarse cry, lethargy, slow movements, constipation, macroglossia, umbilical hernia, large fontanelle, hypotonia and dry skin. Around the world, various strategies are used for the screening of the CH. In Brazil, screening for CH is mandatory by law and usually done by serum TSH in dried blood collected from the heel. The recommended age for performing this test is after 48 hours of life until the 4th day. Diagnostic confirmation is required dosing TSH and free T4 or total T4 in serum.
Congenital hypothyroidism; neonatal screening
CONSENSO DE TIREOIDE
Hipotireoidismo congênito: recomendações do Departamento de Tireoide da Sociedade Brasileira de Endocrinologia e Metabologia
Léa Maria Zanini MacielI; Edna Teruko KimuraII; Célia Regina NogueiraIII; Glaucia M. F. S. MazetoIII; Patrícia Künzle Ribeiro MagalhãesI; Marilza Leal NascimentoIV; Suzana Nesi-FrançaV; Sandra E. VieiraVI
IDivisão de Endocrinologia e Metabologia, Faculdade de Medicina de Ribeirão Preto, Universidade de São Paulo (FMRP-USP), Ribeirão Preto, SP, Brasil
IIInstituto de Ciências Biomédicas, USP, São Paulo, SP, Brasil
IIIDivisão de Endocrinologia e Metabologia, Departamento de Clínica Médica, Faculdade de Medicina de Botucatu, Universidade Estadual de São Paulo (Unesp), Botucatu, SP, Brasil
IVUniversidade Federal de Santa Catarina (UFSC), Florianópolis, SC, Brasil
VUnidade de Endocrinologia Pediátrica, Departamento de Pediatria, Universidade Federal do Paraná (UFPR), Curitiba, PR, Brasil
VIDepartamento de Pediatria, Faculdade de Medicina da Universidade de São Paulo (FMUSP), SP, Brasil
Correspondência para Correspondência para: Léa Maria Zanini Maciel Departamento de Clínica Médica Av. Bandeirantes, 3900 14049-900 - Ribeirão Preto, SP, Brasil lmzmacie@fmrp.usp.br
RESUMO
O hipotireoidismo congênito (HC) é o distúrbio endócrino congênito mais frequente, com incidência variando de 1:2.000 a 1:4.000 crianças nascidas vivas e uma das principais causas de retardo mental que pode ser prevenida. Os Programas de Triagem Neonatal para a doença permitem a identificação precoce dos afetados e seu tratamento de modo a evitar as complicações da falta do hormônio. A maioria dos casos de hipotireoidismo congênito é decorrente de disgenesias tireoidianas (85%), entre elas a ectopia, hipoplasia ou agenesia tireoidianas, e os demais resultam de defeitos de síntese hormonal. As crianças afetadas (> 95%) geralmente não apresentam sintomas sugestivos da doença ao nascimento. Os sintomas e sinais mais comuns são: icterícia neonatal prolongada, choro rouco, letargia, movimentos lentos, constipação, macroglossia, hérnia umbilical, fontanelas amplas, hipotonia e pele seca. Várias estratégias são utilizadas para a triagem do HC. No Brasil, esta é obrigatória por lei e geralmente é feita com a dosagem de TSH em sangue seco coletado do calcanhar. A idade recomendada para sua realização é após as 48 horas de vida até o quarto dia. A confirmação diagnóstica é obrigatória com as dosagens de TSH e T4 livre ou T4 total.
Descritores: Hipotireoidismo congênito; triagem neonatal
INTRODUÇÃO
O hipotireoidismo congênito (HC) é o distúrbio endócrino congênito mais frequente e com incidência variando de 1:2.000 a 1:4.000 crianças nascidas vivas em países com suficiência iódica (1,2) (B). No Brasil, a prevalência de HC é aproximada a esses valores, variando de 1:2.595 a 1:4.795 (3,4) (D). Entretanto, estudos recentes apontam para uma maior incidência do HC nos Estados Unidos, de 1:4094 em 1987 para 1:2372 em 2002 (5) (B). As razões para isso não estão muito claras, mas é justificada por alguns pesquisadores pela maior detecção de casos subclínicos da doença devido à utilização de níveis de corte mais baixos para o teste de triagem com hormônio estimulante da tireoide (TSH) e pela inclusão de hipotireoidismos transitórios (6-9) (D).
A prevalência do HC é variável entre os grupos étnicos, sendo consideravelmente menos prevalente entre os negros americanos que entre os hispânicos (1:10.000 x 1:2.700), assim como é mais prevalente em mulheres (2:1). Crianças com síndrome de Down têm um risco 35 vezes maior para apresentar o HC que a população geral (10) (B).
Na ausência de um diagnóstico precoce e tratamento adequado, a maioria das crianças desenvolverá vários graus de deficiências neurológicas, motoras e de crescimento, incluindo o retardo mental irreversível.
MÉTODOS
Foram realizadas buscas ativas nas bases de dados primárias MedLine e SciELO, utilizando os seguintes termos descritivos (MeSH Terms): congenital hypothyroidism; neonatal screening.
Grau de recomendação e força de evidência:
A: Estudos experimentais e/ou observacionais de melhor consistência.
B: Estudos experimentais e/ou observacionais de menor consistência.
C: Relato de casos.
D: Opinião desprovida de avaliação crítica, baseada em consensos, estudos fisiológicos ou modelos animais.
1. QUAIS SÃO AS CAUSAS DO HIPOTIREOIDISMO CONGÊNITO?
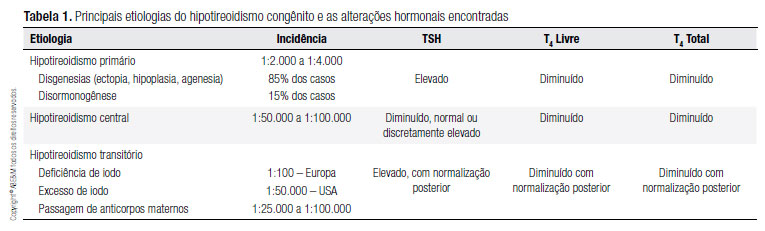
A causa mais frequente de HC permanente resulta de defeitos na formação glandular durante a embriogênese, denominados disgenesias tireoidianas, e representa 85% dos casos (Tabela 1). Esse grupo inclui a ectopia, a agenesia e a hipoplasia tireoidianas, que representam 30%-45%, 35%-45% e 5% dos casos, respectivamente (11) (D). O entendimento preciso dessas alterações permanece desconhecido, apesar de mutações em fatores transcricionais que regulam o desenvolvimento da glândula tireoide como o thyroid transcription factor 2 (TTF-2), NKX2.1 (também conhecido como TTF-1) e o PAX-8 tenham sido implicadas. Entretanto, somente 2% dos casos de disgenesias apresentam essas mutações genéticas (12) (B). Esses fatores de transcrição se manifestam em outros tecidos e estão associados com HC sindrômico. Assim, mutações no NKX2.1, gene que participa do desenvolvimento do pulmão e cérebro, leva o recém-nascido (RN) a apresentar insuficiência respiratória neonatal e coreoatetose. Pacientes com mutações no TTF-2 se apresentam com cabelo espetado, palato fendido, atresia de anus e agenesia tireoidiana (11) (D).
Outras etiologias de HC permanente são os defeitos na produção hormonal, denominados de disormonogênese, e representam cerca de 15% dos casos. São defeitos autossômicos recessivos e incluem mutações em genes que codificam o transportador de iodo-sódio (NIS) (gene SLC5A5), a tireoperoxidase (TPO), a geração de peróxido de hidrogênio [thyroid oxidase e dual oxidase maturation factors (genes DUOXA1 e DUOX2)], a tireoglobulina (Tg) e a iodotirosina deiodinase (13).
Causas incomuns de HC incluem defeitos no transporte de hormônio tireoidiano (HT), como mutações no gene MCT 8 (monocarboxylate transporter 8) (14) (C), a resistência à ação do HT (síndrome de resistência ao hormônio tireoidiano) (15) (D), a resistência ao TSH (16) (C) e o hipotireoidismo central (17,18) (B).
O hipotireoidismo central decorre da deficiência isolada de TSH ou, mais comumente, do hipopituitarismo resultando na deficiência de diversos hormônios da adeno-hipófise. Mutações de diversos genes envolvidos no desenvolvimento ou função hipofisária foram implicadas, entre eles HESX1, LHX4, PIT-1 e PROP1. A resistência ao hormônio liberador de tireotrofina (TRH) (mutação no gene do receptor do TRH) também pode causar hipotireoidismo central (18).
A síndrome de resistência ao hormônio tireoidiano é uma doença rara com espectro clínico variável decorrente de diminuição da responsividade aos HT.
A resistência ao TSH é definida quando as concentrações séricas de TSH são elevadas (hipertireotrofinemia) na ausência de bócio. Indivíduos afetados têm glândula tireoidiana normal ou hipoplásica e valores séricos de T4 e T3 normais ou baixos.
Defeitos no transporte de HT causados por mutações no gene MCT-8, localizado no cromossomo X, fazem com que o transporte de T3 fique prejudicado, levando ao retardo mental. A síndrome é caracterizada por concentrações séricas elevadas de T3, baixas de T4 e elevadas de TSH.
Recomendação 1
A causa mais frequente de hipotireoidismo congênito permanente é a disgenesia tireoidiana, que inclui agenesia, ectopia e hipoplasia de tecido tireoidiano (B). Em segundo lugar, estão as disormonogêneses (B). Causas raras de HC são: hipotireoidismo central (B), síndrome de resistência ao hormônio tireoidiano (D), síndrome de resistência ao TSH (C) e mutações no MCT-8 (C).
2. O HIPOTIREOIDISMO CONGÊNITO PODE SER TRANSITÓRIO?
O HC pode ser transitório e resultar de diversas causas:
ingestão excessiva (ou deficiente) de iodo pela mãe;
ingestão materna de drogas antitireoidianas em mães portadoras de hipertireoidismo;
passagem placentária de anticorpos maternos bloqueadores do receptor de TSH. Esse diagnóstico deve ser considerado quando houver relato de mais de um filho com hipotireoidismo transitório detectado pela triagem neonatal. Geralmente perdura 1 a 3 meses até que os anticorpos desapareçam da circulação;
mutações em heterozigose das enzimas DUOX1 (gene DUOXA1) e de DUOX2 ou THOX (gene DUOX2);
hemangiomas hepáticos de grandes dimensões (aumento da atividade da desiodase do tipo 3) (7,8) (D).
Pacientes considerados como sendo portadores de HC transitório foram acompanhados por três anos e apenas 47% evoluíram com hipotireoidismo permanente. Dessa forma, recomenda-se a reavaliação aos 3 anos para definir a permanência ou não da doença (19) (B).
Recomendação 2
O hipotireoidismo neonatal pode ser permanente ou transitório. Recomenda-se a reavaliação após os 3 anos de idade com a suspensão da levotiroxina (L-T4) nas crianças em tratamento, que não apresentem etiologia do hipotireoidismo estabelecida (B).
3. MANIFESTAÇÕES CLÍNICAS DO HIPOTIREOIDISMO CONGÊNITO
A maioria das crianças com HC (> 95%) apresenta poucas ou nenhuma manifestação clínica da doença ao nascimento (20) (B). Isso se deve ao fato de o T4 materno passar a barreira placentária (21) (B) e também em função de a maioria das crianças afetadas apresentar algum tecido tireoidiano funcionante. Como o HT tem meia-vida de seis dias, por volta de 3-4 semanas de vida do RN, o hormônio materno será metabolizado e excretado.
As crianças afetadas, tipicamente, apresentam peso e estatura dentro da faixa de normalidade. Um dos primeiros sinais observados é a icterícia neonatal prolongada (22,23) (B). À medida que o tempo passa a criança sem diagnóstico se apresentará letárgica, com movimentos lentos, choro rouco, engasgos frequentes, constipação, macroglossia, hérnia umbilical, fontanela ampla, hipotonia, pele seca, cabelos ralos e adquire a fácies típica com nariz em sela. Poucos RN com disormonogênese apresentam bócio palpável ao nascimento, porém este pode aparecer mais tarde mesmo com tratamento (23). A radiografia de epífises do joelho poderá revelar atraso de ossificação, o que reflete a gravidade do hipotireoidismo fetal. Na tabela 2, encontram-se os sintomas ou sinais apresentados em crianças afetadas recém-diagnosticadas de acordo com a gravidade da doença (24) (B). Na triagem de neonatos brasileiros, o HC associou-se a hérnia umbilical (48,9%), base nasal alargada (46,6%) e icterícia prolongada além de 7 dias (44,4%); e 20% dos casos não tinham nenhuma manifestação clínica (25) (A).
Quando o diagnóstico etiológico do HC for hipopituitarismo, a criança terá tendência à hipoglicemia pela deficiência de hormônio do crescimento e do hormônio adrenocorticotrófico (ACTH)/cortisol e, se for do sexo masculino, apresentará micropênis. Essa criança corre risco de morte se não for detectada precocemente e geralmente não será detectada pela triagem neonatal quando esta é feita com a dosagem do TSH.
Recomendação 3
Apesar da possibilidade de ausência de manifestações clínicas em recém-nascidos com hipotireoidismo congênito, os sinais e sintomas descritos na tabela 2 devem servir de alerta (B).
4. O HIPOTIREOIDISMO CONGÊNITO PODE OCORRER EM ASSOCIAÇÃO A ANORMALIDADES CONGÊNITAS?
Crianças com HC têm risco adicional de apresentar malformações (10% vs. 3% nas crianças normais), afetando principalmente o coração (4 vezes mais), mas também os rins, o trato urinário e os sistemas gastrointestinal e esquelético (26,27) (B).
Crianças com HC e palato fendido podem apresentar mutações no TTF-2 (gene FOXE-1) (28) (C) e as com sintomas neurológicos persistentes, incluindo ataxia, são suspeitas de apresentarem mutações no gene NKX2 (29) (C).
Problemas auditivos ocorrem em até 20% das crianças com HC e todas as crianças afetadas deverão ser submetidas a teste de screening auditivo (30,31) (B).
Não existe um consenso para a realização de testes de screening para anomalias congênitas, entretanto, um exame físico cuidadoso é importante e, na presença de qualquer alteração ao exame, a criança deverá ser encaminhada para avaliação.
O conhecimento precoce de outras malformações em portadores de HC pode modificar o prognóstico dos pacientes (32) (B).
Recomendação 4
É recomendado o screening auditivo e um exame físico cuidadoso para a pesquisa de outras anormalidades congênitas em crianças com hipotireoidismo congênito (B).
5. A TRIAGEM NEONATAL É EFICAZ PARA O RASTREAMENTO PRECOCE DO HIPOTIREOIDISMO CONGÊNITO?
O principal objetivo da triagem neonatal para o HC é evitar as sequelas, principalmente o retardo mental secundário ao hipotiroidismo, o que pode ser conseguido com o início da terapêutica adequada nas duas primeiras semanas de vida (33) (B).
A triagem neonatal para o HC é rotina nos Estados Unidos, no Canadá, na Europa, em Israel, no Japão, na Austrália e na Nova Zelândia e está em desenvolvimento no Leste Europeu, na América do Sul, na Ásia e na África.
A sensibilidade dos testes de triagem neonatal para HC é elevada, o que a torna eficaz para rastrear a doença. Estudos populacionais realizados na Europa e nos Estados Unidos relatam sensibilidades próximas de 97% a 100% e especificidades de 98% a 100% (34,35) (A).
Recomendação 5
A triagem neonatal é recomendada para o rastreamento do hipotireoidismo congênito (A).
6. QUANDO DEVEM SER FEITOS OS TESTES PARA TRIAGEM NEONATAL DO HIPOTIREOIDISMO CONGÊNITO?
Para o teste de triagem neonatal, o sangue do calcanhar é coletado em cartões nos quais são inseridos os dados da criança (data de nascimento, idade gestacional, sexo, peso, se houve transfusão ou não etc.) e como localizá-la. Nesse cartão de dados, é anexado o papel de filtro onde o sangue será impregnado e seco antes do envio para o laboratório de triagem. A idade do RN recomendada para essa coleta é após as 48 horas de vida até o quarto dia (36), quando já ocorreu a diminuição do pico pós-natal de elevação fisiológica do TSH. Idealmente, o teste deve ser colhido antes da alta da maternidade; no entanto, coletas em altas precoces (< 48 horas) podem resultar em resultados falso-positivos mais frequentes. Nas crianças criticamente doentes ou pré-termos, a recomendação é para a coleta ser realizada aos sete dias de vida; entretanto, é importante ter presente que as coletas obtidas após quatro dias de vida poderão ser tardias para as crianças portadoras de hiperplasia adrenal congênita ou doença metabólica (36). Devido à imaturidade do eixo hipotálamo-hipófise-adrenal dos prematuros, alguns autores recomendam a repetição do teste de triagem nesses bebês com duas a quatro semanas de vida.
Quando houver necessidade de transfusão de sangue total, o teste deve ser coletado antes que a criança seja transfundida, independentemente da sua idade (37) (D).
Recomendação 6
A idade recomendada para a coleta de sangue do RN para a triagem neonatal é após as 48 horas de vida até o quarto dia ou antes que o RN deixe o hospital nas altas precoces e sempre antes de transfusões sanguíneas (D).
7. QUAIS OS EXAMES ADOTADOS NO BRASIL PARA A TRIAGEM DO HIPOTIREOIDISMO CONGÊNITO?
Existem diversas estratégias para a triagem do HC:
1. Dosagem de TSH.
2. Dosagens de TSH e T4 simultaneamente.
3. Dosagem inicial de T4 seguida da dosagem de TSH nas amostras com T4 abaixo de determinado limite (usualmente abaixo do percentil 10).
A dosagem de TSH tem maior especificidade em relação à dosagem isolada de T4. A dosagem simultânea de TSH e T4 tem maior sensibilidade em relação a todos os protocolos, mas também leva a maior número de falsos-positivos (38) (B). No Brasil, no sistema público, adota-se a triagem com TSH (TSHneo) apenas, com valores de corte de TSHneo variando de 5-20 µU/ml. Crianças com TSHneo elevado são convocadas para avaliação e confirmação (25) (A).
Em alguns centros de triagem neonatal, crianças com valores de TSHneo entre 10-20 µU/ml são reconvocadas para uma segunda coleta em papel-filtro e, somente após esse resultado - caso o TSH se apresente acima de 10 µU/ml -, a criança é convocada para a confirmação no soro.
Com a dosagem inicial de TSH apenas, crianças com hipotireoidismo central ou que apresentarem elevação tardia do TSH poderão ser perdidas. Elevações tardias de TSH são particularmente comuns nas crianças com baixo peso ao nascimento (PN < 2.500 g) e em prematuros (39) (B).
Quando a triagem é feita com a dosagem inicial de T4 seguida da dosagem de TSH, além de permitir a detecção dos casos de hipotireoidismo primário, poderá detectar o hipotireoidismo central e identificar crianças com deficiência de proteína transportadora de hormônio tireoidiano (TBG). Essas últimas apresentam T4 total (T4T) baixo e T4 livre (T4L) normal e não requererão tratamento para o HC. Entretanto, essa abordagem não detectará crianças com HC e que apresentam T4 normal por disfunções tireoidianas mais leves. Uma comparação entre as duas abordagens que envolvem as dosagens de TSH e T4 em sequências diferentes mostrou que 1 criança entre 93.000 triadas não seria diagnosticada com a abordagem inicial com T4, o que não aconteceria, caso se utilizasse o TSH como o exame inicial (40) (B).
Recomendação 7
No Brasil, a triagem neonatal para HC é realizada por meio da dosagem de TSH em papel-filtro, seguida de dosagem de T4 total e/ou livre no soro, quando necessária. Essa estratégia é eficaz e também adotada em outros países (A).
8. OS TESTES DE TRIAGEM COM RESULTADOS ALTERADOS DEVEM SER CONFIRMADOS?
Os testes de triagem neonatal para HC não são diagnósticos e os resultados alterados devem ser confirmados por métodos quantitativos de rotina para as dosagens de concentrações séricas de TSH e T4T ou T4L (41) (B). A maioria dos testes confirmatórios deve ocorrer por volta da primeira à segunda semana de vida do RN, quando a faixa superior de normalidade para o TSH caiu para 10 µU/mL. Deve-se ter presente que a faixa de normalidade é diferente da observada em adultos. Assim, entre 4 e 30 dias de vida do RN, a faixa normal de T4T é de 7-16 µg/dL e de T4L de 0,8 a 2,3 ng/dL (42). Valores de TSH acima de 10 µU/mL e T4L ou T4T baixos confirmam o diagnóstico do hipotireoidismo primário e as crianças deverão ser tratadas (36).
Crianças com TSH confirmatório entre 6-10 µU/mL e T4T/T4L normais deverão ser seguidas cuidadosamente com novas dosagens em uma semana. Caso o TSH persista discretamente elevado por volta de 1 mês de idade da criança, mesmo com T4 na faixa da normalidade, alguns pesquisadores sugerem o tratamento com reavaliação após os 3 anos (19,43) (B,D). Crianças prematuras e doentes de qualquer natureza (síndrome do doente eutireoidiano) poderão ter T4T/T4L baixos com TSH normal e não se recomenda o tratamento com L-T4, a não ser que apresentem evidências de doença hipotalâmica ou hipofisária (44).
Recomendação 8
Os testes de triagem para hipotireoidismo congênito com resultados alterados devem ser confirmados por meio da dosagem quantitativa venosa de TSH, T4T/T4L (B).
9. IDENTIFICAÇÃO DA ETIOLOGIA DO HIPOTIREOIDISMO
Se o diagnóstico de hipotireoidismo for confirmado, outros estudos serão necessários para a pesquisa da etiologia da doença; entretanto, a decisão de se tratar a doença é baseada nas dosagens hormonais e os exames adicionais são opcionais, não devendo ser motivo para o retardo do início do tratamento.
Os exames que podem ser solicitados para a elucidação etiológica do HC são:
Ultrassonografia cervical - seria o principal exame inicial. Uma vez localizada a tireoide, a agenesia ou ectopia seriam descartadas. Entretanto, a ultrassonografia é menos sensível que a cintilografia tireoidiana para a detecção da glândula ectópica, apesar de a ultrassonografia com Doppler poder identificar 90% das glândulas ectópicas (45). A ultrassonografia apresenta sensibilidade e especificidade de 90,5% e 47,8%, respectivamente, para o diagnóstico de agenesia, e 100% e 80,4%, respectivamente, para hipoplasia, porém tem baixa sensibilidade para o diagnóstico de ectopia (somente 10%) (46) (B). Apresenta como vantagens evitar a exposição à radiação e ter menor custo (47) (B).
Mapeamento com 99mTc - indicado quando a ultrassonografia não detecta a glândula ectópica. A cintilografia poderá ser feita com pertecnetato de tecnésio (99mTc) ou iodo (123I), em vez do 131I, devido à menor irradiação que proporciona à criança. Bócio pode ser observado quando existe um defeito enzimático. Possui sensibilidade e especificidade de 92% e 97,1%, respectivamente, nos casos de glândula ectópica (46) (B).
Dosagem de tireoglobulina - existe uma grande sobreposição de valores de tireoglobulina nas diferentes etiologias de HC e, portanto, ela é utilizada em situações especiais. A associação entre o nível da tireoglobulina e a ultrassonografia pode distinguir entre atireose e ectopia glandular. Se não é visualizado nenhum tecido tireoidiano em localização normal e os níveis de T4 e tireoglobulina são mensuráveis, algum tecido funcional ectópico está presente (36,42).
Dosagens de anticorpos antitireoidianos (anticorpo antiperoxidase [TPO] e anticorpo bloqueador do receptor do TSH [TRAb]) - podem ser úteis para justificar a presença de TSH elevado em filhos de mães com tireoidite de Hashimoto (hipotireoidismo transitório), assim como em filhos de mães com doença de Graves (36).
Iodúria - poderá confirmar a falta ou excesso de iodo em casos suspeitos, e o tratamento com L-T4 deverá ser instituído por vários meses até ser gradualmente reduzido.
Recomendação 9
Exames complementares são utilizados para estudar a etiologia do hipotireoidismo congênito (B), mas nunca devem postergar o início do tratamento.
10. QUANDO O TRATAMENTO DEVE SER INICIADO?
A idade de início do tratamento, a dose de L-T4 administrada e o monitoramento do tratamento são essenciais para o desenvolvimento cerebral do paciente com HC. Existe uma relação inversa entre a idade do diagnóstico/tratamento e o quociente de inteligência (QI). Crianças detectadas pelos programas de triagem neonatal e tratadas nas primeiras semanas de vida geralmente têm QI normal, embora alguns estudos mostrem alguns déficits cognitivos (48,49) (B).
Recomendação 10
O início do tratamento deve ser o mais precoce possível, preferencialmente nas duas primeiras semanas de vida (B).
11. A TERAPÊUTICA COM L-T4 SÓDICA É EFICAZ PARA A NORMALIZAÇÃO DOS NÍVEIS HORMONAIS NA CRIANÇA COM HIPOTIREOIDISMO CONGÊNITO?
A administração oral de L-T4 sódica é o tratamento de escolha para o HC. A dose recomendada pela Academia Americana de Pediatria é de 10-15 µg/kg/dia e deve ser iniciada o mais precocemente possível, idealmente até 14 dias de vida, mesmo na ausência de sintomas (36) (D). Estudos mostram que com essas doses as concentrações de T4L ou T4T se normalizarão em três dias e as de TSH, em duas a quatro semanas (50) (A).
Devem ser utilizados comprimidos de L-T4, uma vez que não existe aprovação de soluções líquidas do hormônio. O comprimido deve ser macerado e dissolvido com pequena quantidade de água e administrado pela manhã, idealmente em jejum. Manter 30 minutos sem alimentação. Em caso de vômitos imediatos, repetir a mesma dose. Com boa absorção por via oral, e com meia-vida de aproximadamente sete dias, a L-T4 é administrada em dose única diária (36) (D). Apesar de ser recomendada a administração com estômago vazio e evitar alimentação após 30-60 minutos, isso não é prático em uma criança. Assim, a L-T4 poderá ser administrada no intervalo entre as mamadas e as doses devem ser ajustadas baseando-se nas concentrações séricas dos hormônios. A L-T4 não pode ser administrada com outras substâncias que interferem na sua absorção, como soja, ferro ou cálcio.
Recomendação 11
O tratamento do HC deve se iniciado o mais precocemente possível, preferencialmente antes de 15 dias de vida. É recomendada levotiroxina por via oral, na dose inicial de 10-15 µg/kg/dia (A).
12. COMO DEVE SER MONITORADO O TRATAMENTO?
O desenvolvimento do cérebro tem uma dependência importante dos hormônios tireoidianos nos primeiros dois a três anos. Existem estudos que mostram que concentrações persistentemente baixas de T4 sérico (T4T abaixo de 10 µU/mL) no primeiro ano de vida foram associadas à QI inferior a 18 pontos (51) (B). As recomendações da Academia Americana de Pediatria (36) (D) quanto ao tratamento e monitoramento das crianças estão na tabela 3 (43).
Testes laboratoriais mais frequentes poderão ser necessários quando não há boa aderência ao tratamento, valores anormais observados ou nas mudanças de posologias.
A meta do tratamento é assegurar à criança o crescimento adequado e o desenvolvimento psicomotor mais próximo possível do seu potencial genético.
Cuidado terá que se ter para evitar tratamento excessivo por período prolongado, pois isso poderá levar a craniossinostose e alterações no temperamento da criança (51).
Recomendação 12
A monitorização do tratamento do hipotireoidismo congênito necessita ser mais frequente nos primeiros anos da vida, pois o desenvolvimento cerebral é dependente da reposição hormonal, mas o acompanhamento deverá ser mantido até a idade de adulto (B).
Recebido em 19/Mar/2013
Aceito em 19/Mar/2013
Declaração: os autores declaram não haver conflitos de interesse científico neste estudo.
- 1. Waller DK, Anderson JL, Lorey F, Cunningham GC. Risk factors for congenital hypothyroidism: an investigation of infant's birth weight, ethnicity, and gender in California, 1990-1998. Teratology. 2000;62(1):36-41.
- 2. Corbetta C, Weber G, Cortinovis F, Calebiro D, Passoni A, Vigone MC, et al. A 7-year experience with low blood TSH cutoff levels for neonatal screening reveals an unsuspected frequency of congenital hypothyroidism (CH). Clin Endocrinol (Oxf). 2009;71(5):739-45.
- 3. Ramos HE, Nesi-França S, Maciel RM. New aspects of genetics and molecular mechanisms on thyroid morphogenesis for the understanding of thyroid dysgenesia. Arq Bras Endocrinol Metabol. 2008;52(9):1403-15.
- 4. Magalhães PK, Turcato M de F, Angulo Ide L, Maciel LM. Neonatal screening program at the university hospital of the Ribeirão Preto School of Medicine, São Paulo University, Brazil. Cad Saude Publica. 2009;25(2):445-54.
- 5. Harris KB, Pass KA. Increase in congenital hypothyroidism in New York State and in the United States. Mol Genet Metab. 2007;91(3):268-77.
- 6. Shapira SK, Lloyd-Puryear MA, Boyle C. Future research directions to identify causes of the increasing incidence rate of congenital hypothyroidism in the United States. Pediatrics. 2010;125 Suppl 2:S64-8.
- 7. Parks JS, Lin M, Grosse SD, Hinton CF, Drummond-Borg M, Borgfeld L, et al. The impact of transient hypothyroidism on the increasing rate of congenital hypothyroidism in the United States. Pediatrics. 2010;125 Suppl 2:S54-63.
- 8. Olney RS, Grosse SD, Vogt RF Jr. Prevalence of congenital hypothyroidism--current trends and future directions: workshop summary. Pediatrics. 2010;125 Suppl 2:S31-6.
- 9. Hertzberg V, Mei J, Therrell BL. Effect of laboratory practices on the incidence rate of congenital hypothyroidism. Pediatrics. 2010;125 Suppl 2:S48-53.
- 10. Roberts HE, Moore CA, Fernhoff PM, Brown AL, Khoury MJ. Population study of congenital hypothyroidism and associated birth defects, Atlanta, 1979-1992. Am J Med Genet. 1997;71(1):29-32.
- 11. Park SM, Chatterjee VK. Genetics of congenital hypothyroidism. J Med Genet. 2005;42(5):379-89.
- 12. Al Taji E, Biebermann H, Límanová Z, Hníková O, Zikmund J, Dame C, et al. Screening for mutations in transcription factors in a Czech cohort of 170 patients with congenital and early-onset hypothyroidism: identification of a novel PAX8 mutation in dominantly inherited early-onset non-autoimmune hypothyroidism. Eur J Endocrinol. 2007;156(5):521-9.
- 13. Cangul H, Aycan Z, Olivera-Nappa A, Saglam H, Schoenmakers NA, Boelaert K, et al. Thyroid dyshormonogenesis is mainly caused by TPO mutations in consanguineous community. Clin Endocrinol (Oxf). 2012 Dec 13. doi: 10.1111/cen.12127. [Epub ahead of print]
- 14. Friesema EC, Grueters A, Biebermann H, Krude H, von Moers A, Reeser M, et al. Association between mutations in a thyroid hormone transporter and severe X-linked psychomotor retardation. Lancet. 2004;364(9443):1435-7.
- 15. Refetoff S, Weiss RE, Usala SJ. The syndromes of resistance to thyroid hormone. Endocr Rev. 1993;14(3):348-99.
- 16. Alberti L, Proverbio MC, Costagliola S, Romoli R, Boldrighini B, Vigone MC, et al. Germline mutations of TSH receptor gene as cause of nonautoimmune subclinical hypothyroidism. J Clin Endocrinol Metab. 2002;87(6):2549-55.
- 17. Hanna CE, Krainz PL, Skeels MR, Miyahira RS, Sesser DE, LaFranchi SH. Detection of congenital hypopituitary hypothyroidism: ten-year experience in the Northwest Regional Screening Program. J Pediatr. 1986;109(6):959-64.
- 18. Persani L. Clinical review: central hypothyroidism: pathogenic, diagnostic, and therapeutic challenges. J Clin Endocrinol Metab. 2012;97(9):3068-78.
- 19. Korzeniewski SJ, Grigorescu V, Kleyn M, Young WI, Birbeck G, Todem D, et al. Transient hypothyroidism at 3-year follow-up among cases of congenital hypothyroidism detected by newborn screening. J Pediatr. 2013;162(1):177-82.
- 20. Alm J, Hagenfeldt L, Larsson A, Lundberg K. Incidence of congenital hypothyroidism: retrospective study of neonatal laboratory screening versus clinical symptoms as indicators leading to diagnosis. Br Med J (Clin Res Ed). 1984;289(6453):1171-5.
- 21. Vulsma T, Gons MH, de Vijlder JJ. Maternal-fetal transfer of thyroxine in congenital hypothyroidism due to a total organification defect or thyroid agenesis. N Engl J Med. 1989;321(1):13-6.
- 22. LaFranchi SH, Murphey WH, Foley TP Jr, Larsen PR, Buist NR. Neonatal hypothyroidism detected by the Northwest Regional Screening Program. Pediatrics. 1979;63(2):180-91.
- 23. Ramos JC, Lacerda Filho Ld, DeMartini Ade A, Silveira RB, Pereira RM, Sandrini Neto R, et al. Clinical and laboratory features of children and adolescents with congenital hypothyroidism due to dyshormonogenesis in southern Brazil. Arq Bras Endocrinol Metabol. 2012;56(3):201-8.
- 24. Grant DB, Smith I, Fuggle PW, Tokar S, Chapple J. Congenital hypothyroidism detected by neonatal screening: relationship between biochemical severity and early clinical features. Arch Dis Child. 1992;67(1):87-90.
- 25. Nascimento ML, Rabello FH, Ohira M, Simoni G, Cechinel E, Linhares RM, da Silva PC. [Newborn Screening Program for congenital hypothyroidism of the State of Santa Catarina, Brazil: etiological investigation in the first visit]. Arq Bras Endocrinol Metabol. 2012;56(9):627-32.
- 26. Olivieri A, Stazi MA, Mastroiacovo P, Fazzini C, Medda E, Spagnolo A, et al.; Study Group for Congenital Hypothyroidism. A population-based study on the frequency of additional congenital malformations in infants with congenital hypothyroidism: data from the Italian Registry for Congenital Hypothyroidism (1991-1998). J Clin Endocrinol Metab. 2002;87(2):557-62.
- 27. Kumar J, Gordillo R, Kaskel FJ, Druschel CM, Woroniecki RP. Increased prevalence of renal and urinary tract anomalies in children with congenital hypothyroidism. J Pediatr. 2009;154(2):263-6.
- 28. Castanet M, Park SM, Smith A, Bost M, Léger J, Lyonnet S, et al. A novel loss-of-function mutation in TTF-2 is associated with congenital hypothyroidism, thyroid agenesis and cleft palate. Hum Mol Genet. 2002;11(17):2051-9.
- 29. Doyle DA, Gonzalez I, Thomas B, Scavina M. Autosomal dominant transmission of congenital hypothyroidism, neonatal respiratory distress, and ataxia caused by a mutation of NKX2-1. J Pediatr. 2004;145(2):190-3.
- 30. Pharoah PO, Buttfield IH, Hetzel BS. Neurological damage to the fetus resulting from severe iodine deficiency during pregnancy. Lancet. 1971;1(7694):308-10.
- 31. Léger J, Ecosse E, Roussey M, Lanoë JL, Larroque B; French Congenital Hypothyroidism Study Group. Subtle health impairment and socioeducational attainment in young adult patients with congenital hypothyroidism diagnosed by neonatal screening: a longitudinal population-based cohort study. J Clin Endocrinol Metab. 2011;96(6):1771-82.
- 32. Azar-Kolakez A, Ecosse E, Dos Santos S, Léger J. All-cause and disease-specific mortality and morbidity in patients with congenital hypothyroidism treated since the neonatal period: a national population-based study. J Clin Endocrinol Metab. 2013;98(2):785-93.
- 33. Bongers-Schokking JJ, Koot HM, Wiersma D, Verkerk PH, de Muinck Keizer-Schrama SM. Influence of timing and dose of thyroid hormone replacement on development in infants with congenital hypothyroidism. J Pediatr. 2000;136(3):292-7.
- 34. Pharoah PO, Madden MP. Audit of screening for congenital hypothyroidism. Arch Dis Child. 1992;67(9):1073-6.
- 35. Kwon C, Farrell PM. The magnitude and challenge of false-positive newborn screening test results. Arch Pediatr Adolesc Med. 2000;154(7):714-8.
- 36. American Academy of Pediatrics, Rose SR; Section on Endocrinology and Committee on Genetics, American Thyroid Association, Brown RS; Public Health Committee, Lawson Wilkins Pediatric Endocrine Society, Foley T, Kaplowitz PB, Kaye CI, Sundararajan S, Varma SK. Update of newborn screening and therapy for congenital hypothyroidism. Pediatrics. 2006;117(6):2290-303.
- 37. Kaye CI; Committee on Genetics, Accurso F, La Franchi S, Lane PA, Northrup H, et al. Introduction to the newborn screening fact sheets. Pediatrics. 2006;118(3):1304-12.
- 38. Korzeniewski SJ, Grigorescu V, Kleyn M, Young W, Birbeck GL, Todem D, et al. Performance metrics after changes in screening protocol for congenital hypothyroidism. Pediatrics. 2012;130(5):e1252-60.
- 39. Tylek-Lemańska D, Kumorowicz-Kopiec M, Starzyk J. Screening for congenital hypothyroidism: the value of retesting after four weeks in neonates with low and very low birth weight. J Med Screen. 2005;12(4):166-9.
- 40. Dussault JH, Morissette J. Higher sensitivity of primary thyrotropin in screening for congenital hypothyroidism: a myth? J Clin Endocrinol Metab. 1983;56(4):849-52.
- 41. Zilka LJ, Lott JA, Baker LC, Linard SM. Finding blunders in thyroid testing: experience in newborns. J Clin Lab Anal. 2008;22(4):254-6.
- 42. Elmlinger MW, Kühnel W, Lambrecht HG, Ranke MB. Reference intervals from birth to adulthood for serum thyroxine (T4), triiodothyronine (T3), free T3, free T4, thyroxine binding globulin (TBG) and thyrotropin (TSH). Clin Chem Lab Med. 2001;39(10):973-9.
- 43. LaFranchi SH. Approach to the diagnosis and treatment of neonatal hypothyroidism. J Clin Endocrinol Metab. 2011;96(10):2959-67.
- 44. Larson C, Hermos R, Delaney A, Daley D, Mitchell M. Risk factors associated with delayed thyrotropin elevations in congenital hypothyroidism. J Pediatr. 2003;143(5):587-91.
- 45. Ohnishi H, Sato H, Noda H, Inomata H, Sasaki N. Color Doppler ultrasonography: diagnosis of ectopic thyroid gland in patients with congenital hypothyroidism caused by thyroid dysgenesis. J Clin Endocrinol Metab. 2003;88(11):5145-9.
- 46. Karakoc-Aydiner E, Turan S, Akpinar I, Dede F, Isguven P, Adal E, et al. Pitfalls in the diagnosis of thyroid dysgenesis by thyroid ultrasonography and scintigraphy. Eur J Endocrinol. 2012;166(1):43-8.
- 47. Supakul N, Delaney LR, Siddiqui AR, Jennings SG, Eugster EA, Karmazyn B. Ultrasound for primary imaging of congenital hypothyroidism. AJR Am J Roentgenol. 2012;199(3):W360-6.
- 48. LaFranchi SH, Austin J. How should we be treating children with congenital hypothyroidism? J Pediatr Endocrinol Metab. 2007;20(5):559-78.
- 49. Huo K, Zhang Z, Zhao D, Li H, Wang J, Wang X, et al. Risk factors for neurodevelopmental deficits in congenital hypothyroidism after early substitution treatment. Endocr J. 2011;58(5):355-61.
- 50. Selva KA, Mandel SH, Rien L, Sesser D, Miyahira R, Skeels M, et al. Initial treatment dose of L-thyroxine in congenital hypothyroidism. J Pediatr. 2002;141(6):786-92.
- 51. Rovet J, Alvarez M. Thyroid hormone and attention in congenital hypothyroidism. J Pediatr Endocrinol Metab. 1996;9(1):63-6.
Correspondência para:
Datas de Publicação
-
Publicação nesta coleção
10 Maio 2013 -
Data do Fascículo
Abr 2013
Histórico
-
Recebido
19 Mar 2013 -
Aceito
19 Mar 2013