Resumos
A Artrite Encefalite Caprina (AEC) e a Linfadenite Caseosa (LC) possuem alta incidência e transmissibilidade em pequenos ruminantes. Como ambas possuem tropismo por monócitos-macrófagos e afetam mecanismos da resposta inata do hospedeiro, acredita-se que a AEC predispõe o animal a infecções por Corynebacteruim pseudotuberculosis, agente etiológico da LC. Para confirmar esta hipótese, avaliou-se a fagocitose de células da série monócito-macrófago de cabras naturalmente infectadas pelo vírus da AEC (VAEC). Para tanto, foram utilizadas 30 cabras da raça Saanen, alocadas em dois grupos distintos, com 15 animais cada, conforme a sororreatividade de anticorpos séricos antivírus da AEC. Células mononucleares de sangue periférico foram isoladas por gradiente de densidade e plaqueadas para isolamento de células da série monócito-macrófago. Posteriormente, o ensaio de fagocitose de C. pseudotuberculosis foi realizado, após incubação por duas horas a 37ºC a 5% de CO2, e a visualização da fagocitose foi identificada por microscopia óptica. O presente estudo não encontrou diferença na porcentagem de monócito-macrófagos que realizaram fagocitose entre os diferentes grupos (P = 0,41). Todavia, a análise quantitativa de bactérias fagocitadas, demonstrou maior capacidade fagocítica pelos macrófagos-monócitos do grupo sororreagente ao vírus da AEC. Correlação entre monócitos fagocitando e macrófagos que fagocitaram mais de 12 bactérias foi observado neste grupo (r = 0,488; P = 0,006), não sendo o mesmo encontrado no grupo de animais sorroreagentes negativos. Os dados demonstram aumento na intensidade da fagocitose de macrófagos de animais infectados com o vírus da AEC.
Linfadenite caseosa; artrite encefalite caprina; fagócitos; células mononucleares; caprinos
Caprine arthritis encephalitis (CAE) and caseous lymphadenitis (CL) have high incidence and transmissibility in small ruminants. Since both virus have tropism for macrophages and monocytes and affect the innate immune response, it is believed that CAE can predispose the animal to infection by Corynebacteruim pseudotuberculosis, the etiological agent of CL. To confirm this hypothesis, we evaluated phagocytosis from the monocyte-macrophage cells from 30 Saanen goats. Goats were uniformly divided in two groups according to results of agar gel immunodiffusion test for CAE virus (CAEV). Peripheral blood mononuclear cells were isolated by density gradient centrifugation and the monocyte-macrophage cells were isolated from the mononuclear cells by their adhesion properties in plaques. Afterwards, phagocytosis of C. psudotuberculosis was performed for two hours at 37ºC, 5% of CO2, and assessed by microscopic visualization. There was no difference in the percentage of monocyte-macrophage cells that phagocytozed C. bovis between groups (P=0.41). However, when phagocytosis rates were classified according to the number of C. pseudotuberculosis phagocyted, the percentage of monocyte-macrophage cells that internalized more than 12 bacteria were higher in serologically CAEV positive animals compared to the serologically negative ones (P<0.001). Furthermore, a positive and significant correlation (r = 0.488; P = 0.006) between the percentage of monocyte-macrophage cells that internalized more than 12 bacteria and the percentage of monocyte that were carrying out phagocytosis was also encountered in serologically CAEV positive goats, however the same were not observed in serologically negative ones. These results demonstrated an alteration in the intensity of C. pseudotuberculosis phagocytosis by monocytes-macrophages from goats infected by CAEV. Thus, these results indicated that goats infected with CAEV may be more susceptible to CL.
Caseous lymphadenitis; caprine arthritis encephalitis; phagocytes; mononuclear cells; caprine
ANIMAIS DE PRODUÇÃO
Fagocitose intensificada de Corynebacterium pseudotuberculosis por células da série monócito-macrófago de caprinos naturalmente infectados pelo vírus da artrite encefalite
Enhanced phagocytosis of Corynebacterium pseudotuberculosis by monocyte-macrophage cells from goats naturally infected with caprine arthritis encephalitis vírus
Bárbara G.S. Sanches; Fernando N. Souza; Milton R. Azedo; Camila F. Batista* * Autor para correspondência: camilafb@usp.br ; Heloisa G. Bertagnon; Maiara G. Blagitz; Alice M.M.P. Della Libera
Departamento de Clínica Médica, Faculdade de Medicina Veterinária e Zootecnia, Universidade de São Paulo (USP), Av. Prof. Dr. Orlando Marques de Paiva 87, São Paulo, SP 05508-270, Brazil
RESUMO
A Artrite Encefalite Caprina (AEC) e a Linfadenite Caseosa (LC) possuem alta incidência e transmissibilidade em pequenos ruminantes. Como ambas possuem tropismo por monócitos-macrófagos e afetam mecanismos da resposta inata do hospedeiro, acredita-se que a AEC predispõe o animal a infecções por Corynebacteruim pseudotuberculosis, agente etiológico da LC. Para confirmar esta hipótese, avaliou-se a fagocitose de células da série monócito-macrófago de cabras naturalmente infectadas pelo vírus da AEC (VAEC). Para tanto, foram utilizadas 30 cabras da raça Saanen, alocadas em dois grupos distintos, com 15 animais cada, conforme a sororreatividade de anticorpos séricos antivírus da AEC. Células mononucleares de sangue periférico foram isoladas por gradiente de densidade e plaqueadas para isolamento de células da série monócito-macrófago. Posteriormente, o ensaio de fagocitose de C. pseudotuberculosis foi realizado, após incubação por duas horas a 37ºC a 5% de CO2, e a visualização da fagocitose foi identificada por microscopia óptica. O presente estudo não encontrou diferença na porcentagem de monócito-macrófagos que realizaram fagocitose entre os diferentes grupos (P = 0,41). Todavia, a análise quantitativa de bactérias fagocitadas, demonstrou maior capacidade fagocítica pelos macrófagos-monócitos do grupo sororreagente ao vírus da AEC. Correlação entre monócitos fagocitando e macrófagos que fagocitaram mais de 12 bactérias foi observado neste grupo (r = 0,488; P = 0,006), não sendo o mesmo encontrado no grupo de animais sorroreagentes negativos. Os dados demonstram aumento na intensidade da fagocitose de macrófagos de animais infectados com o vírus da AEC.
Termos de indexação: Linfadenite caseosa, artrite encefalite caprina, fagócitos, células mononucleares, caprinos.
ABSTRACT
Caprine arthritis encephalitis (CAE) and caseous lymphadenitis (CL) have high incidence and transmissibility in small ruminants. Since both virus have tropism for macrophages and monocytes and affect the innate immune response, it is believed that CAE can predispose the animal to infection by Corynebacteruim pseudotuberculosis, the etiological agent of CL. To confirm this hypothesis, we evaluated phagocytosis from the monocyte-macrophage cells from 30 Saanen goats. Goats were uniformly divided in two groups according to results of agar gel immunodiffusion test for CAE virus (CAEV). Peripheral blood mononuclear cells were isolated by density gradient centrifugation and the monocyte-macrophage cells were isolated from the mononuclear cells by their adhesion properties in plaques. Afterwards, phagocytosis of C. psudotuberculosis was performed for two hours at 37ºC, 5% of CO2, and assessed by microscopic visualization. There was no difference in the percentage of monocyte-macrophage cells that phagocytozed C. bovis between groups (P=0.41). However, when phagocytosis rates were classified according to the number of C. pseudotuberculosis phagocyted, the percentage of monocyte-macrophage cells that internalized more than 12 bacteria were higher in serologically CAEV positive animals compared to the serologically negative ones (P<0.001). Furthermore, a positive and significant correlation (r = 0.488; P = 0.006) between the percentage of monocyte-macrophage cells that internalized more than 12 bacteria and the percentage of monocyte that were carrying out phagocytosis was also encountered in serologically CAEV positive goats, however the same were not observed in serologically negative ones. These results demonstrated an alteration in the intensity of C. pseudotuberculosis phagocytosis by monocytes-macrophages from goats infected by CAEV. Thus, these results indicated that goats infected with CAEV may be more susceptible to CL.
Index terms: Caseous lymphadenitis, caprine arthritis encephalitis, phagocytes, mononuclear cells, caprine.
INTRODUÇÃO
Afecções como a artrite encefalite caprina (AEC) e a linfadenitecaseosa (LC) são mundialmente disseminadas, inclusive no Brasil, e apesar de não causarem sintomatologia expressiva na maioria das vezes, estão implicadas na baixa produtividade dos animais (Ribeiro et al. 2011, Souza et al. 2011, Andrade et al. 2012). O vírus da AEC (VAEC) e Corynebacterium pseudotuberculosis, agente etiológico da LC, apresentam em comum o tropismo pelas células da série monócito-macrófago, que disseminam os agentes no hospedeiro (Lara et al. 2005, Blacklaws 2012).
O vírus da AEC (VAEC), da família Retroviridae possui similiaridade com outros vírus causadores de imunodeficiências, como o vírus da imunodeficiência humana (HIV) (Quinn et al. 2005, Al-Qudah et al. 2006). A infecção pelo vírus da AEC compromete a função de linfócitos T auxiliares (Zink et al. 1990), resultando na redução da produção de citocinas ou alteração de seu perfil de produção, o que pode prejudicar tanto a resposta celular como a resposta humoral contra o vírus (Fluri et al. 2006).
A LC é causada por um actinomiceto que possui similaridades com o Mycobacterium pseudotuberculosis. Ambos possuem lipídeos em sua parede celular que dificultam a fagocitose da bactéria promovendo toxicidade às células do hospedeiro (Tashjian & Campbell 1983). Pelo fato de ser um patógeno intracelular facultativo, a imunidade contra C. pseudotuberculosis é complexa e envolve principalmente a resposta imune celular (Ellis et al. 1990, Prescott 2002). No entanto, as células cronicamente infectadas parecem ter sua função diminuída, favorecendo a permanência do patógeno no hospedeiro (Mueller & Pieters 2006).
Outro fator a ser considerado é que a forma pulmonar da infecção por C. pseudotuberculosis ocorre com mais frequência em ovinos infectados por lentiviroses (Brodie et al. 1992). É também reportado, em humanos, que a infecção por Mycobacterium tuberculosis é mais comum nos indivíduos portadores do HIV, e que esta doença bacteriana pode acelerar a progressão desta última (Elner 1990). Estas duas infecções parecem ter efeito sinérgico causando uma mudança a favor dos seus agentes etiológicos que não pode ser revertida pelo tratamento com agentes antimicobacterianos (Wallis & Ellner 1994). Foi então sugerido que as infecções micobacterianas poderiam causar aumento na produção de interleucina (IL)-6, a qual suprime a resposta imune celular. Deste modo, a IL-6, assim como a IL-1 e o TNF-alfa, foram implicadas na indução da replicação do HIV (Van Heyningen et al. 1997). Destarte, sendo o vírus da AEC pertencente à mesma família e ao mesmo gênero do HIV (Quinn et al. 2005) e C. pseudotuberculosis, um actinomiceto como M. tuberculosis (Dorella et al. 2006), e considerando suas similaridades na modulação da resposta imune, acredita-se que a progressão destas doenças também pode apresentar um efeito sinérgico entre si. Estudos também apontam que mediadores solúveis secretados na resposta frente a esta bactéria podem modular a replicação de lentivírus, e, por extensão, favorecer a progressão da doença em ovinos infectados por ambas enfermidades (Ellis et al. 1994).
Uma vez que ambas as afecções AEC e LC possuem alta incidência e transmissibilidade, além dos agentes etiológicos destas enfermidades possuírem tropismo por monócitos-macrófagos, o presente estudo teve como objetivo avaliar a fagocitose C. pseudotuberculosis por células da série monócito-macrófago de cabras naturalmente infectadas pelo VAEC.
MATERIAL E MÉTODOS
Foram coletadas amostras sanguíneas de 30 cabras adultas da raça Saanen, sem alterações no exame clinico e no hemograma, distribuídas uniformemente em dois grupos conforme a reatividade do soro sanguíneo ao vírus da AEC. O sorodiagnóstico deu-se por kit comercial (Biovetech, Brasil) utilizando o antígeno proteico (p28) extraído do capsídeo do vírus da AEC, e a leitura realizada após 48 e 72 horas de incubação.
A cepa de C. pseudotuberculosis utilizada no ensaio de fagocitose foi isolada por punção aspirativa de linfonodo aumentado de caprino com LC, e, posteriormente, semeada em placas de ágar-sangue contendo 5% de sangue de carneiro desfibrinado e incubadas a 37ºC por 72 horas. A identificação do agente etiológico foi feita por coloração de Gram, e por testes bioquímicos, através do kit ApiCoryne® (Biomérieux, França), conforme recomendações do fabricante.
A quantidade de C. pseudotuberculosis para o ensaio de fagocitose foi mensurada pela Escala de Mac Farland, correspondente a 30x108 bactérias/mL (Bier 1984), sendo utilizadas seis bactérias para cada célula mononuclear (6:1) (Kapetanovic et al. 2007, Rajavelu & das 2007).
O ensaio de fagocitose das células da série monócito-macrófagos foi realizado conforme descrito por Azedo et al. (2011) e Bastos et al. (2012) com algumas modificações. Resumidamente, as células mononucleares de sangue periférico (CMSP) foram isoladas por gradiente de densidade, utilizando Ficoll-Paque Plus® (GE Heathcare, Suécia), e ajustadas para 1 x 107 células mononucleares/mL viáveis, por exclusão do azul de trypan, adicionadas sobre lamínulas de vidro polidas de 13 mm de diâmetro em placas de 24 poços de poliestireno, e incubadas em estufa com 5% de CO2 a 37ºC, por 1 hora, para isolamento dos monócitos por sua propriedade de adesão em vidro (Stabel et al. 2007). Removidas da estufa, aos poços das placas foram instilados solução salina tamponada em temperatura ambiente para a remoção das células não aderentes. Posteriormente, foram adicionadas alíquotas de 20µL da suspensão contendo 6x107 de bactérias sobre as lamínulas de vidro dentro dos poços. As placas foram novamente incubadas a 37ºC durante 2 horas, em 5% de CO2, e fixadas com glutaraldeído a 0,5%, por 10 minutos.
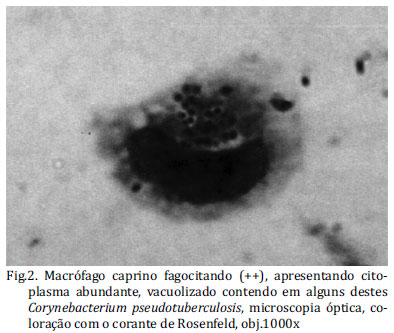
Para o teste de fagocitose procedeu-se à leitura das lamínulas em microscopia óptica em aumento de 1000 X, após coloração com o corante de Rosenfeld. Foram contadas 400 células, avaliando-se a porcentagem de monócitos aderidos, monócitos que fagocitaram C. pseudotuberculosis, macrófagos aderidos, macrófagos espraiados, macrófagos que fagocitaram até 12 C. pseudotuberculosis (Fagocitose +) e macrófagos que fagocitaram mais de 12 C. pseudotuberculosis; (Fagocitose ++) (Figura 2), conforme estabelecido por Rivas et al. (2002). Para determinar esta classificação, considerou-se o número de células bacterianas no interior dos vacúolos celulares (Fig.2).
A normalidade da distribuição dos dados foi verificada, utilizando-se do teste de Anderson-Darling, e sua homoscedasticidade, utilizando-se do teste F. Para a avaliação das diferenças entre as médias dos resultados, foi feito o teste de análise variância T. Para a avaliação das correlações entre os dados observados, foi realizada a análise do coeficiente de correlação de Pearson, utilizando-se critério de classificação indicado por Callegari-Jacques (2006). Para todos os resultados, foram consideradas significantes as análises que apresentaram P<0,05. Os dados estão expressos como média (± desvio padrão). Nas avaliações estatísticas, foi utilizado o software estatístico MINITAB®, versão 15 (Global Tech InformáticaTM, Belo Horizonte, MG).
RESULTADOS E DISCUSSÃO
A AEC e a LC são duas importantes afecções crônicas com diferentes agentes etiológicos, culminando em estudos sobre as duas afecções de forma isolada (Lara et al. 2005, Chirino-Zárraga et al. 2006). Baseando-se na hipótese de que as células alvo dos animais portadores do vírus tenham a função fagocítica comprometida ou alterada (Patel et al. 2012), predispondo a futuras infecções, como a LC, o presente trabalho avaliou a função fagocítica ex vivo de células da série monócito-macrófago de animais infectados pelo vírus da AEC utilizando-se da bactéria C. pseudotuberculosis.
Assim a análise dos grupos experimentais permitiu observar três importantes fenômenos: houve maior porcentagem de macrófagos com fagocitose ++ nas células obtidas do grupo de animais sororreagentes quando comparadas às células do grupo de animais não sororreagentes ao VAEC (P=0,001). Por sua vez, observou-se maior porcentagem de macrófagos com fagocitose + nas células obtidas do grupo de animais não sororreagentes, quando comparadas às células obtidas no grupo de animais sororreagentes (P=0,012) (Quadro 1). Ainda, correlação positiva no grupo dos animais sororreagentes entre macrófagos fagocitando ++ com monócitos fagocitando (r=0,488, P=0,006) foi evidenciada (Fig.1). Neste contexto sabe-se que um dos mecanismos mais importantes na resposta imune inata contra o VAEC é a produção de interferon tipo I, que pode interferir com a diferenciação dos monócitos (Blacklaws 2012), o que pode resultar na maturação de monócitos em macrófagos, supostamente favorecendo maior atividade fagocítica (Patel et al. 2012), demonstrada no presente estudo pela maior capacidade de realizar fagocitose, quando comparada às células dos animais não sororreagentes.
O percentual total de macrófagos fagocitando (fagocitose ++ e fagocitose +), assim como a porcentagem total de células fagocitando (macrófagos e monócitos) não diferiu entre os grupos (Tabela 1), em concordância com a literatura (Anderson et al. 1983). Esse é um dado importante, o qual demonstra não haver diferença na quantidade de células realizando fagocitose, independente se o animal apresenta ou não anticorpos antivírus da AEC.
Os fagócitos mononucleares apresentam papel fundamental na patogênese da infecção por C. pseudotuberculosis, fornecendo um nicho intracelular para sobrevivência e multiplicação deste bastonete gram-positivo intracelular facultativo, cuja evasão do sistema imune ocorre por inibição da formação do fagolisossomo, resultando em multiplicação da bactéria e morte celular, provocando lesão necrótica e liberação da bactéria (Walker et al. 1994). No entanto, deve-se salientar que a fagocitose de C. pseudotuberculosis pode variar de acordo com a cepa (Stefánska et al. 2010), embora Abreu et al. (2008), em condições brasileiras, encontrou um único padrão genotípico de C. pseudotuberculosis responsável por abscessos superficiais.
Pelo supra descrito, os resultados do presente estudo indicam para maior disseminação da LC em caprinos infectados pelo vírus da AEC, pois, neste grupo, houve uma maior quantidade de células bacterianas fagocitadas, o que poderia propiciar a disseminação do patógeno para outros tecidos e a formação de novos granulomas.
CONCLUSÃO
O presente estudo permitiu concluir que a infecção pelo vírus da artrite encefalite caprina ocasiona aumento na intensidade de fagocitose das células da série monócito-macrófago, sugerindo que a AEC predispõe os animais à LC e/ ou favorece a progressão da mesma, todavia mais estudos são necessários para confirmar esta hipótese.
Recebido em 2 de abril de 2012
Aceito para publicação em 31 de julho de 2012
- Abreu S.R.O., Mota R.A., Rosinha G.M.S., Forner O., Pinheiro Júnior J.W., Pereira R.R.B., de Castro R.S., Elisei C., Soares C.O., Araújo F.R. & Madureira R.C. 2008. Comparação genotípica de isolados de Corynebacterium pseudotuberculosis de caprinos e ovinos do sertão de Pernambuco. Pesq. Vet. Bras. 28(10):481-487.
- Al-Qudah K., Al-Majali A.M. & Ismail Z.B. 2006. Epidemiological studies on caprine arthritis-encephalitis virus infection in Jordan. Small Rumin. Res. 66(1/3):181-186.
- Anderson L.W., Klevjer-Anderson P. & Liggitif H.D. 1983. Susceptibility of blood-derived monocytes and macrophages to caprine arthritis-encephalitis virus. Infect. Immun. 41(2):837-840.
- Andrade J.S.L., Azevedo S.S., Teles J.A.A., Higino S.S.S. & Azevedo E.O. 2012. Ocorrência e fatores de risco associados à infecção por Corynebacterium pseudotuberculosis em caprinos e ovinos do semiárido paraibano. Pesq. Vet. Bras. 32(2):116-120.
- Azedo M.R., Blagitz M.G., Souza F.N., Benesi F.J. & Della Libera A.M.M.P. 2011. Avaliação funcional de monócitos de bovinos naturalmente infectados pelo vírus da leucose bovina. Arq. Bras. Med. Vet. Zootec. 63(5):1131-1140.
- Bastos C.R., Blagitz M.G., Souza F.N., Batista C.F., Stricagnolo C.R., Azedo M.R. & Della Libera A.M.M.P. 2012. Viabilidade celular, fagocitose e espraiamento de fagócitos mononucleares, e liberação de peróxido de hidrogênio por leucócitos de glândulas mamárias sadias e infectadas. Pesq. Vet. Bras. 32(9):850-854.
- Bier O. 1984, Microbiologia e Imunologia. 23Ş ed. Melhoramentos, São Paulo. p.930-931.
- Blacklaws B.A. 2012. Small ruminant lentiviruses: Immunopathogenesis of visna-maedi and caprine arthritis and encephalitis virus. Comp. Immunol. Microbiol. Infect. Dis. 35:259-269.
- Brodie S.J., Marcom H.A., Pearson L.D., Anderson B.C., Concha-Bremejillo A., Ellis J.A. & Demartini J.C. 1992. The effect of virus load in the pathogenesis of lentivirus-induced lymphoid intersticial pneumonia. J. Infect. Dis. 166(3):531-541.
- Callegari-Jacques S.M. 2003. Bioestatística: princípios e aplicações. Artmed, Porto Alegre. 256 p.
- Chirino-Zárraga C., Scaramelli A. & Rey-Valeiron C. 2006. Bacteriological characterization of Corynebacterium pseudotuberculosis in Venezuela goat flocks. Small Rumin. Res. 65(1/2):170-175.
- Dorella F.A., Pacheco L.G.C., Oliveira S.C., Miyoshi A. & Azevedo V. 2006. Corynebacterium pseudotuberculosis: Microbiology, biochemical properties, pathogenesis and molecular studies of virulence. Vet. Res. 37(2):201-218.
- Ellis J.A., Russell H.I. & Du C.W. 1994. Effect of selected cytokines on the replication of Corynebacterium pseudotuberculosis and ovine lentiviruses in the pulmonary macrophages. Vet. Immunol. Immunopathol. 40(1):31-47.
- Elner J.J. 1990. Tuberculosis in the time of AIDS: The facts and the message. Chest 98(5):1051-1052.
- Fluri A., Nenci C., Zahno M.L., Vogt H.R., Charan S., Busato A., Pancino G., Peterhans E., Obexer-Ruff G. & Bertoni G. 2006. The MHC-haplotype influences primary, but not memory, immune responses to an immunodominant peptide containing T- and B-cell epitopes of the caprine arthritis encephalitis virus Gag protein.Vaccine 24(5):597-606.
- Kapetanovic R., Nahori M.A., Balloy V., Fitting C., Philpott D.J., Cavaillon J.M. & Conquy M.A. 2007. Contribuition of phagocytosis by Staphylococcus aureus activated macrophages. Infect. Immun. 75(2):830-837.
- Lara M.C.C.S.H., BirgelJunior E.H., Gregory L. & Birgel E.H. 2005. Aspectos clínicos da artrite-encefalite dos caprinos. Arq. Bras. Med. Vet. Zootec. 57(6):736-740.
- Mueller P. & Pieters J. 2006. Modulation of macrophage antimicrobial mechanisms by pathogenic mycobacteria. Immunobiology 211(6/8):549-556.
- Patel J.R., Heldensb J.G.M., Bakinyic T. & Rusvais M. 2012. Important mammalian veterinary viral immunodiseases and their control. Vaccine 30(10):1767-1781.
- Prescott J.F., Mnzies P.I. & Hwang Y.T. 2002. An interferon-gamma assay for diagnosis of Corynebacterium pseudotuberculosis infection in adult sheep from a research flock. Vet. Microbiol. 88(3):287-297.
- Quinn P.J., Markey B.K., Carter M.E., Donnelly W.J. & Leonard F.C. 2005. Microbiologia Veterinária e Doenças Infecciosas. Artmed, Porto Alegre, p.67-70.
- Rajavelu P. & Das S.D. 2007. A correlation between phagocytosis and apoptosis in THP-1 cells infected with prevalent strains of Mycobacterium tuberculosis Microbiol. Immunol. 51(2):201-210.
- Ribeiro M.G., Belotta A.F., Fernandes M.C., Guena R., Nardi Júnior G., Lara G.H.B., Giuffrida R. & Zamprogna T.O. 2011. Citologia aspirativa no diagnóstico da linfadenite em ovinos. Pesq. Vet. Bras. 31(10):839-843.
- Rivas A.L., Tadevosyan R., Quimby F.W., Coksaygan T. & Lein D.H. 2002. Identification of subpopulations of bovine mammary-gland phagocytes and evaluation of sensitivity and specificity of morphologic and functional indicators of bovine mastitis. Can. J. Vet. Res. 66(3):165-167.
- Stabel J.R., Kehrli Jr M.E., Reinhardt T.A. & Nonnecke B.J. 1997. Functional assessment of bovine monocytes isolated from peripheral blood. Vet. Immunol. Immunopathol. 58(2):147-153.
- Stefánska I., Giervnska M., Rzewuska M. & Binek M. 2010. Survival of Corynebacterium pseudotuberculosis within macrophages and induction of phagocytes death. Pol. J. Vet. Sci. 13(1):143-149.
- Souza M.F., Carvalho A.Q., Garino Jr F. & Riet-Correa F. 2011. Linfadenite caseosa em ovinos deslanados abatidos em um frigorífico da Paraíba. Pesq. Vet. Bras. 31(3):224-230.
- Tashjian J.J. & Campbell S.G. 1983. Interaction between caprine macrophages and Corynebacterium pseudotuberculosis: An electron microscopic study. Am. J. Vet. Res. 44(4):690-693.
- Van Heyningen T.K., Collins H.L. & Russell D.G. 1997. IL-6 produced by macrophages infected with Mycobacterium species suppresses T cell responses. J. Immunol. 158(1):330-337.
- Walker J., Jackson H.J., Eggleton D.G., Meeusen E.N.T., Wilson M.J. & Brandon M.R. 1994. Identification of a novel antigen from Corynebacterium pseudotuberculosis that protects sheep against caseous lymphadenitis. Infect. Immun. 62(6):2562-2567.
- Wallis R. & Ellner J. 1994. Cytokines and tuberculosis. J. Leukocyte Biol. 55(5):676-681.
- Zink M.C., Yager J.A. & Myers J.D. 1990. Pathogenesis of caprine arthritis-encephalitis virus; Cellular localization of viral transcripts in tissues of infected goats. Am. J. Pathol. 136(4):843-854.
Datas de Publicação
-
Publicação nesta coleção
28 Jan 2013 -
Data do Fascículo
Dez 2012
Histórico
-
Recebido
02 Abr 2012 -
Aceito
31 Jul 2012