RESUMO:
Vinte e dois casos de meningiomas em cães, diagnosticados num período de aproximadamente 18 anos, foram revisados. Os neoplasmas foram graduados e classificados histologicamente de acordo com os critérios da Organização Mundial da Saúde (OMS de 2007) para meningiomas em humanos adaptados para cães, em Grau I (G-I; benignos), Grau II (G-II; atípicos) e Grau III (G-III; anaplásico ou maligno). Dos protocolos de necropsias foram retiradas adicionalmente informações referentes ao sexo, idade, raça, evolução clínica, sinais clínicos, localização anatômica e achados macroscópicos. Os meningiomas intracranianos supratentoriais foram os mais frequentes em relação às demais localizações intracranianas ou intraespinhais. Os intracranianos caracterizaram-se principalmente por sinais clínicos de alteração tálamo-cortical. Os intraespinhais caracterizaram-se principalmente por causarem ataxia. Meningiomas G-I foram os mais frequentes (63,6%) nos 22 cães, seguidos pelos G-III (22,7%) e G-II (13,6%). Os G-I caracterizaram-se por ter o subtipo psammomatoso como o mais frequente, mais de um padrão morfológico em um mesmo tumor, e um terço deles apresentando áreas de invasão do tecido nervoso, 71,4% dos casos acometendo fêmeas, uma média de idade de 11 anos, cães com raça definida como os mais acometidos e por ter o maior tempo de sobrevivência após a manifestação dos sinais clínicos. Os meningiomas G-II caracterizaram-se por ter o subtipo cordoide como o mais frequente, invasão do tecido nervoso em um terço dos casos, somente fêmeas acometidas, uma média de idade de 12 anos, dois terços dos cães acometidos sem raça definida e o tempo máximo de sobrevivência de 20 dias. Os meningiomas G-III caracterizaram-se por ter o subtipo papilar como o mais frequente, invasão do tecido nervoso em 80% dos casos, 60% dos casos acometendo fêmeas, uma média de idade de 8 anos, 80% dos cães acometidos da raça Boxer e o tempo máximo de sobrevivência de 90 dias. Este estudo permitiu estabelecer uma relação entre os três graus histológicos observados em 22 casos de meningiomas em cães com vários parâmetros clínico-epidemiológicos e patológicos, fornecendo informações úteis para um melhor conhecimento da correlação entre a graduação histológica e a evolução clínica desses neoplasmas.
TERMOS DE INDEXAÇÃO:
Meningiomas; neoplasmas encefálicos; graduação histológica; caninos; doenças de cães; patologia
ABSTRACT:
Twenty two cases of meningiomas in dogs, diagnosed in about 18 years, were analyzed. The neoplasms were histologicaly classified and graded according to the World and Health Organization (WHO of 2007) for human meningiomas, adapted for dogs, in Grade I (G-I; benign), Grade II (G-II; atypical), and Grade III (G-III; anaplastic or malignant). Additional data about gender, age, breed, skull conformation, clinical course and signs, anatomic localization, gross and histological findings were obtained from the necropsy reports. Intracranial and supratentorial meningiomas were the most frequent in relation to the other intracranial or intraspinal sites. The intracranial ones were characterized mainly by clinical signs of thalamic-cortical alteration. Intraspinal ones were mainly characterized by ataxia. G-I meningiomas were the most frequent (63.6%) in dogs, followed by G-III (22.7%) and G-II (13.6%). GI were characterized by having the psammomatous subtype as the most frequent, more than one morphological pattern in the same tumor, one third presenting areas of invasion of nervous tissue, 71.4% of cases involving females, a mean age of 11 years, pure breed dogs as the most affected ones and for having the longest survival time after the manifestation of clinical signs. G-II meningiomas were characterized by having the chordoid subtype as the most frequent, invasion of nervous tissue in one third of cases, only females affected, a mean age of 12 years, two-thirds of the dogs affected were mongrels and the maximum survival time of 20 days. The G-III meningiomas were characterized by having the papillary subtype as the most frequent, invasion of the nervous tissue in 80% of the cases, 60% of the cases involving females, a mean age of 8 years, 80% of dogs affected were Boxers and the maximum survival time of 90 days. In conclusion, this study allowed to establish a relationship between the three histological grades observed in 22 cases of meningiomas in dogs with various clinical-epidemiological and pathological parameters, providing useful information for a better understanding of the correlation between the histological grading and the clinical evolution of these neoplasms.
INDEX TERMS:
Meningioma; brain neoplasms; histological gradind; dogs; pathology
Introdução
Na rotina do Laboratório de Patologia Veterinária da Universidade Federal de Santa Maria (LPV-UFSM), neoplasmas representam a segunda causa de morte ou razão para eutanásia de cães da Mesorregião do Centro Ocidental Rio-Grandense, atrás apenas das doenças infecciosas, perfazendo 7,8% dos casos (Fighera et al. 2008Fighera R.A., Souza T.M., Silva M.C., Brum J.S., Graça D.L., Kommers G.D., Irigoyen L.F. & Barros C.S.L. 2008. Causas de morte e razões para eutanásia de cães. Pesq. Vet. Bras. 28(4):223-230. http://dx.doi.org/10.1590/S0100-736X2008000400005.
https://doi.org/10.1590/S0100-736X200800...
). A maior parte dos neoplasmas primários do SNC de cães da rotina de diagnóstico do LPV-UFSM são meningiomas (44,4%) (Fighera et al. 2008Fighera R.A., Souza T.M., Silva M.C., Brum J.S., Graça D.L., Kommers G.D., Irigoyen L.F. & Barros C.S.L. 2008. Causas de morte e razões para eutanásia de cães. Pesq. Vet. Bras. 28(4):223-230. http://dx.doi.org/10.1590/S0100-736X2008000400005.
https://doi.org/10.1590/S0100-736X200800...
). Em contraste com estudos europeus, em que os gliomas são os mais prevalentes em cães (Summers et al. 1995Summers B.A., Cummings J.F. & De Lahunta A. 1995. Tumors of the central nervous system, p.351-401. In: Summers B.A., Cummings J.F. & De Lahunta A. (Eds), Veterinary Neuropathology. Mosby, Missouri., Koestner & Higgins 2002Koestner A. & Higgins R. 2002. Tumors of the nervous system, p.697-738. In: Meuten D.J. (Ed.), Tumors in Domestic Animals. 4th ed. Iowa State Press, Iowa. 788p.). Meningioma é um neoplasma do sistema nervoso central (SNC) que se origina das células meningoteliais das leptomeninges, que na maioria são considerados benignos do ponto de vista histológico, mas pelo crescimento dentro do espaço intracraniano e subdural, geram consequências malignas do ponto de vista biológico (Costa 2009Costa R.C. 2009. Neoplasias do sistema nervoso, p.412-427. In: Daleck R.C., De Nardi A.B. & Rodaski S. (Eds), Oncologia em Cães e Gatos. Roca, São Paulo. 612p.). Nos Estados Unidos é o tumor primário do SNC mais comum em cães (40% dos tumores primários) (Snyder et al. 2006Snyder J.M., Shofer F.S., Van Winkle T.J. & Massicotte C. 2006. Canine intracranial primary neoplasia: 173 cases (1986-2003). J. Vet. Intern. Med. 20(3):669-675. PMid:16734106., Vandevelde et al. 2012Vandevelde R., Higgins R.J. & Oevermannn A. 2012. Neoplasia. p.129-156. In: Vandevelde R., Higgins R.J. & Oevermannn A. (Eds), Veterinary neuropathology essentials of theory and practice. Wiley-Blackwell, West Sussex. 212p.) e gatos (Troxel et al. 2004Troxel M.T., Vite C.H., Massicotte C., McLear R.C., Winkle T.J.V., Glass E.N., Tiches D. & Dayrell-Hart B. 2004. Magnetic resonance imaging features of feline intracranial neoplasia: retrospective analysis of 46 cats. J. Vet. Intern. Med. 18(2):176-189. http://dx.doi.org/10.1111/j.1939-1676.2004.tb00158.x. PMid:15058768.
https://doi.org/10.1111/j.1939-1676.2004...
), e são relatados esporadicamente em cavalos (Kreeger et al. 2002Kreeger J.M., Templer A., Tumquist S.E., Bailey K.L., Johnson P.J. & Wilson D.A. 2002. Paranasal meningioma in a horse. J. Vet. Diagn. Invest. 14(4):322-325. http://dx.doi.org/10.1177/104063870201400408. PMid:12152812.
https://doi.org/10.1177/1040638702014004...
), bovinos (Josephson & Little 1990Josephson G.K.A. & Little P.B. 1990. Four bovine meningeal tumors. Can. Vet. J. 31(10):700-703. PMid:17423678.) e ovinos (Koestner & Higgins 2002Koestner A. & Higgins R. 2002. Tumors of the nervous system, p.697-738. In: Meuten D.J. (Ed.), Tumors in Domestic Animals. 4th ed. Iowa State Press, Iowa. 788p., Vandevelde et al. 2012Vandevelde R., Higgins R.J. & Oevermannn A. 2012. Neoplasia. p.129-156. In: Vandevelde R., Higgins R.J. & Oevermannn A. (Eds), Veterinary neuropathology essentials of theory and practice. Wiley-Blackwell, West Sussex. 212p.).
Meningiomas em humanos e animais domésticos são histologicamente variados e podem sofrer diferenciação epitelial ou mesenquimal (Summers et al. 1995Summers B.A., Cummings J.F. & De Lahunta A. 1995. Tumors of the central nervous system, p.351-401. In: Summers B.A., Cummings J.F. & De Lahunta A. (Eds), Veterinary Neuropathology. Mosby, Missouri., Koestner & Higgins 2002Koestner A. & Higgins R. 2002. Tumors of the nervous system, p.697-738. In: Meuten D.J. (Ed.), Tumors in Domestic Animals. 4th ed. Iowa State Press, Iowa. 788p.). Essa variedade histológica é reflexo da contribuição do mesoderma e da crista neural para a sua formação (Koestner & Higgins 2002Koestner A. & Higgins R. 2002. Tumors of the nervous system, p.697-738. In: Meuten D.J. (Ed.), Tumors in Domestic Animals. 4th ed. Iowa State Press, Iowa. 788p.). Não há predisposição sexual em cães (Patnaik et al. 1986Patnaik A.K., Kay W.J. & Hurvitz A.I. 1986. Intracranial meningioma: a comparative pathologic study of 28 dogs. Vet. Pathol. 23(4):369-373. http://dx.doi.org/10.1177/030098588602300404. PMid:3750730.
https://doi.org/10.1177/0300985886023004...
), entretanto, mulheres apresentam maior incidência de meningiomas (Koestner & Higgins 2002Koestner A. & Higgins R. 2002. Tumors of the nervous system, p.697-738. In: Meuten D.J. (Ed.), Tumors in Domestic Animals. 4th ed. Iowa State Press, Iowa. 788p., Montoliu et al. 2006Montoliu P., Anor S., Vidal E. & Pumarola M. 2006. Histological and immunohistochemical study of 30 cases of canine meningioma. J. Comp. Pathol. 135(4):200-207. http://dx.doi.org/10.1016/j.jcpa.2006.06.006. PMid:17049358.
https://doi.org/10.1016/j.jcpa.2006.06.0...
).
Pela classificação da Organização Mundial da Saúde (OMS) de 1999 (Koestner et al. 1999Koestner A., Bilzer T., Fatzer R., Schulmer F.Y.S., Summer B.A. & Van Winkle T.J. 1999. Histological classification of the tumors of the nervous system of domestic animals. p.25-26. In: Koestner A., Bilzer T., Fatzer R., Schulmer F.Y.S., Summer B.A. & Van Winkle T.J. (Eds), International Histological Classification of the Tumors of Domestic Animals. 2nd Series, Vol.5. Armed Forces Institute of Pathology, Washington, D.C.) dos tumores do SNC de animais domésticos, os meningiomas de cães são dividos histologicamente em dois grupos principais: benignos, aqueles de crescimento lento de vários subtipos (meningotelial, fibroblástico, transicional, psamomatoso, angiomatoso, papilar, de células granulares e mixoide) e anaplásicos (malignos) (Koestner et al. 1999Koestner A., Bilzer T., Fatzer R., Schulmer F.Y.S., Summer B.A. & Van Winkle T.J. 1999. Histological classification of the tumors of the nervous system of domestic animals. p.25-26. In: Koestner A., Bilzer T., Fatzer R., Schulmer F.Y.S., Summer B.A. & Van Winkle T.J. (Eds), International Histological Classification of the Tumors of Domestic Animals. 2nd Series, Vol.5. Armed Forces Institute of Pathology, Washington, D.C.). O subtipo microcístico foi posteriormente identificado de forma independente (Montoliu et al. 2006Montoliu P., Anor S., Vidal E. & Pumarola M. 2006. Histological and immunohistochemical study of 30 cases of canine meningioma. J. Comp. Pathol. 135(4):200-207. http://dx.doi.org/10.1016/j.jcpa.2006.06.006. PMid:17049358.
https://doi.org/10.1016/j.jcpa.2006.06.0...
).
Não há dados disponíveis na literatura correlacionando o comportamento biológico e a evolução clínica com o sistema de classificação da OMS de 1999 (Koestner et al. 1999Koestner A., Bilzer T., Fatzer R., Schulmer F.Y.S., Summer B.A. & Van Winkle T.J. 1999. Histological classification of the tumors of the nervous system of domestic animals. p.25-26. In: Koestner A., Bilzer T., Fatzer R., Schulmer F.Y.S., Summer B.A. & Van Winkle T.J. (Eds), International Histological Classification of the Tumors of Domestic Animals. 2nd Series, Vol.5. Armed Forces Institute of Pathology, Washington, D.C.) para meningiomas em cães. Em humanos, um sistema de classificação mais detalhado permite a correlação consistente dos achados histológicos com o comportamento biológico dos meningiomas (Sturges et al. 2008Sturges B.K., Dickinson P.J., Bollen P.D., Koblik P.H., Kass G.D., Kortz K.M., Vernau M.F., Knipe R.A., Lecouteur R.A. & Higgins R.J. 2008. Magnetic resonance imaging and histological classification of intracranial meningiomas in 112 dogs. J. Vet. Intern. Med. 22(3):586-595. http://dx.doi.org/10.1111/j.1939-1676.2008.00042.x. PMid:18466258.
https://doi.org/10.1111/j.1939-1676.2008...
). Um componente importante deste sistema de classificação é o agrupamento dos meningiomas em três graus histológicos, Grau I (benigno), Grau II (atípico) e Grau III (maligno ou anaplásico), que é fundamental para prever o comportamento clínico e a evolução clínica nos humanos (Louis et al. 2007Louis D.N., Ohgaki H., Wiestler O.D., Cavenee W.K., Burger P.C., Jouvet A., Scheithauer B.W. & Kleihues P. 2007. The WHO classification of tumours of the central nervous system. Acta Neuropathol. 114(2):97-109. http://dx.doi.org/10.1007/s00401-007-0243-4. PMid:17618441.
https://doi.org/10.1007/s00401-007-0243-...
).
A partir de 2008, vários autores (Petersen et al. 2008Petersen S.A., Sturges B.K., Dickinson P.J., Pollard R.E., Kass P.H., Kent M., Vernau K.M., Lecouteur R.A. & Higgins R.J. 2008. Canine intraspinal meningiomas: imaging features, histopathologic classification, and long-term outcome in 34 dogs. J. Vet. Intern. Med. 22(4):946-953. http://dx.doi.org/10.1111/j.1939-1676.2008.0106.x. PMid:18482277.
https://doi.org/10.1111/j.1939-1676.2008...
, Sturges et al. 2008Sturges B.K., Dickinson P.J., Bollen P.D., Koblik P.H., Kass G.D., Kortz K.M., Vernau M.F., Knipe R.A., Lecouteur R.A. & Higgins R.J. 2008. Magnetic resonance imaging and histological classification of intracranial meningiomas in 112 dogs. J. Vet. Intern. Med. 22(3):586-595. http://dx.doi.org/10.1111/j.1939-1676.2008.00042.x. PMid:18466258.
https://doi.org/10.1111/j.1939-1676.2008...
, Vandevelde et al. 2012Vandevelde R., Higgins R.J. & Oevermannn A. 2012. Neoplasia. p.129-156. In: Vandevelde R., Higgins R.J. & Oevermannn A. (Eds), Veterinary neuropathology essentials of theory and practice. Wiley-Blackwell, West Sussex. 212p., Cantile & Youssef 2016Cantile C. & Youssef S. 2016. Nervous system, p.251-406. In: Maxie M.G. (Ed.), Jubb, Kennedy and Palmer’s Pathology of Domestic Animals. Vol.1. 6th ed. Saunders Elsevier, Philadelphia. 797p. http://dx.doi.org/10.1016/B978-0-7020-5317-7.00004-7.
https://doi.org/10.1016/B978-0-7020-5317...
) passaram a classificar os meningiomas de cães através do sistema de graduação adaptado daquele utilizado para humanos pela OMS de 2007 (Louis et al. 2007Louis D.N., Ohgaki H., Wiestler O.D., Cavenee W.K., Burger P.C., Jouvet A., Scheithauer B.W. & Kleihues P. 2007. The WHO classification of tumours of the central nervous system. Acta Neuropathol. 114(2):97-109. http://dx.doi.org/10.1007/s00401-007-0243-4. PMid:17618441.
https://doi.org/10.1007/s00401-007-0243-...
). Pelo fato de meningiomas caninos serem histologicamente muito semelhantes aos seus homólogos de humanos, indicadores preditivos e prognósticos clínicos utilizados em pessoas podem ser valiosos no tratamento de cães com meningiomas (Sturges et al. 2008Sturges B.K., Dickinson P.J., Bollen P.D., Koblik P.H., Kass G.D., Kortz K.M., Vernau M.F., Knipe R.A., Lecouteur R.A. & Higgins R.J. 2008. Magnetic resonance imaging and histological classification of intracranial meningiomas in 112 dogs. J. Vet. Intern. Med. 22(3):586-595. http://dx.doi.org/10.1111/j.1939-1676.2008.00042.x. PMid:18466258.
https://doi.org/10.1111/j.1939-1676.2008...
).
Na rotina diagnóstica busca-se adotar esquemas de classificação de tumores que permitam uma boa correlação entre a classificação histológica e o prognóstico, melhorando a sua aplicabilidade prática. Como no Brasil a terapia oncológica em geral para cães tem ampliado sua utilização, há cada vez mais uma demanda para o tratamento de meningiomas, baseado em seu comportamento biológico.
Com base nessa problemática, este estudo retrospectivo teve como objetivo principal classificar e graduar 22 meningiomas diagnosticados em cães necropsiados ao longo de aproximadamente 18 anos no LPV-UFSM através do sistema de graduação histológica proposto na literatura internacional para cães (Petersen et al. 2008Petersen S.A., Sturges B.K., Dickinson P.J., Pollard R.E., Kass P.H., Kent M., Vernau K.M., Lecouteur R.A. & Higgins R.J. 2008. Canine intraspinal meningiomas: imaging features, histopathologic classification, and long-term outcome in 34 dogs. J. Vet. Intern. Med. 22(4):946-953. http://dx.doi.org/10.1111/j.1939-1676.2008.0106.x. PMid:18482277.
https://doi.org/10.1111/j.1939-1676.2008...
, Sturges et al. 2008Sturges B.K., Dickinson P.J., Bollen P.D., Koblik P.H., Kass G.D., Kortz K.M., Vernau M.F., Knipe R.A., Lecouteur R.A. & Higgins R.J. 2008. Magnetic resonance imaging and histological classification of intracranial meningiomas in 112 dogs. J. Vet. Intern. Med. 22(3):586-595. http://dx.doi.org/10.1111/j.1939-1676.2008.00042.x. PMid:18466258.
https://doi.org/10.1111/j.1939-1676.2008...
, Vandevelde et al. 2012Vandevelde R., Higgins R.J. & Oevermannn A. 2012. Neoplasia. p.129-156. In: Vandevelde R., Higgins R.J. & Oevermannn A. (Eds), Veterinary neuropathology essentials of theory and practice. Wiley-Blackwell, West Sussex. 212p., Cantile & Youssef 2016Cantile C. & Youssef S. 2016. Nervous system, p.251-406. In: Maxie M.G. (Ed.), Jubb, Kennedy and Palmer’s Pathology of Domestic Animals. Vol.1. 6th ed. Saunders Elsevier, Philadelphia. 797p. http://dx.doi.org/10.1016/B978-0-7020-5317-7.00004-7.
https://doi.org/10.1016/B978-0-7020-5317...
), adaptado do utilizado para humanos pela OMS de 2007 (Louis et al. 2007Louis D.N., Ohgaki H., Wiestler O.D., Cavenee W.K., Burger P.C., Jouvet A., Scheithauer B.W. & Kleihues P. 2007. The WHO classification of tumours of the central nervous system. Acta Neuropathol. 114(2):97-109. http://dx.doi.org/10.1007/s00401-007-0243-4. PMid:17618441.
https://doi.org/10.1007/s00401-007-0243-...
). Os resultados serão computados e relacionados aos aspectos epidemiológicos, clínicos e anatomopatológicos. Os dados obtidos serão comparados ao que é descrito na literatura para meningiomas de cães e humanos, a fim de fornecer subsídios para clínicos e patologistas veterinários no que se refere a esse neoplasma.
Material e Métodos
Os casos de meningiomas diagnosticados em cães no LPV-UFSM, entre janeiro de 1999 e abril de 2016 (18 anos e 13 meses) foram revisados. Este estudo foi dividido em quatro etapas: (1) separação e análise dos protocolos de necropsia, (2) catalogação dos dados, (3) reavaliação histológica e (4) graduação histológica de acordo com Petersen et al. (2008)Petersen S.A., Sturges B.K., Dickinson P.J., Pollard R.E., Kass P.H., Kent M., Vernau K.M., Lecouteur R.A. & Higgins R.J. 2008. Canine intraspinal meningiomas: imaging features, histopathologic classification, and long-term outcome in 34 dogs. J. Vet. Intern. Med. 22(4):946-953. http://dx.doi.org/10.1111/j.1939-1676.2008.0106.x. PMid:18482277.
https://doi.org/10.1111/j.1939-1676.2008...
, Sturges et al. (2008)Sturges B.K., Dickinson P.J., Bollen P.D., Koblik P.H., Kass G.D., Kortz K.M., Vernau M.F., Knipe R.A., Lecouteur R.A. & Higgins R.J. 2008. Magnetic resonance imaging and histological classification of intracranial meningiomas in 112 dogs. J. Vet. Intern. Med. 22(3):586-595. http://dx.doi.org/10.1111/j.1939-1676.2008.00042.x. PMid:18466258.
https://doi.org/10.1111/j.1939-1676.2008...
, Vandevelde et al. (2012)Vandevelde R., Higgins R.J. & Oevermannn A. 2012. Neoplasia. p.129-156. In: Vandevelde R., Higgins R.J. & Oevermannn A. (Eds), Veterinary neuropathology essentials of theory and practice. Wiley-Blackwell, West Sussex. 212p. e Cantile & Youssef (2016)Cantile C. & Youssef S. 2016. Nervous system, p.251-406. In: Maxie M.G. (Ed.), Jubb, Kennedy and Palmer’s Pathology of Domestic Animals. Vol.1. 6th ed. Saunders Elsevier, Philadelphia. 797p. http://dx.doi.org/10.1016/B978-0-7020-5317-7.00004-7.
https://doi.org/10.1016/B978-0-7020-5317...
. Dos protocolos de necropsia foram retiradas informações referentes ao sexo e ao status reprodutivo (se eram castrados ou não), idade, raça (com ou sem raça definida [SRD] e conformação do crânio [dolicocefálicos, braquicefálicos ou mesocefálicos]), sinais clínicos, evolução clínica (após o início dos sinais clínicos), ocorrência de tratamento clínico, localização anatômica, achados macroscópicos e histológicos.
Os meningiomas foram descritos de acordo com sua localização anatômica intracraniana como das regiões: olfatória, convexidade do cérebro, parasselar, parassagital, falcino, tentorial e do ângulo ponto-cerebelar, de acordo com Sturges et al. (2008)Sturges B.K., Dickinson P.J., Bollen P.D., Koblik P.H., Kass G.D., Kortz K.M., Vernau M.F., Knipe R.A., Lecouteur R.A. & Higgins R.J. 2008. Magnetic resonance imaging and histological classification of intracranial meningiomas in 112 dogs. J. Vet. Intern. Med. 22(3):586-595. http://dx.doi.org/10.1111/j.1939-1676.2008.00042.x. PMid:18466258.
https://doi.org/10.1111/j.1939-1676.2008...
. A origem do tumor (OT) para cada região foi: região olfatória (OT: lâmina crivosa, osso pré-esfenoide, crânio ventral se estendendo ao osso frontal), parasselar (OT: osso basoesfenoide, fossa hipofisiária, tubérculo selar, seio cavernoso), parassagital (OT: ângulo parassagital [o espaço formado pela convexidade da dura-máter e a parede lateral da foice cerebral]), falcino (OT: foice cerebral [tumores completamente escondidos pelo córtex cerebral sobreposto]), convexidade do cérebro (OT: convexidade cerebral frontal, parietal, occipital e temporal), tentorial (OT: região do osso tentório), ângulo ponto-cerebelar. Na medula espinhal, os meningiomas foram descritos de acordo com sua localização anatômica em segmentos C1-C5, C6-T1 e T2-T5 (Petersen et al. 2008Petersen S.A., Sturges B.K., Dickinson P.J., Pollard R.E., Kass P.H., Kent M., Vernau K.M., Lecouteur R.A. & Higgins R.J. 2008. Canine intraspinal meningiomas: imaging features, histopathologic classification, and long-term outcome in 34 dogs. J. Vet. Intern. Med. 22(4):946-953. http://dx.doi.org/10.1111/j.1939-1676.2008.0106.x. PMid:18482277.
https://doi.org/10.1111/j.1939-1676.2008...
).
Os sinais clínicos foram agrupados conforme as manifestações clínicas neurológicas, de acordo com Costa (2009)Costa R.C. 2009. Neoplasias do sistema nervoso, p.412-427. In: Daleck R.C., De Nardi A.B. & Rodaski S. (Eds), Oncologia em Cães e Gatos. Roca, São Paulo. 612p., e incluíram: alterações tálamo-corticais, vestibulares centrais e medulares. Os achados histológicos reavaliados em cada caso incluíram: (1) arranjo celular, (2) padrão estromal (escasso ou abundante), (3) índice mitótico, (4) atipia nuclear, (5) presença de células pequenas, (6) pleomorfismo celular, (7) invasão vascular e/ou do parênquima adjacente, (8) necrose, hemorragia e inflamação em meio ao tumor e (9) alterações no tecido nervoso adjacente ao tumor. De forma geral, esses aspectos histológicos fazem parte das características contempladas na descrição de meningiomas (Petersen et al. 2008Petersen S.A., Sturges B.K., Dickinson P.J., Pollard R.E., Kass P.H., Kent M., Vernau K.M., Lecouteur R.A. & Higgins R.J. 2008. Canine intraspinal meningiomas: imaging features, histopathologic classification, and long-term outcome in 34 dogs. J. Vet. Intern. Med. 22(4):946-953. http://dx.doi.org/10.1111/j.1939-1676.2008.0106.x. PMid:18482277.
https://doi.org/10.1111/j.1939-1676.2008...
, Sturges et al. 2008Sturges B.K., Dickinson P.J., Bollen P.D., Koblik P.H., Kass G.D., Kortz K.M., Vernau M.F., Knipe R.A., Lecouteur R.A. & Higgins R.J. 2008. Magnetic resonance imaging and histological classification of intracranial meningiomas in 112 dogs. J. Vet. Intern. Med. 22(3):586-595. http://dx.doi.org/10.1111/j.1939-1676.2008.00042.x. PMid:18466258.
https://doi.org/10.1111/j.1939-1676.2008...
, Vandevelde et al. 2012Vandevelde R., Higgins R.J. & Oevermannn A. 2012. Neoplasia. p.129-156. In: Vandevelde R., Higgins R.J. & Oevermannn A. (Eds), Veterinary neuropathology essentials of theory and practice. Wiley-Blackwell, West Sussex. 212p., Cantile & Youssef 2016Cantile C. & Youssef S. 2016. Nervous system, p.251-406. In: Maxie M.G. (Ed.), Jubb, Kennedy and Palmer’s Pathology of Domestic Animals. Vol.1. 6th ed. Saunders Elsevier, Philadelphia. 797p. http://dx.doi.org/10.1016/B978-0-7020-5317-7.00004-7.
https://doi.org/10.1016/B978-0-7020-5317...
). Os meningiomas foram graduados histologicamente e classificados em subtipos de acordo com os critérios da OMS de 2007 para meningiomas em humanos (Louis et al. 2007Louis D.N., Ohgaki H., Wiestler O.D., Cavenee W.K., Burger P.C., Jouvet A., Scheithauer B.W. & Kleihues P. 2007. The WHO classification of tumours of the central nervous system. Acta Neuropathol. 114(2):97-109. http://dx.doi.org/10.1007/s00401-007-0243-4. PMid:17618441.
https://doi.org/10.1007/s00401-007-0243-...
), adaptados às características histológicas de meningiomas em cães (Petersen et al. 2008Petersen S.A., Sturges B.K., Dickinson P.J., Pollard R.E., Kass P.H., Kent M., Vernau K.M., Lecouteur R.A. & Higgins R.J. 2008. Canine intraspinal meningiomas: imaging features, histopathologic classification, and long-term outcome in 34 dogs. J. Vet. Intern. Med. 22(4):946-953. http://dx.doi.org/10.1111/j.1939-1676.2008.0106.x. PMid:18482277.
https://doi.org/10.1111/j.1939-1676.2008...
, Sturges et al. 2008Sturges B.K., Dickinson P.J., Bollen P.D., Koblik P.H., Kass G.D., Kortz K.M., Vernau M.F., Knipe R.A., Lecouteur R.A. & Higgins R.J. 2008. Magnetic resonance imaging and histological classification of intracranial meningiomas in 112 dogs. J. Vet. Intern. Med. 22(3):586-595. http://dx.doi.org/10.1111/j.1939-1676.2008.00042.x. PMid:18466258.
https://doi.org/10.1111/j.1939-1676.2008...
, Vandevelde et al. 2012Vandevelde R., Higgins R.J. & Oevermannn A. 2012. Neoplasia. p.129-156. In: Vandevelde R., Higgins R.J. & Oevermannn A. (Eds), Veterinary neuropathology essentials of theory and practice. Wiley-Blackwell, West Sussex. 212p., Cantile & Youssef 2016Cantile C. & Youssef S. 2016. Nervous system, p.251-406. In: Maxie M.G. (Ed.), Jubb, Kennedy and Palmer’s Pathology of Domestic Animals. Vol.1. 6th ed. Saunders Elsevier, Philadelphia. 797p. http://dx.doi.org/10.1016/B978-0-7020-5317-7.00004-7.
https://doi.org/10.1016/B978-0-7020-5317...
). A graduação compreendeu: Grau I (G-I, benignos), Grau II (G-II, atípicos) e Grau III (G-III, maligno ou anaplásico). Os meningiomas de G-I foram classificados nos subtipos histológicos meningotelial, transicional, microcístico, fibroblástico e psamomatoso. Os meningiomas de G-II foram classificados nos subtipos atípico e cordoide. Os G-III foram classificados nos subtipos papilar e maligno.
Resultados
Os resultados referentes aos aspectos clínico-epidemiológicos, achados de necropsia e achados histopatológicos serão apresentados baseados nos graus histológicos, sendo que os meningiomas foram classificados em: G-I (14 casos), G-II (3 casos) e G-III (5 casos).
Achados clínico-epidemiológicos
Entre janeiro de 1999 e abril de 2016 foram realizadas 4.893 necropsias de cães no LPV-UFSM. Nesse período, 22 cães (0,4%) foram diagnosticados com meningioma. Desses, 16 eram fêmeas (72,7%; 2/16 castradas) e seis eram machos (27,3%; 1/6 castrado), com idades que variaram entre 5 e 15 anos. A média de idade foi de 11 anos para cães com meningioma GI, 12 anos para os com G-II e 8 anos para os com G-III. Quanto à raça, 16 (72,7%) eram de raça e 6 (27,3%) eram SRD. As raças incluíram: Boxer (7/16; 43,7%), Pastor Alemão (4/16; 25%), Rottweiler (3/16; 18,7%), Dachshund (1/16; 6,2%) e Poodle (1/16; 6,2%). Quanto à conformação do crânio dos cães de raça, 7/16 eram braquicéfalos, 5/16 eram dolicocéfalos e 4/16 eram mesocéfalos. As informações detalhadas de cada caso estão no Quadro 1.
Quanto ao quadro clínico, baseado na localização, 65% dos casos (13/20) manifestaram sinais de alterações tálamo-corticais, 20% (4/20) de alterações vestibulares centrais e 15% (3/20) de alterações medulares (Quadros 1 e 2). Em dois casos não havia informações sobre o quadro clínico. Quanto ao tratamento, em 12 casos (8 de G-I, 2 de G-II e 2 de G-III) havia informação de os cães terem sido tratados. Esses tratamentos incluíam a utilização de corticoides e anticonvulsivantes.
Com relação ao desfecho clínico, 12/22 cães foram submetidos à eutanásia e em 9/22 a morte foi espontânea. Em um caso, não havia informação. Independentemente do desfecho, a evolução clínica variou de poucos dias até 1 ano para os cães com meningiomas de G-I, de 7 a 20 dias para os de G-II e de 30 a 90 dias para os de G-III (Quadro 1).
Achados de necropsia
Com relação à localização, 4/22 foram na região olfatória, 4/22 na região parassagital, 3/22 na convexidade do cérebro, 3/22 na região parasselar, 2/22 foram tentoriais, 2/22 no ângulo ponto-cerebelar, 1/22 no falcino e 3/22 na medula espinal.
Os meningiomas G-I se apresentaram como intracranianos em 12/14 casos, sendo de localização parassagital em 4/12, olfatória em 3/12 (2/3 estendiam-se para os seios paranasais), na convexidade do cérebro em 2/12, parasselar em 1/12 (afetando o nervo óptico), falcino em 1/12 e tentorial (1/12). Os intraespinhais foram 2/14 e vistos na medula espinhal C6-T1 e T2. Os G-I se apresentaram principalmente na forma de massa (12/14) e em placa (2/14). Os meningiomas em forma de massa variaram entre 0,3 x 0,6 x 0,7cm a 4,0 x 2,0 x 2,0cm. Eram branco-acinzentados (11/12) ou avermelhados (1/12), macios (4/12) ou firmes (8/12) e alguns tinham áreas císticas (2/12). Aqueles descritos como placas (2/14) mediram entre 1,0 e 1,5cm em seu maior eixo, e tinham localização parasselar (1/2; afetando o nervo óptico) ou parassagital (1/2). Eram branco-acinzentados (1/2), avermelhados (1/2) e firmes (2/2).
Todos os meningiomas G-II foram descritos como massas (3/3) tinham entre 2,5x2x1cm e 3x2x1,5cm; eram brancacentos ou acinzentados (2/3) ou avermelhados (1/3) e macios (3/3). Eram intracranianos (vistos no ângulo ponto-cerebelar (1/3) e região parasselar (1/3) ou intraespinhais (vistos na medula espinhal C1-C2 [1/3]).
Os meningiomas G-III foram vistos na forma de massas (4/5) e placas (1/5). Os meningiomas em forma de massa variaram entre 1x1,5x0,5cm a 4x2x0,5cm e todos eram intracranianos, com localização olfatória (1/4), parasselar (1/4), tentorial (1/4) e no ângulo ponto-cerebelar (1/4); eram branco-acinzentados (4/5), avermelhados (1/5) e macios. Um caso foi descrito como placa (com 1,5cm no seu maior eixo); era branco-acinzentado e macio.
Achados histopatológicos
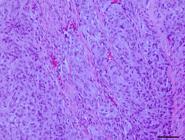
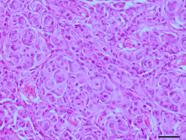
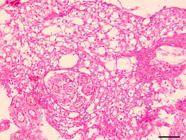
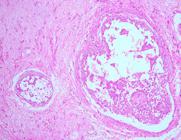
Como informado anteriormente, quanto às características histológicas, os meningiomas foram classificados em: G-I (14 casos), G-II (3 casos) e G-III (5 casos), conforme o Quadro 1. Os subtipos histológicos incluídos como G-I (14/22) foram: psamomatoso (5/14) (Fig.1), meningotelial (3/14) (Fig.2), transicional (3/14) (Fig.3), microcístico (2/14) (Fig.4) e fibroblástico (1/14) (Fig.5). O subtipo psamomatoso foi identificado pelo predomínio de estruturas espirais, com o centro hialino lamelar ou mineralizado, denominadas corpos de psamoma (psamomma bodies). O estroma era escasso (3/5) e moderado (2/5). O subtipo meningotelial caracterizou-se pelo predomínio de células neoplásicas arranjadas em lóbulos de diferentes tamanhos (padrão sincicial). Em todos os casos o estroma era escasso e havia algumas células neoplásicas com pseudoinclusões intranucleares. O subtipo fibroblástico foi caracterizado pelo predomínio de células neoplásicas arranjadas em feixes direcionados paralelamente ou entrelaçados, em meio a uma matriz rica em fibras colágenas. Algumas áreas apresentavam hialinização de fibras colágenas.
Meningioma meningotelial, grau I, com múltiplos lóbulos de células meningoteliais. HE, obj.20x.
Meningioma transicional, grau I, há múltiplos espirais de células neoplásicas fusiformes. HE, obj.40x.
Meningioma fibroblástico, grau I, caracterizado por feixes intercalantes de células fusiformes. HE, obj.20x.
O subtipo transicional foi caracterizado pela presença dos padrões meningotelial e fibroblástico em igual proporção, com frequentes redemoinhos (padrão misto). O estroma variou de moderado (2/3) a acentuado (1/3). Em dois casos, havia algumas pseudoinclusões intranucleares. O subtipo microcístico foi caracterizado pelo predomínio de células neoplásicas com formação de processos alongados e vacuolização citoplasmática e intersticial. O estroma era escasso nos dois casos.
Na maioria dos meningiomas G-I, pequenas áreas de proliferação de células neoplásicas com características de outros padrões foram observadas. Assim, em dois casos (2/14) havia áreas de padrão microcístico (casos 4 e 10). Foram observados três casos com (3/14) áreas de padrão psamomatoso (casos 8, 10 e 11). Umas poucas áreas do subtipo fibroblástico (caso 10). No caso 9 se observaram algumas áreas do padrão papilar.
Nos meningiomas de G-I, atipia e pleomorfismo foram moderados em um caso (1/14). Em 5/14 casos (transicional - 2 casos, cães 9 e 10; meningotelial - 2 casos, cães 6 e 8; psamomatoso - 1 caso, cão 3) havia invasão local de ilhas sólidas de células neoplásicas no tecido nervoso peritumoral. Outros achados incluíram: necrose (7/14), proliferação vascular peritumoral (4/14), edema peritumoral (4/14), hemorragia (2/14), degeneração walleriana medular espinhal (2/14), infiltrado inflamatório neutrofílico (1/14) e linfocítico (1/14).
Dos 22 meningiomas, três foram classificados como G-II (atípicos), sendo dois do subtipo cordoide e um do subtipo atípico. O subtipo cordoide (2/3) (Fig.6) foi caracterizado pela presença de células epitelioides neoplásicas arranjadas em cordões (1/2) e trabéculas (1/2) imersos em uma matriz basofílica mucoide. O subtipo atípico (Fig.7) foi caracterizado principalmente por ter 14 mitoses/10 campos de grande aumento (cga; 400x) e por células neoplásicas arranjadas em manto ou espirais, com alta celularidade, pleomorfismo e atipia acentuadas, células pequenas e estroma escasso. Há pequenas áreas do subtipo meningotelial nos três casos (casos 15 a 17). Observou-se a invasão de grupos sólidos de células neoplásicas no parênquima da medula espinhal (caso 17). Necrose multifocal (2/3), hemorragia (2/3) e proliferação vascular peritumoral (1/3) foram observadas.
Meningioma cordoide, grau II, há cordões de células epitelioides imersos em uma matriz basofílica. HE, obj.40x.
Meningioma atípico, grau II, com característica hipercelularidade de células pequenas e com arranjo em manto. HE, obj.40x.
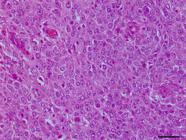
Dos 22 meningiomas, cinco foram classificados como malignos (G-III) e incluíram os subtipos papilar (4/5) e maligno (1/5). O subtipo papilar (Fig.8) foi identificado pela presença de células neoplásicas dispostas em camadas ao longo de eixos conjuntivo-vasculares, que lembram pseudo-rosetas perivasculares (pseudopapilíferas). Em um caso havia invasão vascular (Fig.9) na forma de grupos neoplásicos pseudopapilíferos. O subtipo maligno (Fig.10) foi caracterizado principalmente por ter 27 mitoses/10 cga e pela presença das células neoplásicas organizadas em lóbulos, alguns formando espirais, com alta celularidade, pleomorfismo e atipia nucleares acentuados e nucléolos proeminentes. O estroma era escasso. Em todos os casos de G-III foram observadas áreas de atipia e pleomorfismo celulares acentuados. Algumas áreas bem diferenciadas do padrão meningotelial foram observadas no caso 22. Foi observada invasão cerebral em 4/5 casos (cães 18 a 20 e 22). Necrose multifocal (3/5) ou coalescente (2/5), edema (2/5), hemorragia (1/5), proliferação vascular peritumoral (1/5) e infiltrado neutrofílico (1/5) foram também observados.
Meningioma papilar, grau III, êmbolos de células neoplásicas em vasos sanguíneos peritumorais. HE, obj.20x.
Meningioma maligno, grau III, células anaplásicas com numerosas figuras mitóticas. HE, obj.40x.
Discussão
A graduação dos meningiomas varia consideravelmente de acordo com sua aparência histológica e taxa mitótica (Vandevelde et al. 2012Vandevelde R., Higgins R.J. & Oevermannn A. 2012. Neoplasia. p.129-156. In: Vandevelde R., Higgins R.J. & Oevermannn A. (Eds), Veterinary neuropathology essentials of theory and practice. Wiley-Blackwell, West Sussex. 212p.). A aparência histológica é variada e depende principalmente da diferenciação epitelial ou mesenquimal e do arranjo do tumor (Summers et al. 1995Summers B.A., Cummings J.F. & De Lahunta A. 1995. Tumors of the central nervous system, p.351-401. In: Summers B.A., Cummings J.F. & De Lahunta A. (Eds), Veterinary Neuropathology. Mosby, Missouri.). Neste estudo, os meningiomas G-I perfizeram 63,6% dos casos, os G-II, 13,6% e os G-III, 22,7%. Isto diferiu da literatura internacional, em que a ordem decrescente de ocorrência geralmente é de G-I para G-III (Petersen et al. 2008Petersen S.A., Sturges B.K., Dickinson P.J., Pollard R.E., Kass P.H., Kent M., Vernau K.M., Lecouteur R.A. & Higgins R.J. 2008. Canine intraspinal meningiomas: imaging features, histopathologic classification, and long-term outcome in 34 dogs. J. Vet. Intern. Med. 22(4):946-953. http://dx.doi.org/10.1111/j.1939-1676.2008.0106.x. PMid:18482277.
https://doi.org/10.1111/j.1939-1676.2008...
, Sturges et al. 2008Sturges B.K., Dickinson P.J., Bollen P.D., Koblik P.H., Kass G.D., Kortz K.M., Vernau M.F., Knipe R.A., Lecouteur R.A. & Higgins R.J. 2008. Magnetic resonance imaging and histological classification of intracranial meningiomas in 112 dogs. J. Vet. Intern. Med. 22(3):586-595. http://dx.doi.org/10.1111/j.1939-1676.2008.00042.x. PMid:18466258.
https://doi.org/10.1111/j.1939-1676.2008...
). Não foi possível estabelecer possíveis causas para essa diferença.
Quanto aos G-I, outros estudos foram relativamente semelhantes na frequência de ocorrência, perfazendo 53% dos casos (Petersen et al. 2008Petersen S.A., Sturges B.K., Dickinson P.J., Pollard R.E., Kass P.H., Kent M., Vernau K.M., Lecouteur R.A. & Higgins R.J. 2008. Canine intraspinal meningiomas: imaging features, histopathologic classification, and long-term outcome in 34 dogs. J. Vet. Intern. Med. 22(4):946-953. http://dx.doi.org/10.1111/j.1939-1676.2008.0106.x. PMid:18482277.
https://doi.org/10.1111/j.1939-1676.2008...
) ou 56% (Sturges et al. 2008Sturges B.K., Dickinson P.J., Bollen P.D., Koblik P.H., Kass G.D., Kortz K.M., Vernau M.F., Knipe R.A., Lecouteur R.A. & Higgins R.J. 2008. Magnetic resonance imaging and histological classification of intracranial meningiomas in 112 dogs. J. Vet. Intern. Med. 22(3):586-595. http://dx.doi.org/10.1111/j.1939-1676.2008.00042.x. PMid:18466258.
https://doi.org/10.1111/j.1939-1676.2008...
). O subtipo psamomatoso foi o mais frequente (35,7%) dentre os G-I neste estudo, sendo considerado incomum (Montoliu et al. 2006Montoliu P., Anor S., Vidal E. & Pumarola M. 2006. Histological and immunohistochemical study of 30 cases of canine meningioma. J. Comp. Pathol. 135(4):200-207. http://dx.doi.org/10.1016/j.jcpa.2006.06.006. PMid:17049358.
https://doi.org/10.1016/j.jcpa.2006.06.0...
, Sturges et al. 2008Sturges B.K., Dickinson P.J., Bollen P.D., Koblik P.H., Kass G.D., Kortz K.M., Vernau M.F., Knipe R.A., Lecouteur R.A. & Higgins R.J. 2008. Magnetic resonance imaging and histological classification of intracranial meningiomas in 112 dogs. J. Vet. Intern. Med. 22(3):586-595. http://dx.doi.org/10.1111/j.1939-1676.2008.00042.x. PMid:18466258.
https://doi.org/10.1111/j.1939-1676.2008...
) ou nem relatado por outros autores (Patnaik et al. 1986Patnaik A.K., Kay W.J. & Hurvitz A.I. 1986. Intracranial meningioma: a comparative pathologic study of 28 dogs. Vet. Pathol. 23(4):369-373. http://dx.doi.org/10.1177/030098588602300404. PMid:3750730.
https://doi.org/10.1177/0300985886023004...
, Barnhart et al. 2002Barnhart K.F., Wojcieszyn J. & Storts R.W. 2002. Immunohistochemical staining patterns of canine meningiomas and correlation with published immunophenotypes. Vet. Pathol. 39(3):311-321. http://dx.doi.org/10.1354/vp.39-3-311. PMid:12014495.
https://doi.org/10.1354/vp.39-3-311...
, Petersen et al. 2008Petersen S.A., Sturges B.K., Dickinson P.J., Pollard R.E., Kass P.H., Kent M., Vernau K.M., Lecouteur R.A. & Higgins R.J. 2008. Canine intraspinal meningiomas: imaging features, histopathologic classification, and long-term outcome in 34 dogs. J. Vet. Intern. Med. 22(4):946-953. http://dx.doi.org/10.1111/j.1939-1676.2008.0106.x. PMid:18482277.
https://doi.org/10.1111/j.1939-1676.2008...
), sugerindo ser relativamente raro na literatura internacional. Na maioria dos estudos (Petersen et al. 2008Petersen S.A., Sturges B.K., Dickinson P.J., Pollard R.E., Kass P.H., Kent M., Vernau K.M., Lecouteur R.A. & Higgins R.J. 2008. Canine intraspinal meningiomas: imaging features, histopathologic classification, and long-term outcome in 34 dogs. J. Vet. Intern. Med. 22(4):946-953. http://dx.doi.org/10.1111/j.1939-1676.2008.0106.x. PMid:18482277.
https://doi.org/10.1111/j.1939-1676.2008...
, Sturges et al. 2008Sturges B.K., Dickinson P.J., Bollen P.D., Koblik P.H., Kass G.D., Kortz K.M., Vernau M.F., Knipe R.A., Lecouteur R.A. & Higgins R.J. 2008. Magnetic resonance imaging and histological classification of intracranial meningiomas in 112 dogs. J. Vet. Intern. Med. 22(3):586-595. http://dx.doi.org/10.1111/j.1939-1676.2008.00042.x. PMid:18466258.
https://doi.org/10.1111/j.1939-1676.2008...
, José-López et al. 2013José-López R., De la Fuente C., Pumarola M. & Anor S. 2013. Spinal meningiomas in dogs: description of 8 cases including a novel radiological and histopathological presentation. Can. Vet. J. 54(10):948-954. PMid:24155414.), os subtipos meningotelial e transicional são os mais comuns, sendo que neste trabalho cada um representou 21,4% dos G-I, ambos obtendo a segunda maior frequência nesse grau. O subtipo microcístico foi mencionado em livros textos referência em neuropatologia veterinária (Summers et al. 1995Summers B.A., Cummings J.F. & De Lahunta A. 1995. Tumors of the central nervous system, p.351-401. In: Summers B.A., Cummings J.F. & De Lahunta A. (Eds), Veterinary Neuropathology. Mosby, Missouri., Koestner & Higgins 2002Koestner A. & Higgins R. 2002. Tumors of the nervous system, p.697-738. In: Meuten D.J. (Ed.), Tumors in Domestic Animals. 4th ed. Iowa State Press, Iowa. 788p.), mas não foi contemplado na classificação da OMS de 1999 para animais domésticos (Koestner et al. 1999Koestner A., Bilzer T., Fatzer R., Schulmer F.Y.S., Summer B.A. & Van Winkle T.J. 1999. Histological classification of the tumors of the nervous system of domestic animals. p.25-26. In: Koestner A., Bilzer T., Fatzer R., Schulmer F.Y.S., Summer B.A. & Van Winkle T.J. (Eds), International Histological Classification of the Tumors of Domestic Animals. 2nd Series, Vol.5. Armed Forces Institute of Pathology, Washington, D.C.). Posteriormente, este subtipo foi abordado por Montoliu et al. (2006)Montoliu P., Anor S., Vidal E. & Pumarola M. 2006. Histological and immunohistochemical study of 30 cases of canine meningioma. J. Comp. Pathol. 135(4):200-207. http://dx.doi.org/10.1016/j.jcpa.2006.06.006. PMid:17049358.
https://doi.org/10.1016/j.jcpa.2006.06.0...
de forma independente. Foi diagnosticado um caso do subtipo fibroblástico (7,1%), sendo também reportado em outros estudos como incomum (Patnaik et al. 1986Patnaik A.K., Kay W.J. & Hurvitz A.I. 1986. Intracranial meningioma: a comparative pathologic study of 28 dogs. Vet. Pathol. 23(4):369-373. http://dx.doi.org/10.1177/030098588602300404. PMid:3750730.
https://doi.org/10.1177/0300985886023004...
, Barnhart et al. 2002Barnhart K.F., Wojcieszyn J. & Storts R.W. 2002. Immunohistochemical staining patterns of canine meningiomas and correlation with published immunophenotypes. Vet. Pathol. 39(3):311-321. http://dx.doi.org/10.1354/vp.39-3-311. PMid:12014495.
https://doi.org/10.1354/vp.39-3-311...
, Montoliu et al. 2006Montoliu P., Anor S., Vidal E. & Pumarola M. 2006. Histological and immunohistochemical study of 30 cases of canine meningioma. J. Comp. Pathol. 135(4):200-207. http://dx.doi.org/10.1016/j.jcpa.2006.06.006. PMid:17049358.
https://doi.org/10.1016/j.jcpa.2006.06.0...
).
Além disso, é comum se observar dois ou mais diferentes padrões morfológicos no mesmo tumor, por isso a classificação do subtipo histológico dos meningiomas é baseada no padrão predominante (Patnaik et al. 1986Patnaik A.K., Kay W.J. & Hurvitz A.I. 1986. Intracranial meningioma: a comparative pathologic study of 28 dogs. Vet. Pathol. 23(4):369-373. http://dx.doi.org/10.1177/030098588602300404. PMid:3750730.
https://doi.org/10.1177/0300985886023004...
, Summers et al. 1995Summers B.A., Cummings J.F. & De Lahunta A. 1995. Tumors of the central nervous system, p.351-401. In: Summers B.A., Cummings J.F. & De Lahunta A. (Eds), Veterinary Neuropathology. Mosby, Missouri.). Neste estudo, aproximadamente 28,5% tinham arranjo de dois subtipos, enquanto cerca de 7,1% tinham quatro subtipos no mesmo tumor. No caso 9, cujo padrão predominante era o transicional, observou-se aproximadamente 20% do tumor com padrão papilar. Por mais que o arranjo papilar seja de alto grau (G-III), segundo a OMS de 2007, este subtipo tem que representar mais de 50% do tumor para considerar-se nessa graduação (Mawrin & Perry 2010Mawrin C. & Perry A. 2010. Pathological classification and molecular genetics of meningiomas. J. Neurooncol. 99(3):379-391. http://dx.doi.org/10.1007/s11060-010-0342-2. PMid:20809251.
https://doi.org/10.1007/s11060-010-0342-...
, Lopes & Vandenberg 2013Lopes M.B.S. & Vandenberg S.R. 2013. Tumor of the central nervous system, p.1933-2031. In: Fletcher C.D.M. (Ed.), Diagnostic Histopathology of Tumors. Vol.2. 4th ed. Saunders Elsevier, Philadelphia. 2145p.). Nesses casos, alguns autores adicionam no diagnóstico de meningiomas humanos a variante (por exemplo, meningioma transicional com padrão papilar focal) (Mawrin & Perry 2010).
Algumas “peculiaridades” dos meningiomas classificados como G-I (benignos) merecem ser discutidas. Na metade dos casos observaram-se grandes áreas de necrose na região central do tumor. Em neoplasmas em geral, estas são atribuíveis à isquemia devido à perfusão inadequada através da vasculatura anormalmente permeável ou ao aumento da pressão no centro da massa, a qual restringe a perfusão de vasos de pequeno calibre (Cullen et al. 2002Cullen J.M., Page R. & Misdorp W. 2002. An overview of cancer, pathogenesis, diagnosis, and management, p.3-44. In: Meuten D.J. (Ed.), Tumors in Domestic Animals. 4th ed. Iowa State Press, Iowa. 788p. http://dx.doi.org/10.1002/9780470376928.ch1.
https://doi.org/10.1002/9780470376928.ch...
). Em um caso foram observadas áreas de atipia nuclear. Vale salientar que “atipias nucleares” não são confiáveis para determinar um grau mais elevado ao tumor (G-II, por exemplo), pois meningiomas G-I podem mostrar graus consideráveis de atipias nucleares “degenerativas”, semelhantes às observadas nos G-II subtipo atípico em humanos, em que a “atipia nuclear” não tem uma correspondência com um comportamento clínico subsequente (Mawrin & Perry 2010Mawrin C. & Perry A. 2010. Pathological classification and molecular genetics of meningiomas. J. Neurooncol. 99(3):379-391. http://dx.doi.org/10.1007/s11060-010-0342-2. PMid:20809251.
https://doi.org/10.1007/s11060-010-0342-...
).
A invasão do tecido nervoso, como observada neste estudo (35,7% dos G-I, 33,3% dos G-II e 80% dos G-III), já foi relatada em meningiomas G-I e G-II (atípicos) em cães (Sturges et al. 2008Sturges B.K., Dickinson P.J., Bollen P.D., Koblik P.H., Kass G.D., Kortz K.M., Vernau M.F., Knipe R.A., Lecouteur R.A. & Higgins R.J. 2008. Magnetic resonance imaging and histological classification of intracranial meningiomas in 112 dogs. J. Vet. Intern. Med. 22(3):586-595. http://dx.doi.org/10.1111/j.1939-1676.2008.00042.x. PMid:18466258.
https://doi.org/10.1111/j.1939-1676.2008...
). A questão da “invasão do tecido nervoso” observada em alguns meningiomas histologicamente classificados como benignos merece alguns esclarecimentos. Pela classificação dos meningiomas em humanos da OMS de 2007 (Louis et al. 2007Louis D.N., Ohgaki H., Wiestler O.D., Cavenee W.K., Burger P.C., Jouvet A., Scheithauer B.W. & Kleihues P. 2007. The WHO classification of tumours of the central nervous system. Acta Neuropathol. 114(2):97-109. http://dx.doi.org/10.1007/s00401-007-0243-4. PMid:17618441.
https://doi.org/10.1007/s00401-007-0243-...
), a invasão encefálica não está incluída entre os critérios histológicos para a classificação dos mengiomas grau II (atípicos), permitindo que meningiomas de grau I (benignos) possam apresentar essa característica, sem que isso altere sua graduação para graus mais elevados. Entretanto, em alguns estudos observou-se que a invasão cerebral em tumores grau I implicou estatisticamente em taxas de recidiva e mortalidade semelhantes às dos G-II. Portanto, para alguns autores, do ponto de vista prognóstico, meningiomas de humanos que invadem o cérebro, mesmo se histologicamente benignos (G-I), deveriam ser considerados como um G-II da OMS (Mawrin & Perry 2010Mawrin C. & Perry A. 2010. Pathological classification and molecular genetics of meningiomas. J. Neurooncol. 99(3):379-391. http://dx.doi.org/10.1007/s11060-010-0342-2. PMid:20809251.
https://doi.org/10.1007/s11060-010-0342-...
, Lopes & Vandenberg 2013Lopes M.B.S. & Vandenberg S.R. 2013. Tumor of the central nervous system, p.1933-2031. In: Fletcher C.D.M. (Ed.), Diagnostic Histopathology of Tumors. Vol.2. 4th ed. Saunders Elsevier, Philadelphia. 2145p.). Em um estudo publicado em 2014, verificou-se que a frequência de invasão do SNC peritumoral em humanos aumentou com o grau do meningioma, sendo de 28% para os G-I, 64% para G-II e 100% para G-III (Pizem et al. 2014Pizem J., Velnar T., Prestor B., Mlakar J. & Popovic M. 2014. Brain invasion assessability in meningiomas is related to meningioma size and grade, and can be improved by extensive sampling of the surgically removed meningioma specimen. Clin. Neuropathol. 33(5):354-363. http://dx.doi.org/10.5414/NP300750. PMid:25034703.
https://doi.org/10.5414/NP300750...
). Recentemente, um artigo resumindo as mudanças na nova classificação de meningiomas em humanos da OMS de 2016 (Louis et al. 2016Louis D.N., Perry A., Reifenberger G., von Deimling A., Figarella-Branger D., Cavenee W.K., Ohgaki H., Wiestler O.D., Kleihues P. & Ellison D.W. 2016. The 2016 world health organization classification of tumors of the central nervous system: a summary. Acta Neuropathol. 131(6):803-820. http://dx.doi.org/10.1007/s00401-016-1545-1. PMid:27157931.
https://doi.org/10.1007/s00401-016-1545-...
), mostra que a invasão cerebral passou a constar como critério de classificação de meningiomas atípicos (no G-II). Já tem sido sugerido incluir esse critério para atribuir um G-II em meningiomas de cães (Mandara et al. 2010Mandara M.T., Pavone S., Brunetti B. & Mandrioli L. 2010. A comparative study of canine and feline meningioma classification based on the WHO histological classification system in humans. Proc. 22nd Symposium ESVN-ECVN, Bologna, 24-26 September 2009. J. Vet. Intern. Med. 24:235-258.), porém isso ainda não foi adotado em medicina veterinária.
Os meningiomas G-II representaram 13,6%, em contraste com estudos em que sua frequência atingiu 43% (Sturges et al. 2008Sturges B.K., Dickinson P.J., Bollen P.D., Koblik P.H., Kass G.D., Kortz K.M., Vernau M.F., Knipe R.A., Lecouteur R.A. & Higgins R.J. 2008. Magnetic resonance imaging and histological classification of intracranial meningiomas in 112 dogs. J. Vet. Intern. Med. 22(3):586-595. http://dx.doi.org/10.1111/j.1939-1676.2008.00042.x. PMid:18466258.
https://doi.org/10.1111/j.1939-1676.2008...
) e 44% (Petersen et al. 2008Petersen S.A., Sturges B.K., Dickinson P.J., Pollard R.E., Kass P.H., Kent M., Vernau K.M., Lecouteur R.A. & Higgins R.J. 2008. Canine intraspinal meningiomas: imaging features, histopathologic classification, and long-term outcome in 34 dogs. J. Vet. Intern. Med. 22(4):946-953. http://dx.doi.org/10.1111/j.1939-1676.2008.0106.x. PMid:18482277.
https://doi.org/10.1111/j.1939-1676.2008...
). Não foi possível estabelecer possíveis razões para essa diferença na prevalência. Chamou a atenção a maior frequência do subtipo cordoide em relação ao atípico, o que foi incomum na literatura consultada (Sturges et al. 2008Sturges B.K., Dickinson P.J., Bollen P.D., Koblik P.H., Kass G.D., Kortz K.M., Vernau M.F., Knipe R.A., Lecouteur R.A. & Higgins R.J. 2008. Magnetic resonance imaging and histological classification of intracranial meningiomas in 112 dogs. J. Vet. Intern. Med. 22(3):586-595. http://dx.doi.org/10.1111/j.1939-1676.2008.00042.x. PMid:18466258.
https://doi.org/10.1111/j.1939-1676.2008...
, Petersen et al. 2008Petersen S.A., Sturges B.K., Dickinson P.J., Pollard R.E., Kass P.H., Kent M., Vernau K.M., Lecouteur R.A. & Higgins R.J. 2008. Canine intraspinal meningiomas: imaging features, histopathologic classification, and long-term outcome in 34 dogs. J. Vet. Intern. Med. 22(4):946-953. http://dx.doi.org/10.1111/j.1939-1676.2008.0106.x. PMid:18482277.
https://doi.org/10.1111/j.1939-1676.2008...
, Mandara et al. 2010Mandara M.T., Pavone S., Brunetti B. & Mandrioli L. 2010. A comparative study of canine and feline meningioma classification based on the WHO histological classification system in humans. Proc. 22nd Symposium ESVN-ECVN, Bologna, 24-26 September 2009. J. Vet. Intern. Med. 24:235-258.). À medida que os meningiomas se tornam menos diferenciados (G-II), passam a apresentar três ou mais dos seguintes critérios como: arranjo em manto, células pequenas, atipia, aumento da celularidade e áreas de necrose (Sturges et al. 2008Sturges B.K., Dickinson P.J., Bollen P.D., Koblik P.H., Kass G.D., Kortz K.M., Vernau M.F., Knipe R.A., Lecouteur R.A. & Higgins R.J. 2008. Magnetic resonance imaging and histological classification of intracranial meningiomas in 112 dogs. J. Vet. Intern. Med. 22(3):586-595. http://dx.doi.org/10.1111/j.1939-1676.2008.00042.x. PMid:18466258.
https://doi.org/10.1111/j.1939-1676.2008...
, Mawrin & Perry 2010Mawrin C. & Perry A. 2010. Pathological classification and molecular genetics of meningiomas. J. Neurooncol. 99(3):379-391. http://dx.doi.org/10.1007/s11060-010-0342-2. PMid:20809251.
https://doi.org/10.1007/s11060-010-0342-...
, Vandevelde et al. 2012Vandevelde R., Higgins R.J. & Oevermannn A. 2012. Neoplasia. p.129-156. In: Vandevelde R., Higgins R.J. & Oevermannn A. (Eds), Veterinary neuropathology essentials of theory and practice. Wiley-Blackwell, West Sussex. 212p.). No único caso do subtipo atípico, foram observados quatro de cinco critérios de morfologia, além do índice mitótico elevado (o critério é >4 a 19 mitoses/10cga). Em humanos, aproximadamente 75% dos meningiomas G-II são classificados em virtude de seu índice mitótico (Barresi et al. 2016Barresi V., Caffo M. & Tuccari G. 2016. Classification of human meningiomas: lights, shadows, and future perspectives. J. Neurosci. Res. 94(12):1604-1612. http://dx.doi.org/10.1002/jnr.23801. PMid:27376782.
https://doi.org/10.1002/jnr.23801...
).
Para o subtipo cordoide, os critérios morfológicos descritos acima para o G-II (subtipo atípico) não se aplicam, pois só o padrão já representa um pior prognóstico (Vandevelde et al. 2012Vandevelde R., Higgins R.J. & Oevermannn A. 2012. Neoplasia. p.129-156. In: Vandevelde R., Higgins R.J. & Oevermannn A. (Eds), Veterinary neuropathology essentials of theory and practice. Wiley-Blackwell, West Sussex. 212p.), tendo aqui uma baixa frequência (2/22), semelhante a um estudo anterior (Sturges et al. 2008Sturges B.K., Dickinson P.J., Bollen P.D., Koblik P.H., Kass G.D., Kortz K.M., Vernau M.F., Knipe R.A., Lecouteur R.A. & Higgins R.J. 2008. Magnetic resonance imaging and histological classification of intracranial meningiomas in 112 dogs. J. Vet. Intern. Med. 22(3):586-595. http://dx.doi.org/10.1111/j.1939-1676.2008.00042.x. PMid:18466258.
https://doi.org/10.1111/j.1939-1676.2008...
). Este subtipo tem sido considerado com base em publicações e livros de referência mais recentes (Sturges et al. 2008Sturges B.K., Dickinson P.J., Bollen P.D., Koblik P.H., Kass G.D., Kortz K.M., Vernau M.F., Knipe R.A., Lecouteur R.A. & Higgins R.J. 2008. Magnetic resonance imaging and histological classification of intracranial meningiomas in 112 dogs. J. Vet. Intern. Med. 22(3):586-595. http://dx.doi.org/10.1111/j.1939-1676.2008.00042.x. PMid:18466258.
https://doi.org/10.1111/j.1939-1676.2008...
, Vandevelde et al. 2012Vandevelde R., Higgins R.J. & Oevermannn A. 2012. Neoplasia. p.129-156. In: Vandevelde R., Higgins R.J. & Oevermannn A. (Eds), Veterinary neuropathology essentials of theory and practice. Wiley-Blackwell, West Sussex. 212p., Cantile & Youssef 2016Cantile C. & Youssef S. 2016. Nervous system, p.251-406. In: Maxie M.G. (Ed.), Jubb, Kennedy and Palmer’s Pathology of Domestic Animals. Vol.1. 6th ed. Saunders Elsevier, Philadelphia. 797p. http://dx.doi.org/10.1016/B978-0-7020-5317-7.00004-7.
https://doi.org/10.1016/B978-0-7020-5317...
). Anteriormente, era denominado variante mixoide (Van Winkle et al. 1994Van Winkle T.J., Steinberg H.S., DeCarlo A.J., Dayrell-Hart B., Steinberg S.A., Smith C.A. & Summers B.A. 1994. Myxoid meningiomas of the Rostral Cervical Spinal Cord and Caudal Fossa in four dogs. Vet. Pathol. 31(4):468-471. http://dx.doi.org/10.1177/030098589403100410. PMid:7941237.
https://doi.org/10.1177/0300985894031004...
), porém passou a ser chamado cordoide pelos neuropatologistas americanos pela semelhança com a variante cordoide descrita em humanos (AFIP 2008Afip 2008. Armed Forces Institute of Pathology. Proceedings of the Wednesday Slide Conference, Silver Spring, MD. Disponível em <Disponível em http://www.askjpc.org/wsco/wsc_showcase2.php?id=192
> Acesso em 14 abr. 2015.
http://www.askjpc.org/wsco/wsc_showcase2...
). Invasão ao parênquima foi observada nos dois casos aqui descritos, semelhantemente a outro estudo (Sturges et al. 2008Sturges B.K., Dickinson P.J., Bollen P.D., Koblik P.H., Kass G.D., Kortz K.M., Vernau M.F., Knipe R.A., Lecouteur R.A. & Higgins R.J. 2008. Magnetic resonance imaging and histological classification of intracranial meningiomas in 112 dogs. J. Vet. Intern. Med. 22(3):586-595. http://dx.doi.org/10.1111/j.1939-1676.2008.00042.x. PMid:18466258.
https://doi.org/10.1111/j.1939-1676.2008...
).
Neste estudo, foi observada uma alta frequência (22,7%) de meningiomas de G-III comparado a maioria dos estudos internacionais em que os G-III perfizeram 1% (Sturges et al. 2008Sturges B.K., Dickinson P.J., Bollen P.D., Koblik P.H., Kass G.D., Kortz K.M., Vernau M.F., Knipe R.A., Lecouteur R.A. & Higgins R.J. 2008. Magnetic resonance imaging and histological classification of intracranial meningiomas in 112 dogs. J. Vet. Intern. Med. 22(3):586-595. http://dx.doi.org/10.1111/j.1939-1676.2008.00042.x. PMid:18466258.
https://doi.org/10.1111/j.1939-1676.2008...
) e 3% (Petersen et al. 2008Petersen S.A., Sturges B.K., Dickinson P.J., Pollard R.E., Kass P.H., Kent M., Vernau K.M., Lecouteur R.A. & Higgins R.J. 2008. Canine intraspinal meningiomas: imaging features, histopathologic classification, and long-term outcome in 34 dogs. J. Vet. Intern. Med. 22(4):946-953. http://dx.doi.org/10.1111/j.1939-1676.2008.0106.x. PMid:18482277.
https://doi.org/10.1111/j.1939-1676.2008...
). Isso foi consequência da alta frequência (18,2%; 4/22) do subtipo papilar aqui observada. Os meningiomas papilares são reportados esporadicamente na literatura veterinária (Koestner et al. 1999Koestner A., Bilzer T., Fatzer R., Schulmer F.Y.S., Summer B.A. & Van Winkle T.J. 1999. Histological classification of the tumors of the nervous system of domestic animals. p.25-26. In: Koestner A., Bilzer T., Fatzer R., Schulmer F.Y.S., Summer B.A. & Van Winkle T.J. (Eds), International Histological Classification of the Tumors of Domestic Animals. 2nd Series, Vol.5. Armed Forces Institute of Pathology, Washington, D.C., Montoliu et al. 2006Montoliu P., Anor S., Vidal E. & Pumarola M. 2006. Histological and immunohistochemical study of 30 cases of canine meningioma. J. Comp. Pathol. 135(4):200-207. http://dx.doi.org/10.1016/j.jcpa.2006.06.006. PMid:17049358.
https://doi.org/10.1016/j.jcpa.2006.06.0...
), e em outros estudos retrospectivos eles não foram observados (Petersen et al. 2008Petersen S.A., Sturges B.K., Dickinson P.J., Pollard R.E., Kass P.H., Kent M., Vernau K.M., Lecouteur R.A. & Higgins R.J. 2008. Canine intraspinal meningiomas: imaging features, histopathologic classification, and long-term outcome in 34 dogs. J. Vet. Intern. Med. 22(4):946-953. http://dx.doi.org/10.1111/j.1939-1676.2008.0106.x. PMid:18482277.
https://doi.org/10.1111/j.1939-1676.2008...
, Sturges et al. 2008Sturges B.K., Dickinson P.J., Bollen P.D., Koblik P.H., Kass G.D., Kortz K.M., Vernau M.F., Knipe R.A., Lecouteur R.A. & Higgins R.J. 2008. Magnetic resonance imaging and histological classification of intracranial meningiomas in 112 dogs. J. Vet. Intern. Med. 22(3):586-595. http://dx.doi.org/10.1111/j.1939-1676.2008.00042.x. PMid:18466258.
https://doi.org/10.1111/j.1939-1676.2008...
). Em um estudo na Itália (Mandara et al. 2015Mandara M.T., Reginato A., Foiani G., Baroni M., Poli F., Gasparinetti N. & Bernardini M. 2015. Papillary meningioma in the dog: a clinicopathological case series study. Res. Vet. Sci. 100:213-219. http://dx.doi.org/10.1016/j.rvsc.2015.03.029. PMid:25847284.
https://doi.org/10.1016/j.rvsc.2015.03.0...
), houve também uma alta frequência de meningiomas papilares (15,7%). Dos quatro casos de meningioma papilar, um deles apresentou critérios de malignidade como invasão intravascular que foi semelhante aos meningiomas papilares em humanos. Segundo a OMS, a taxa de metástase extracraniana de meningiomas papilares em humanos é relatada em 20% dos casos (Lopes & Vandenberg 2013Lopes M.B.S. & Vandenberg S.R. 2013. Tumor of the central nervous system, p.1933-2031. In: Fletcher C.D.M. (Ed.), Diagnostic Histopathology of Tumors. Vol.2. 4th ed. Saunders Elsevier, Philadelphia. 2145p.).
Segundo uma revisão (Motta et al. 2012Motta L., Mandara M.T. & Skerritt G.C. 2012. Canine and feline intracranial meningiomas: an updated review. Vet J. 192(2):153-165. http://dx.doi.org/10.1016/j.tvjl.2011.10.008. PMid:22104505.
https://doi.org/10.1016/j.tvjl.2011.10.0...
), a ocorrência de metástases de meningiomas é rara em animais domésticos e tem sido sugerido que as metástases de meningiomas são infrequentes devido à presença de intercomunicações desmossomais e interdigitações entre as células das meninges, o que reduz a esfoliação celular. As metástases ocorreriam por via hematógena ou pelo líquor (Long 2006Long S. 2006. Neoplasia of the Nervous System. Disponível em <Disponível em http://www.ivis.org/advances/Vite/braund26/chapter. asp?LA=1
> Accesso em 14 abr. 2015.
http://www.ivis.org/advances/Vite/braund...
). A malignidade dos meningiomas G-III em cães não está apenas associada à sua capacidade de metastatizar para fora do SNC (Vandevelde et al. 2012Vandevelde R., Higgins R.J. & Oevermannn A. 2012. Neoplasia. p.129-156. In: Vandevelde R., Higgins R.J. & Oevermannn A. (Eds), Veterinary neuropathology essentials of theory and practice. Wiley-Blackwell, West Sussex. 212p.), embora isso possa ocorrer eventualmente (Geib 1966Geib L.W. 1966. Ossifying meningioma with extracranial metastasis in a dog. Pathol Vet. 3(3):247-254. PMid:6006232., Schulman et al. 1992Schulman F.Y., Ribas J.L., Carpenter J.L., Sisson A.F. & LeCouteur R.A. 1992. Intracranial meningioma with pulmonary metastasis in three dogs. Vet. Pathol. 29(3):196-202. http://dx.doi.org/10.1177/030098589202900302. PMid:1621330.
https://doi.org/10.1177/0300985892029003...
, Pérez et al. 2005Pérez V., Vidal E., González N., Benavides J., Ferreras M.C., Villagrasa M. & Pumarola M. 2005. Orbital meningioma with a granular cell component in a dog, with extracranial metastasis. J. Comp. Pathol. 133(2-3):212-217. http://dx.doi.org/10.1016/j.jcpa.2005.02.003. PMid:16045918.
https://doi.org/10.1016/j.jcpa.2005.02.0...
). Ela está também associada a fatores que incluem alta taxa mitótica e características citológicas malignas, para o subtipo maligno (Cantile & Youssef 2016Cantile C. & Youssef S. 2016. Nervous system, p.251-406. In: Maxie M.G. (Ed.), Jubb, Kennedy and Palmer’s Pathology of Domestic Animals. Vol.1. 6th ed. Saunders Elsevier, Philadelphia. 797p. http://dx.doi.org/10.1016/B978-0-7020-5317-7.00004-7.
https://doi.org/10.1016/B978-0-7020-5317...
), e alta taxa de recidiva pós-cirúrgica e um baixo tempo de sobrevivência, para o subtipo papilar (Mandara et al. 2015Mandara M.T., Reginato A., Foiani G., Baroni M., Poli F., Gasparinetti N. & Bernardini M. 2015. Papillary meningioma in the dog: a clinicopathological case series study. Res. Vet. Sci. 100:213-219. http://dx.doi.org/10.1016/j.rvsc.2015.03.029. PMid:25847284.
https://doi.org/10.1016/j.rvsc.2015.03.0...
).
Apesar de existirem poucos trabalhos que apresentem a graduação de meningiomas de cães, a maioria concorda que o subtipo maligno é incomum (Petersen et al. 2008Petersen S.A., Sturges B.K., Dickinson P.J., Pollard R.E., Kass P.H., Kent M., Vernau K.M., Lecouteur R.A. & Higgins R.J. 2008. Canine intraspinal meningiomas: imaging features, histopathologic classification, and long-term outcome in 34 dogs. J. Vet. Intern. Med. 22(4):946-953. http://dx.doi.org/10.1111/j.1939-1676.2008.0106.x. PMid:18482277.
https://doi.org/10.1111/j.1939-1676.2008...
, Sturges et al. 2008Sturges B.K., Dickinson P.J., Bollen P.D., Koblik P.H., Kass G.D., Kortz K.M., Vernau M.F., Knipe R.A., Lecouteur R.A. & Higgins R.J. 2008. Magnetic resonance imaging and histological classification of intracranial meningiomas in 112 dogs. J. Vet. Intern. Med. 22(3):586-595. http://dx.doi.org/10.1111/j.1939-1676.2008.00042.x. PMid:18466258.
https://doi.org/10.1111/j.1939-1676.2008...
). Neste estudo, o principal critério de classificação do subtipo maligno foi a alta taxa mitótica (27/10cga; o critério é >20/10 cga). Em geral, esse subtipo pode ter morfologia acentuadamente anaplásica ou indiferenciada, afastando-se da morfologia meningotelial e aproximando-se dos sarcomas, carcinomas ou melanomas (Vandevelde et al. 2012Vandevelde R., Higgins R.J. & Oevermannn A. 2012. Neoplasia. p.129-156. In: Vandevelde R., Higgins R.J. & Oevermannn A. (Eds), Veterinary neuropathology essentials of theory and practice. Wiley-Blackwell, West Sussex. 212p., Cantile & Youssef 2016Cantile C. & Youssef S. 2016. Nervous system, p.251-406. In: Maxie M.G. (Ed.), Jubb, Kennedy and Palmer’s Pathology of Domestic Animals. Vol.1. 6th ed. Saunders Elsevier, Philadelphia. 797p. http://dx.doi.org/10.1016/B978-0-7020-5317-7.00004-7.
https://doi.org/10.1016/B978-0-7020-5317...
). No caso estudado, havia áreas pouco diferenciadas, porém havia áreas menores e focais de diferenciação meningotelial, assegurando o diagnóstico histológico de meningioma. Para meningiomas é reconhecido que o diagnóstico definitivo mais confiável é feito através exame histopatológico (Sturges et al. 2008Sturges B.K., Dickinson P.J., Bollen P.D., Koblik P.H., Kass G.D., Kortz K.M., Vernau M.F., Knipe R.A., Lecouteur R.A. & Higgins R.J. 2008. Magnetic resonance imaging and histological classification of intracranial meningiomas in 112 dogs. J. Vet. Intern. Med. 22(3):586-595. http://dx.doi.org/10.1111/j.1939-1676.2008.00042.x. PMid:18466258.
https://doi.org/10.1111/j.1939-1676.2008...
, Motta et al. 2012Motta L., Mandara M.T. & Skerritt G.C. 2012. Canine and feline intracranial meningiomas: an updated review. Vet J. 192(2):153-165. http://dx.doi.org/10.1016/j.tvjl.2011.10.008. PMid:22104505.
https://doi.org/10.1016/j.tvjl.2011.10.0...
).
De acordo com a literatura (Patnaik et al. 1986Patnaik A.K., Kay W.J. & Hurvitz A.I. 1986. Intracranial meningioma: a comparative pathologic study of 28 dogs. Vet. Pathol. 23(4):369-373. http://dx.doi.org/10.1177/030098588602300404. PMid:3750730.
https://doi.org/10.1177/0300985886023004...
, Montoliu et al. 2006Montoliu P., Anor S., Vidal E. & Pumarola M. 2006. Histological and immunohistochemical study of 30 cases of canine meningioma. J. Comp. Pathol. 135(4):200-207. http://dx.doi.org/10.1016/j.jcpa.2006.06.006. PMid:17049358.
https://doi.org/10.1016/j.jcpa.2006.06.0...
, Sturges et al. 2008Sturges B.K., Dickinson P.J., Bollen P.D., Koblik P.H., Kass G.D., Kortz K.M., Vernau M.F., Knipe R.A., Lecouteur R.A. & Higgins R.J. 2008. Magnetic resonance imaging and histological classification of intracranial meningiomas in 112 dogs. J. Vet. Intern. Med. 22(3):586-595. http://dx.doi.org/10.1111/j.1939-1676.2008.00042.x. PMid:18466258.
https://doi.org/10.1111/j.1939-1676.2008...
, Vandevelde et al. 2012Vandevelde R., Higgins R.J. & Oevermannn A. 2012. Neoplasia. p.129-156. In: Vandevelde R., Higgins R.J. & Oevermannn A. (Eds), Veterinary neuropathology essentials of theory and practice. Wiley-Blackwell, West Sussex. 212p., Cantile & Youssef 2016Cantile C. & Youssef S. 2016. Nervous system, p.251-406. In: Maxie M.G. (Ed.), Jubb, Kennedy and Palmer’s Pathology of Domestic Animals. Vol.1. 6th ed. Saunders Elsevier, Philadelphia. 797p. http://dx.doi.org/10.1016/B978-0-7020-5317-7.00004-7.
https://doi.org/10.1016/B978-0-7020-5317...
) não há predisposição por sexo em cães. Em contraste, em humanos há maior predisposição em mulheres, talvez associada a receptores esteroidais intratumorais. Nas mulheres, a grande maioria dos meningiomas são de G-I. Entretanto, meningiomas com alta graduação são mais frequentes em homens (Lopes & Vandenberg 2013Lopes M.B.S. & Vandenberg S.R. 2013. Tumor of the central nervous system, p.1933-2031. In: Fletcher C.D.M. (Ed.), Diagnostic Histopathology of Tumors. Vol.2. 4th ed. Saunders Elsevier, Philadelphia. 2145p.). No estudo de Mandara et al. (2015)Mandara M.T., Reginato A., Foiani G., Baroni M., Poli F., Gasparinetti N. & Bernardini M. 2015. Papillary meningioma in the dog: a clinicopathological case series study. Res. Vet. Sci. 100:213-219. http://dx.doi.org/10.1016/j.rvsc.2015.03.029. PMid:25847284.
https://doi.org/10.1016/j.rvsc.2015.03.0...
, meningiomas papilares (G-III) foram mais observados em cães machos (10/16). Neste estudo, a ocorrência de meningiomas foi maior em cadelas (relação macho:fêmea de 1:2,7), semelhante ao observado por outros autores (Petersen et al. 2008Petersen S.A., Sturges B.K., Dickinson P.J., Pollard R.E., Kass P.H., Kent M., Vernau K.M., Lecouteur R.A. & Higgins R.J. 2008. Canine intraspinal meningiomas: imaging features, histopathologic classification, and long-term outcome in 34 dogs. J. Vet. Intern. Med. 22(4):946-953. http://dx.doi.org/10.1111/j.1939-1676.2008.0106.x. PMid:18482277.
https://doi.org/10.1111/j.1939-1676.2008...
, Costa 2009Costa R.C. 2009. Neoplasias do sistema nervoso, p.412-427. In: Daleck R.C., De Nardi A.B. & Rodaski S. (Eds), Oncologia em Cães e Gatos. Roca, São Paulo. 612p.), sendo as fêmeas mais representadas nos de G-I (10/14), as únicas acometidas no G-II e perfizeram 3/5 no G-III.
De forma geral, como ocorre para a maioria das neoplasias, independente da origem, cães mais velhos foram os mais acometidos nos 22 casos analisados, em que 50,4% (12/22) tinham 10 anos ou mais, não diferindo de estudos anteriores (Patnaik et al. 1986Patnaik A.K., Kay W.J. & Hurvitz A.I. 1986. Intracranial meningioma: a comparative pathologic study of 28 dogs. Vet. Pathol. 23(4):369-373. http://dx.doi.org/10.1177/030098588602300404. PMid:3750730.
https://doi.org/10.1177/0300985886023004...
, Snyder et al. 2006Snyder J.M., Shofer F.S., Van Winkle T.J. & Massicotte C. 2006. Canine intracranial primary neoplasia: 173 cases (1986-2003). J. Vet. Intern. Med. 20(3):669-675. PMid:16734106., Sturges et al. 2008Sturges B.K., Dickinson P.J., Bollen P.D., Koblik P.H., Kass G.D., Kortz K.M., Vernau M.F., Knipe R.A., Lecouteur R.A. & Higgins R.J. 2008. Magnetic resonance imaging and histological classification of intracranial meningiomas in 112 dogs. J. Vet. Intern. Med. 22(3):586-595. http://dx.doi.org/10.1111/j.1939-1676.2008.00042.x. PMid:18466258.
https://doi.org/10.1111/j.1939-1676.2008...
, Costa 2009Costa R.C. 2009. Neoplasias do sistema nervoso, p.412-427. In: Daleck R.C., De Nardi A.B. & Rodaski S. (Eds), Oncologia em Cães e Gatos. Roca, São Paulo. 612p.). Em humanos o subtipo papilar (G-III) é mais frequente em jovens (Lopes & Vandenberg 2013Lopes M.B.S. & Vandenberg S.R. 2013. Tumor of the central nervous system, p.1933-2031. In: Fletcher C.D.M. (Ed.), Diagnostic Histopathology of Tumors. Vol.2. 4th ed. Saunders Elsevier, Philadelphia. 2145p.). Entretanto, num estudo de 16 cães com meningioma papilar, a média de idade foi 10 anos (cães idosos) (Mandara et al. 2015Mandara M.T., Reginato A., Foiani G., Baroni M., Poli F., Gasparinetti N. & Bernardini M. 2015. Papillary meningioma in the dog: a clinicopathological case series study. Res. Vet. Sci. 100:213-219. http://dx.doi.org/10.1016/j.rvsc.2015.03.029. PMid:25847284.
https://doi.org/10.1016/j.rvsc.2015.03.0...
). Neste estudo, a média de idade para cães com este subtipo (e grau) foi de 8 anos (cães adultos). Para os G-I e G-II, as médias de idade foram 11 e 12 anos, respectivamente.
Meningiomas em cães são descritos comumente no Pastor Alemão (Patnaik et al. 1986Patnaik A.K., Kay W.J. & Hurvitz A.I. 1986. Intracranial meningioma: a comparative pathologic study of 28 dogs. Vet. Pathol. 23(4):369-373. http://dx.doi.org/10.1177/030098588602300404. PMid:3750730.
https://doi.org/10.1177/0300985886023004...
, Montoliu et al. 2006Montoliu P., Anor S., Vidal E. & Pumarola M. 2006. Histological and immunohistochemical study of 30 cases of canine meningioma. J. Comp. Pathol. 135(4):200-207. http://dx.doi.org/10.1016/j.jcpa.2006.06.006. PMid:17049358.
https://doi.org/10.1016/j.jcpa.2006.06.0...
, Sturges et al. 2008Sturges B.K., Dickinson P.J., Bollen P.D., Koblik P.H., Kass G.D., Kortz K.M., Vernau M.F., Knipe R.A., Lecouteur R.A. & Higgins R.J. 2008. Magnetic resonance imaging and histological classification of intracranial meningiomas in 112 dogs. J. Vet. Intern. Med. 22(3):586-595. http://dx.doi.org/10.1111/j.1939-1676.2008.00042.x. PMid:18466258.
https://doi.org/10.1111/j.1939-1676.2008...
), Boxer (Montoliu et al. 2006Montoliu P., Anor S., Vidal E. & Pumarola M. 2006. Histological and immunohistochemical study of 30 cases of canine meningioma. J. Comp. Pathol. 135(4):200-207. http://dx.doi.org/10.1016/j.jcpa.2006.06.006. PMid:17049358.
https://doi.org/10.1016/j.jcpa.2006.06.0...
, Petersen et al. 2008Petersen S.A., Sturges B.K., Dickinson P.J., Pollard R.E., Kass P.H., Kent M., Vernau K.M., Lecouteur R.A. & Higgins R.J. 2008. Canine intraspinal meningiomas: imaging features, histopathologic classification, and long-term outcome in 34 dogs. J. Vet. Intern. Med. 22(4):946-953. http://dx.doi.org/10.1111/j.1939-1676.2008.0106.x. PMid:18482277.
https://doi.org/10.1111/j.1939-1676.2008...
, Sturges et al. 2008Sturges B.K., Dickinson P.J., Bollen P.D., Koblik P.H., Kass G.D., Kortz K.M., Vernau M.F., Knipe R.A., Lecouteur R.A. & Higgins R.J. 2008. Magnetic resonance imaging and histological classification of intracranial meningiomas in 112 dogs. J. Vet. Intern. Med. 22(3):586-595. http://dx.doi.org/10.1111/j.1939-1676.2008.00042.x. PMid:18466258.
https://doi.org/10.1111/j.1939-1676.2008...
, Vandevelde et al. 2012Vandevelde R., Higgins R.J. & Oevermannn A. 2012. Neoplasia. p.129-156. In: Vandevelde R., Higgins R.J. & Oevermannn A. (Eds), Veterinary neuropathology essentials of theory and practice. Wiley-Blackwell, West Sussex. 212p.), Golden Retriever (Petersen et al. 2008Petersen S.A., Sturges B.K., Dickinson P.J., Pollard R.E., Kass P.H., Kent M., Vernau K.M., Lecouteur R.A. & Higgins R.J. 2008. Canine intraspinal meningiomas: imaging features, histopathologic classification, and long-term outcome in 34 dogs. J. Vet. Intern. Med. 22(4):946-953. http://dx.doi.org/10.1111/j.1939-1676.2008.0106.x. PMid:18482277.
https://doi.org/10.1111/j.1939-1676.2008...
, Sturges et al. 2008Sturges B.K., Dickinson P.J., Bollen P.D., Koblik P.H., Kass G.D., Kortz K.M., Vernau M.F., Knipe R.A., Lecouteur R.A. & Higgins R.J. 2008. Magnetic resonance imaging and histological classification of intracranial meningiomas in 112 dogs. J. Vet. Intern. Med. 22(3):586-595. http://dx.doi.org/10.1111/j.1939-1676.2008.00042.x. PMid:18466258.
https://doi.org/10.1111/j.1939-1676.2008...
, Vandevelde et al. 2012Vandevelde R., Higgins R.J. & Oevermannn A. 2012. Neoplasia. p.129-156. In: Vandevelde R., Higgins R.J. & Oevermannn A. (Eds), Veterinary neuropathology essentials of theory and practice. Wiley-Blackwell, West Sussex. 212p.), Labrador (Petersen et al. 2008Petersen S.A., Sturges B.K., Dickinson P.J., Pollard R.E., Kass P.H., Kent M., Vernau K.M., Lecouteur R.A. & Higgins R.J. 2008. Canine intraspinal meningiomas: imaging features, histopathologic classification, and long-term outcome in 34 dogs. J. Vet. Intern. Med. 22(4):946-953. http://dx.doi.org/10.1111/j.1939-1676.2008.0106.x. PMid:18482277.
https://doi.org/10.1111/j.1939-1676.2008...
, Sturges et al. 2008Sturges B.K., Dickinson P.J., Bollen P.D., Koblik P.H., Kass G.D., Kortz K.M., Vernau M.F., Knipe R.A., Lecouteur R.A. & Higgins R.J. 2008. Magnetic resonance imaging and histological classification of intracranial meningiomas in 112 dogs. J. Vet. Intern. Med. 22(3):586-595. http://dx.doi.org/10.1111/j.1939-1676.2008.00042.x. PMid:18466258.
https://doi.org/10.1111/j.1939-1676.2008...
), Poodle (Marcasso et al. 2015Marcasso R.A., Moreira J.R., Valentim L.G., Arias M.V.B. & Bracarense A.P.F.R.L. 2015. Meningiomas em cães: aspectos clínicos, histopatológicos e imuno-histoquímicos. Pesq. Vet. Bras. 35(10):844-852. http://dx.doi.org/10.1590/S0100-736X2015001000005.
https://doi.org/10.1590/S0100-736X201500...
), Collie (Petersen et al. 2008Petersen S.A., Sturges B.K., Dickinson P.J., Pollard R.E., Kass P.H., Kent M., Vernau K.M., Lecouteur R.A. & Higgins R.J. 2008. Canine intraspinal meningiomas: imaging features, histopathologic classification, and long-term outcome in 34 dogs. J. Vet. Intern. Med. 22(4):946-953. http://dx.doi.org/10.1111/j.1939-1676.2008.0106.x. PMid:18482277.
https://doi.org/10.1111/j.1939-1676.2008...
) e Terriers (Song et al. 2013Song R.B., Vite C.H., Bradley C.W. & Cross J.R. 2013. Postmortem evaluation of 435 cases of intracranial neoplasia in dogs and relationship of neoplasm with breed, age, and body weight. J. Vet. Intern. Med. 27(5):1143-1152. http://dx.doi.org/10.1111/jvim.12136. PMid:23865437.
https://doi.org/10.1111/jvim.12136...
). Neste estudo, cães de raça foram os mais acometidos, sendo que a raça Boxer (31,8%) foi a mais representada, seguida pelo Pastor Alemão (18,1%). É válido salientar que na população de raças de cães necropsiados no LPV-UFSM entre 1994 e 2003, as raças Pastor Alemão e Boxer ocuparam o primeiro e terceiro lugares em prevalência, respectivamente, e entre 2004 e 2013 elas ocuparam o terceiro e sexto lugares, respectivamente (Flores 2016Flores M.M. 2016. Aspectos epidemiológicos do câncer em cães da região central do rio grande do sul: 50 anos (1964-2013). Tese de Doutorado em Medicina Veterinária, Universidade Federal de Santa Maria, Santa Maria, RS. 90p.). Apesar do número de casos analisados ser limitado, chama a atenção que de cinco casos classificados como G-III, quatro eram cães Boxer.
Por tratar-se de um sistema de classificação de meningiomas caninos adaptado de humanos, com um número ainda restrito de publicações (Petersen et al. 2008Petersen S.A., Sturges B.K., Dickinson P.J., Pollard R.E., Kass P.H., Kent M., Vernau K.M., Lecouteur R.A. & Higgins R.J. 2008. Canine intraspinal meningiomas: imaging features, histopathologic classification, and long-term outcome in 34 dogs. J. Vet. Intern. Med. 22(4):946-953. http://dx.doi.org/10.1111/j.1939-1676.2008.0106.x. PMid:18482277.
https://doi.org/10.1111/j.1939-1676.2008...
, Sturges et al. 2008Sturges B.K., Dickinson P.J., Bollen P.D., Koblik P.H., Kass G.D., Kortz K.M., Vernau M.F., Knipe R.A., Lecouteur R.A. & Higgins R.J. 2008. Magnetic resonance imaging and histological classification of intracranial meningiomas in 112 dogs. J. Vet. Intern. Med. 22(3):586-595. http://dx.doi.org/10.1111/j.1939-1676.2008.00042.x. PMid:18466258.
https://doi.org/10.1111/j.1939-1676.2008...
, José-López et al. 2013José-López R., De la Fuente C., Pumarola M. & Anor S. 2013. Spinal meningiomas in dogs: description of 8 cases including a novel radiological and histopathological presentation. Can. Vet. J. 54(10):948-954. PMid:24155414., Mandara et al. 2015Mandara M.T., Reginato A., Foiani G., Baroni M., Poli F., Gasparinetti N. & Bernardini M. 2015. Papillary meningioma in the dog: a clinicopathological case series study. Res. Vet. Sci. 100:213-219. http://dx.doi.org/10.1016/j.rvsc.2015.03.029. PMid:25847284.
https://doi.org/10.1016/j.rvsc.2015.03.0...
), a discussão sobre a relação entre os graus histológicos e a evolução clínica ainda permanece limitada, pois ainda não há parâmetros bem estabelecidos para o tempo médio de sobrevivência dos cães após o início dos sinais clínicos em cada grau da classificação histológica. Para humanos, há uma relação bem estabelecida neste sistema de graduação, a qual é baseada no tempo de sobrevivência pós-cirurgia e radioterapia (por exemplo, o tempo livre de recidiva de 10 anos foi de 95% para os G-I, de 56% para os G-II e inexistente para os G-III, os quais não sobreviveram a esse período) (Pizem et al. 2014Pizem J., Velnar T., Prestor B., Mlakar J. & Popovic M. 2014. Brain invasion assessability in meningiomas is related to meningioma size and grade, and can be improved by extensive sampling of the surgically removed meningioma specimen. Clin. Neuropathol. 33(5):354-363. http://dx.doi.org/10.5414/NP300750. PMid:25034703.
https://doi.org/10.5414/NP300750...
). Entretanto, os dados obtidos neste estudo servem como parâmetros comparativos para estudos futuros de meningiomas em cães graduados por este sistema. Os cães com meningiomas G-I tiveram o maior tempo de sobrevivência (máximo de um ano) após a manifestação dos sinais clínicos (8/14 receberam tratamento clínico, incluindo corticoides e anticonvulsivantes). Dos G-III, o tempo máximo de sobrevivência foi de 90 dias, sendo que 2/5 receberam tratamento clínico e dos G-II, o tempo máximo foi de 20 dias, sendo que 2/3 receberam tratamento. Não foi possível estabelecer os fatores que influenciaram na maior sobrevivência dos cães com meningiomas G-III em relação aos G-II aqui estudados, ou a influência do tratamento nessa evolução clínica. Nenhum dos cães deste estudo foi submetido a tratamento cirúrgico.
Ainda assim, algumas comparações podem ser feitas com alguns subtipos específicos. Há um estudo de oito cães com meningiomas G-III (subtipo papilar) em que os animais apenas receberam terapias de suporte e a evolução clínica variou de 1 a 90 dias (Mandara et al. 2015Mandara M.T., Reginato A., Foiani G., Baroni M., Poli F., Gasparinetti N. & Bernardini M. 2015. Papillary meningioma in the dog: a clinicopathological case series study. Res. Vet. Sci. 100:213-219. http://dx.doi.org/10.1016/j.rvsc.2015.03.029. PMid:25847284.
https://doi.org/10.1016/j.rvsc.2015.03.0...
). Neste estudo, quatro cães com meningiomas papilares, dois que receberam e dois que não receberam tratamento, tiveram uma evolução clínica de 30 a 90 dias. Nos dois casos aqui descritos de meningiomas G-I intraespinhais, sem tratamento cirúrgico, a evolução dos sinais clínicos variou de 60 a 120 dias, sendo que, com tratamento cirúrgico, meningiomas G-I tiveram evolução de 110 a 600 dias. O único meningioma G-II intraespinhal (subtipo atípico) deste estudo teve evolução clínica de sete dias. Casos de neoplasmas semelhantes tratados cirurgicamente tiveram evolução de 300 a 540 dias (José-López et al. 2013José-López R., De la Fuente C., Pumarola M. & Anor S. 2013. Spinal meningiomas in dogs: description of 8 cases including a novel radiological and histopathological presentation. Can. Vet. J. 54(10):948-954. PMid:24155414.).
A localização anatômica dos meningiomas determina a sua denominação, tais como, meningiomas intracranianos, intraespinhais, retro-bulbares e paranasais (Koestner & Higgins 2002Koestner A. & Higgins R. 2002. Tumors of the nervous system, p.697-738. In: Meuten D.J. (Ed.), Tumors in Domestic Animals. 4th ed. Iowa State Press, Iowa. 788p., Vandevelde et al. 2012Vandevelde R., Higgins R.J. & Oevermannn A. 2012. Neoplasia. p.129-156. In: Vandevelde R., Higgins R.J. & Oevermannn A. (Eds), Veterinary neuropathology essentials of theory and practice. Wiley-Blackwell, West Sussex. 212p.). A localização dos meningiomas intracranianos foi mais prevalente na região supratentorial como as regiões olfatória, parassagital, convexidade do cérebro e parasselar, semelhante a outros estudos (Patnaik et al. 1986Patnaik A.K., Kay W.J. & Hurvitz A.I. 1986. Intracranial meningioma: a comparative pathologic study of 28 dogs. Vet. Pathol. 23(4):369-373. http://dx.doi.org/10.1177/030098588602300404. PMid:3750730.
https://doi.org/10.1177/0300985886023004...
, Summers et al. 1995Summers B.A., Cummings J.F. & De Lahunta A. 1995. Tumors of the central nervous system, p.351-401. In: Summers B.A., Cummings J.F. & De Lahunta A. (Eds), Veterinary Neuropathology. Mosby, Missouri., Koestner & Higgins 2002Koestner A. & Higgins R. 2002. Tumors of the nervous system, p.697-738. In: Meuten D.J. (Ed.), Tumors in Domestic Animals. 4th ed. Iowa State Press, Iowa. 788p., Snyder et al. 2006Snyder J.M., Shofer F.S., Van Winkle T.J. & Massicotte C. 2006. Canine intracranial primary neoplasia: 173 cases (1986-2003). J. Vet. Intern. Med. 20(3):669-675. PMid:16734106., Sturges et al. 2008Sturges B.K., Dickinson P.J., Bollen P.D., Koblik P.H., Kass G.D., Kortz K.M., Vernau M.F., Knipe R.A., Lecouteur R.A. & Higgins R.J. 2008. Magnetic resonance imaging and histological classification of intracranial meningiomas in 112 dogs. J. Vet. Intern. Med. 22(3):586-595. http://dx.doi.org/10.1111/j.1939-1676.2008.00042.x. PMid:18466258.
https://doi.org/10.1111/j.1939-1676.2008...
), que sugerem uma correlação direta com a densidade dos vilos da aracnoide nessas áreas, como descrito em humanos (Vandevelde et al. 2012Vandevelde R., Higgins R.J. & Oevermannn A. 2012. Neoplasia. p.129-156. In: Vandevelde R., Higgins R.J. & Oevermannn A. (Eds), Veterinary neuropathology essentials of theory and practice. Wiley-Blackwell, West Sussex. 212p.). Em um estudo de 112 casos de meningiomas em cães, não foi observada relação do grau histológico com a localização intracraniana (Sturges et al. 2008Sturges B.K., Dickinson P.J., Bollen P.D., Koblik P.H., Kass G.D., Kortz K.M., Vernau M.F., Knipe R.A., Lecouteur R.A. & Higgins R.J. 2008. Magnetic resonance imaging and histological classification of intracranial meningiomas in 112 dogs. J. Vet. Intern. Med. 22(3):586-595. http://dx.doi.org/10.1111/j.1939-1676.2008.00042.x. PMid:18466258.
https://doi.org/10.1111/j.1939-1676.2008...
). Em contraste, os meningiomas G-II e G-III em humanos ocorrem em baixa frequência na base do crânio (Sade et al. 2007Sade B., Chahlavi A., Krishnaney A., Nagel S., Choi E. & Lee J.H. 2007. World Health Organization Grades II and III meningiomas are rare in the cranial base and spine. Neurosurgery 61(6):1194-1198, discussion 1198. http://dx.doi.org/10.1227/01.neu.0000306097.38141.65. PMid:18162898.
https://doi.org/10.1227/01.neu.000030609...
). Neste estudo, a localização parasselar foi observada em um caso de G-II e em um caso de G-III. Em outro caso de G-III a localização foi na região olfatória. Em outros estudos, apesar de não ter sido discutido o assunto, foi observada uma baixa frequência de G-II e G-III na base do crânio em cães (Mandara et al. 2010Mandara M.T., Pavone S., Brunetti B. & Mandrioli L. 2010. A comparative study of canine and feline meningioma classification based on the WHO histological classification system in humans. Proc. 22nd Symposium ESVN-ECVN, Bologna, 24-26 September 2009. J. Vet. Intern. Med. 24:235-258., Rissi 2015Rissi D.R. 2015. A retrospective study of skull base neoplasia in 42 dogs. J. Vet. Diagn. Invest. 27(6):743-748. http://dx.doi.org/10.1177/1040638715611706. PMid:26462763.
https://doi.org/10.1177/1040638715611706...
).
A localização dos três meningiomas intraespinhais neste estudo ficou restrita entre as regiões de C1 a T2 e eram intradurais/extramedulares. Em outros estudos foi observada uma relação de maior frequência de meningiomas G-I no segmento C1-C4 e os G-II eram predominantes mais caudalmente (Petersen et al. 2008Petersen S.A., Sturges B.K., Dickinson P.J., Pollard R.E., Kass P.H., Kent M., Vernau K.M., Lecouteur R.A. & Higgins R.J. 2008. Canine intraspinal meningiomas: imaging features, histopathologic classification, and long-term outcome in 34 dogs. J. Vet. Intern. Med. 22(4):946-953. http://dx.doi.org/10.1111/j.1939-1676.2008.0106.x. PMid:18482277.
https://doi.org/10.1111/j.1939-1676.2008...
, Vandevelde et al. 2012Vandevelde R., Higgins R.J. & Oevermannn A. 2012. Neoplasia. p.129-156. In: Vandevelde R., Higgins R.J. & Oevermannn A. (Eds), Veterinary neuropathology essentials of theory and practice. Wiley-Blackwell, West Sussex. 212p.). A maioria dos meningiomas intraespinais humanos ocorre na região torácica. A razão dessa predileção ainda não foi estabelecida, mas em humanos as células da membrana aracnoide (encontradas dentro de proliferações aracnoides) poderiam ser as células progenitoras para os meningiomas e outros tipos de proliferações aracnoides, sendo mais comuns na coluna torácica. A distribuição das proliferações aracnoides nas meninges espinhais em cães é desconhecida (Petersen et al. 2008Petersen S.A., Sturges B.K., Dickinson P.J., Pollard R.E., Kass P.H., Kent M., Vernau K.M., Lecouteur R.A. & Higgins R.J. 2008. Canine intraspinal meningiomas: imaging features, histopathologic classification, and long-term outcome in 34 dogs. J. Vet. Intern. Med. 22(4):946-953. http://dx.doi.org/10.1111/j.1939-1676.2008.0106.x. PMid:18482277.
https://doi.org/10.1111/j.1939-1676.2008...
).
Os sinais neurológicos decorrentes de tumores no SNC dependem do tamanho, da localização e da taxa de crescimento tumoral (Costa 2009Costa R.C. 2009. Neoplasias do sistema nervoso, p.412-427. In: Daleck R.C., De Nardi A.B. & Rodaski S. (Eds), Oncologia em Cães e Gatos. Roca, São Paulo. 612p.). Devido a sua cronicidade, as neoplasias causam sinais neurológicos progressivos (Summers et al. 1995Summers B.A., Cummings J.F. & De Lahunta A. 1995. Tumors of the central nervous system, p.351-401. In: Summers B.A., Cummings J.F. & De Lahunta A. (Eds), Veterinary Neuropathology. Mosby, Missouri.). Com relação à localização intracraniana, os sinais de alteração tálamo-cortical (65%) foram os mais frequentes, como previamente observado (Costa 2009Costa R.C. 2009. Neoplasias do sistema nervoso, p.412-427. In: Daleck R.C., De Nardi A.B. & Rodaski S. (Eds), Oncologia em Cães e Gatos. Roca, São Paulo. 612p., Marcasso et al. 2015Marcasso R.A., Moreira J.R., Valentim L.G., Arias M.V.B. & Bracarense A.P.F.R.L. 2015. Meningiomas em cães: aspectos clínicos, histopatológicos e imuno-histoquímicos. Pesq. Vet. Bras. 35(10):844-852. http://dx.doi.org/10.1590/S0100-736X2015001000005.
https://doi.org/10.1590/S0100-736X201500...
), e foram caracterizados principalmente por convulsão (76,9%). Crise convulsiva é a manifestação neurológica mais frequente em cães com neoplasmas encefálicos de qualquer origem (Bagley & Gavin 1998Bagley R.S. & Gavin P.R. 1998. Seizures as a complication of brain tumors in dogs. Clin. Tech. Small Anim. Pract. 13(3):179-184. http://dx.doi.org/10.1016/S1096-2867(98)80039-X. PMid:9775508.
https://doi.org/10.1016/S1096-2867(98)80...
, Snyder et al. 2006Snyder J.M., Shofer F.S., Van Winkle T.J. & Massicotte C. 2006. Canine intracranial primary neoplasia: 173 cases (1986-2003). J. Vet. Intern. Med. 20(3):669-675. PMid:16734106., Costa 2009Costa R.C. 2009. Neoplasias do sistema nervoso, p.412-427. In: Daleck R.C., De Nardi A.B. & Rodaski S. (Eds), Oncologia em Cães e Gatos. Roca, São Paulo. 612p.). Os meningiomas intraespinhais causaram com maior frequência sinais de ataxia proprioceptiva, déficit de propriocepção e paresia/paraplegia. Independentemente do segmento medular afetado, a localização e a extensão da lesão é que determinarão a dificuldade locomotora do animal, podendo variar de monoparesia a tetraplegia (Santos et al. 2012Santos R.P., Fighera R.A., Beckmann D.V., Brum J.S., Ripplinger A., Neto D.P., Baumhardt R. & Mazzanti A. 2012. Neoplasmas envolvendo o sistema nervoso central de cães: 26 casos (2003-2011). Pesq. Vet. Bras. 32(2):153-158. http://dx.doi.org/10.1590/S0100-736X2012000200011.
https://doi.org/10.1590/S0100-736X201200...
, Costa 2009Costa R.C. 2009. Neoplasias do sistema nervoso, p.412-427. In: Daleck R.C., De Nardi A.B. & Rodaski S. (Eds), Oncologia em Cães e Gatos. Roca, São Paulo. 612p., Marcasso et al. 2015Marcasso R.A., Moreira J.R., Valentim L.G., Arias M.V.B. & Bracarense A.P.F.R.L. 2015. Meningiomas em cães: aspectos clínicos, histopatológicos e imuno-histoquímicos. Pesq. Vet. Bras. 35(10):844-852. http://dx.doi.org/10.1590/S0100-736X2015001000005.
https://doi.org/10.1590/S0100-736X201500...
).
Conclusões
Este estudo permitiu estabelecer uma relação entre os três graus histológicos observados em 22 casos de meningiomas em cães com vários parâmetros clínico-epidemiológicos e patológicos, fornecendo informações úteis para um melhor conhecimento da correlação entre a graduação histológica e a evolução clínica desses neoplasmas.
Dentre as principais relações estabelecidas, observou-se que os meningiomas intracranianos e de localização supratentorial foram os mais frequentes; os intracranianos caracterizaram-se principalmente por sinais clínicos de alteração tálamo-cortical; os intraespinhais caracterizaram-se principalmente por causarem ataxia.
Quanto aos meningiomas G-I, o subtipo psamomatoso foi o mais frequente; fêmeas foram mais acometidas (71,4%); a média de idade foi de 11 anos; e um maior tempo de sobrevivência (máximo de um ano) após a manifestação dos sinais clínicos foi observado.
Os G-II tiveram o subtipo cordoide como o mais frequente; somente fêmeas acometidas; a média de idade de 12 anos; e o tempo máximo de sobrevivência de 20 dias.
Os G-III tiveram o subtipo papilar como o mais frequente; um maior número de fêmeas acometidas (60%); uma média de idade de 8 anos; 80% dos cães acometidos da raça Boxer; e o tempo máximo de sobrevivência de 90 dias.
Referências
- Afip 2008. Armed Forces Institute of Pathology. Proceedings of the Wednesday Slide Conference, Silver Spring, MD. Disponível em <Disponível em http://www.askjpc.org/wsco/wsc_showcase2.php?id=192 > Acesso em 14 abr. 2015.
» http://www.askjpc.org/wsco/wsc_showcase2.php?id=192 - Bagley R.S. & Gavin P.R. 1998. Seizures as a complication of brain tumors in dogs. Clin. Tech. Small Anim. Pract. 13(3):179-184. http://dx.doi.org/10.1016/S1096-2867(98)80039-X. PMid:9775508.
» https://doi.org/10.1016/S1096-2867(98)80039-X - Barnhart K.F., Wojcieszyn J. & Storts R.W. 2002. Immunohistochemical staining patterns of canine meningiomas and correlation with published immunophenotypes. Vet. Pathol. 39(3):311-321. http://dx.doi.org/10.1354/vp.39-3-311. PMid:12014495.
» https://doi.org/10.1354/vp.39-3-311 - Barresi V., Caffo M. & Tuccari G. 2016. Classification of human meningiomas: lights, shadows, and future perspectives. J. Neurosci. Res. 94(12):1604-1612. http://dx.doi.org/10.1002/jnr.23801. PMid:27376782.
» https://doi.org/10.1002/jnr.23801 - Cantile C. & Youssef S. 2016. Nervous system, p.251-406. In: Maxie M.G. (Ed.), Jubb, Kennedy and Palmer’s Pathology of Domestic Animals. Vol.1. 6th ed. Saunders Elsevier, Philadelphia. 797p. http://dx.doi.org/10.1016/B978-0-7020-5317-7.00004-7.
» https://doi.org/10.1016/B978-0-7020-5317-7.00004-7 - Costa R.C. 2009. Neoplasias do sistema nervoso, p.412-427. In: Daleck R.C., De Nardi A.B. & Rodaski S. (Eds), Oncologia em Cães e Gatos. Roca, São Paulo. 612p.
- Cullen J.M., Page R. & Misdorp W. 2002. An overview of cancer, pathogenesis, diagnosis, and management, p.3-44. In: Meuten D.J. (Ed.), Tumors in Domestic Animals. 4th ed. Iowa State Press, Iowa. 788p. http://dx.doi.org/10.1002/9780470376928.ch1.
» https://doi.org/10.1002/9780470376928.ch1 - Fighera R.A., Souza T.M., Silva M.C., Brum J.S., Graça D.L., Kommers G.D., Irigoyen L.F. & Barros C.S.L. 2008. Causas de morte e razões para eutanásia de cães. Pesq. Vet. Bras. 28(4):223-230. http://dx.doi.org/10.1590/S0100-736X2008000400005.
» https://doi.org/10.1590/S0100-736X2008000400005 - Flores M.M. 2016. Aspectos epidemiológicos do câncer em cães da região central do rio grande do sul: 50 anos (1964-2013). Tese de Doutorado em Medicina Veterinária, Universidade Federal de Santa Maria, Santa Maria, RS. 90p.
- Geib L.W. 1966. Ossifying meningioma with extracranial metastasis in a dog. Pathol Vet. 3(3):247-254. PMid:6006232.
- José-López R., De la Fuente C., Pumarola M. & Anor S. 2013. Spinal meningiomas in dogs: description of 8 cases including a novel radiological and histopathological presentation. Can. Vet. J. 54(10):948-954. PMid:24155414.
- Josephson G.K.A. & Little P.B. 1990. Four bovine meningeal tumors. Can. Vet. J. 31(10):700-703. PMid:17423678.
- Koestner A. & Higgins R. 2002. Tumors of the nervous system, p.697-738. In: Meuten D.J. (Ed.), Tumors in Domestic Animals. 4th ed. Iowa State Press, Iowa. 788p.
- Koestner A., Bilzer T., Fatzer R., Schulmer F.Y.S., Summer B.A. & Van Winkle T.J. 1999. Histological classification of the tumors of the nervous system of domestic animals. p.25-26. In: Koestner A., Bilzer T., Fatzer R., Schulmer F.Y.S., Summer B.A. & Van Winkle T.J. (Eds), International Histological Classification of the Tumors of Domestic Animals. 2nd Series, Vol.5. Armed Forces Institute of Pathology, Washington, D.C.
- Kreeger J.M., Templer A., Tumquist S.E., Bailey K.L., Johnson P.J. & Wilson D.A. 2002. Paranasal meningioma in a horse. J. Vet. Diagn. Invest. 14(4):322-325. http://dx.doi.org/10.1177/104063870201400408. PMid:12152812.
» https://doi.org/10.1177/104063870201400408 - Long S. 2006. Neoplasia of the Nervous System. Disponível em <Disponível em http://www.ivis.org/advances/Vite/braund26/chapter. asp?LA=1 > Accesso em 14 abr. 2015.
» http://www.ivis.org/advances/Vite/braund26/chapter. asp?LA=1 - Lopes M.B.S. & Vandenberg S.R. 2013. Tumor of the central nervous system, p.1933-2031. In: Fletcher C.D.M. (Ed.), Diagnostic Histopathology of Tumors. Vol.2. 4th ed. Saunders Elsevier, Philadelphia. 2145p.
- Louis D.N., Ohgaki H., Wiestler O.D., Cavenee W.K., Burger P.C., Jouvet A., Scheithauer B.W. & Kleihues P. 2007. The WHO classification of tumours of the central nervous system. Acta Neuropathol. 114(2):97-109. http://dx.doi.org/10.1007/s00401-007-0243-4. PMid:17618441.
» https://doi.org/10.1007/s00401-007-0243-4 - Louis D.N., Perry A., Reifenberger G., von Deimling A., Figarella-Branger D., Cavenee W.K., Ohgaki H., Wiestler O.D., Kleihues P. & Ellison D.W. 2016. The 2016 world health organization classification of tumors of the central nervous system: a summary. Acta Neuropathol. 131(6):803-820. http://dx.doi.org/10.1007/s00401-016-1545-1. PMid:27157931.
» https://doi.org/10.1007/s00401-016-1545-1 - Mandara M.T., Pavone S., Brunetti B. & Mandrioli L. 2010. A comparative study of canine and feline meningioma classification based on the WHO histological classification system in humans. Proc. 22nd Symposium ESVN-ECVN, Bologna, 24-26 September 2009. J. Vet. Intern. Med. 24:235-258.
- Mandara M.T., Reginato A., Foiani G., Baroni M., Poli F., Gasparinetti N. & Bernardini M. 2015. Papillary meningioma in the dog: a clinicopathological case series study. Res. Vet. Sci. 100:213-219. http://dx.doi.org/10.1016/j.rvsc.2015.03.029. PMid:25847284.
» https://doi.org/10.1016/j.rvsc.2015.03.029 - Marcasso R.A., Moreira J.R., Valentim L.G., Arias M.V.B. & Bracarense A.P.F.R.L. 2015. Meningiomas em cães: aspectos clínicos, histopatológicos e imuno-histoquímicos. Pesq. Vet. Bras. 35(10):844-852. http://dx.doi.org/10.1590/S0100-736X2015001000005.
» https://doi.org/10.1590/S0100-736X2015001000005 - Mawrin C. & Perry A. 2010. Pathological classification and molecular genetics of meningiomas. J. Neurooncol. 99(3):379-391. http://dx.doi.org/10.1007/s11060-010-0342-2. PMid:20809251.
» https://doi.org/10.1007/s11060-010-0342-2 - Montoliu P., Anor S., Vidal E. & Pumarola M. 2006. Histological and immunohistochemical study of 30 cases of canine meningioma. J. Comp. Pathol. 135(4):200-207. http://dx.doi.org/10.1016/j.jcpa.2006.06.006. PMid:17049358.
» https://doi.org/10.1016/j.jcpa.2006.06.006 - Motta L., Mandara M.T. & Skerritt G.C. 2012. Canine and feline intracranial meningiomas: an updated review. Vet J. 192(2):153-165. http://dx.doi.org/10.1016/j.tvjl.2011.10.008. PMid:22104505.
» https://doi.org/10.1016/j.tvjl.2011.10.008 - Patnaik A.K., Kay W.J. & Hurvitz A.I. 1986. Intracranial meningioma: a comparative pathologic study of 28 dogs. Vet. Pathol. 23(4):369-373. http://dx.doi.org/10.1177/030098588602300404. PMid:3750730.
» https://doi.org/10.1177/030098588602300404 - Pérez V., Vidal E., González N., Benavides J., Ferreras M.C., Villagrasa M. & Pumarola M. 2005. Orbital meningioma with a granular cell component in a dog, with extracranial metastasis. J. Comp. Pathol. 133(2-3):212-217. http://dx.doi.org/10.1016/j.jcpa.2005.02.003. PMid:16045918.
» https://doi.org/10.1016/j.jcpa.2005.02.003 - Petersen S.A., Sturges B.K., Dickinson P.J., Pollard R.E., Kass P.H., Kent M., Vernau K.M., Lecouteur R.A. & Higgins R.J. 2008. Canine intraspinal meningiomas: imaging features, histopathologic classification, and long-term outcome in 34 dogs. J. Vet. Intern. Med. 22(4):946-953. http://dx.doi.org/10.1111/j.1939-1676.2008.0106.x. PMid:18482277.
» https://doi.org/10.1111/j.1939-1676.2008.0106.x - Pizem J., Velnar T., Prestor B., Mlakar J. & Popovic M. 2014. Brain invasion assessability in meningiomas is related to meningioma size and grade, and can be improved by extensive sampling of the surgically removed meningioma specimen. Clin. Neuropathol. 33(5):354-363. http://dx.doi.org/10.5414/NP300750. PMid:25034703.
» https://doi.org/10.5414/NP300750 - Rissi D.R. 2015. A retrospective study of skull base neoplasia in 42 dogs. J. Vet. Diagn. Invest. 27(6):743-748. http://dx.doi.org/10.1177/1040638715611706. PMid:26462763.
» https://doi.org/10.1177/1040638715611706 - Sade B., Chahlavi A., Krishnaney A., Nagel S., Choi E. & Lee J.H. 2007. World Health Organization Grades II and III meningiomas are rare in the cranial base and spine. Neurosurgery 61(6):1194-1198, discussion 1198. http://dx.doi.org/10.1227/01.neu.0000306097.38141.65. PMid:18162898.
» https://doi.org/10.1227/01.neu.0000306097.38141.65 - Santos R.P., Fighera R.A., Beckmann D.V., Brum J.S., Ripplinger A., Neto D.P., Baumhardt R. & Mazzanti A. 2012. Neoplasmas envolvendo o sistema nervoso central de cães: 26 casos (2003-2011). Pesq. Vet. Bras. 32(2):153-158. http://dx.doi.org/10.1590/S0100-736X2012000200011.
» https://doi.org/10.1590/S0100-736X2012000200011 - Schulman F.Y., Ribas J.L., Carpenter J.L., Sisson A.F. & LeCouteur R.A. 1992. Intracranial meningioma with pulmonary metastasis in three dogs. Vet. Pathol. 29(3):196-202. http://dx.doi.org/10.1177/030098589202900302. PMid:1621330.
» https://doi.org/10.1177/030098589202900302 - Snyder J.M., Shofer F.S., Van Winkle T.J. & Massicotte C. 2006. Canine intracranial primary neoplasia: 173 cases (1986-2003). J. Vet. Intern. Med. 20(3):669-675. PMid:16734106.
- Song R.B., Vite C.H., Bradley C.W. & Cross J.R. 2013. Postmortem evaluation of 435 cases of intracranial neoplasia in dogs and relationship of neoplasm with breed, age, and body weight. J. Vet. Intern. Med. 27(5):1143-1152. http://dx.doi.org/10.1111/jvim.12136. PMid:23865437.
» https://doi.org/10.1111/jvim.12136 - Sturges B.K., Dickinson P.J., Bollen P.D., Koblik P.H., Kass G.D., Kortz K.M., Vernau M.F., Knipe R.A., Lecouteur R.A. & Higgins R.J. 2008. Magnetic resonance imaging and histological classification of intracranial meningiomas in 112 dogs. J. Vet. Intern. Med. 22(3):586-595. http://dx.doi.org/10.1111/j.1939-1676.2008.00042.x. PMid:18466258.
» https://doi.org/10.1111/j.1939-1676.2008.00042.x - Summers B.A., Cummings J.F. & De Lahunta A. 1995. Tumors of the central nervous system, p.351-401. In: Summers B.A., Cummings J.F. & De Lahunta A. (Eds), Veterinary Neuropathology. Mosby, Missouri.
- Troxel M.T., Vite C.H., Massicotte C., McLear R.C., Winkle T.J.V., Glass E.N., Tiches D. & Dayrell-Hart B. 2004. Magnetic resonance imaging features of feline intracranial neoplasia: retrospective analysis of 46 cats. J. Vet. Intern. Med. 18(2):176-189. http://dx.doi.org/10.1111/j.1939-1676.2004.tb00158.x. PMid:15058768.
» https://doi.org/10.1111/j.1939-1676.2004.tb00158.x - Van Winkle T.J., Steinberg H.S., DeCarlo A.J., Dayrell-Hart B., Steinberg S.A., Smith C.A. & Summers B.A. 1994. Myxoid meningiomas of the Rostral Cervical Spinal Cord and Caudal Fossa in four dogs. Vet. Pathol. 31(4):468-471. http://dx.doi.org/10.1177/030098589403100410. PMid:7941237.
» https://doi.org/10.1177/030098589403100410 - Vandevelde R., Higgins R.J. & Oevermannn A. 2012. Neoplasia. p.129-156. In: Vandevelde R., Higgins R.J. & Oevermannn A. (Eds), Veterinary neuropathology essentials of theory and practice. Wiley-Blackwell, West Sussex. 212p.
Datas de Publicação
-
Publicação nesta coleção
Abr 2018
Histórico
-
Recebido
24 Fev 2017 -
Aceito
26 Mar 2017