RESUMO
JUSTIFICATIVA E OBJETIVOS:
O agulhamento seco é uma técnica intervencionista, minimamente invasiva, utilizada no tratamento da dor miofascial. O objetivo deste estudo foi descrever o emprego do agulhamento seco e realizar a análise crítica da literatura sobre os aspectos técnicos de sua utilização por profissionais capacitados da área da saúde.
CONTEÚDO:
Foi realizada uma busca na literatura por livros em inglês, artigos de revisão, estudos clínicos controlados randomizados ou quase-randomizados, encobertos, ou duplamente encobertos e estudos de séries de casos publicados em português ou inglês. Foram utilizadas as seguintes bases de dados: Cochrane, LILACS e Pubmed. Foram selecionados artigos publicados no período de setembro de 1996 a janeiro de 2017, recrutados após a utilização dos seguintes descritores: agulhamento seco versus síndromes da dor miofascial versus síndrome da disfunção da articulação temporomandibular versus pontos-gatilho versus manipulações musculoesqueléticas versus músculo trapézio (superficial back muscles) versus músculo masseter versus músculo temporal versus músculo pterigoideo versus músculo digástrico. Foram excluídos relatos de casos clínicos, estudos abertos “open-label”, estudos em modelos animais e artigos não relacionados ao agulhamento seco. Após o cruzamento dos descritores e aplicação dos critérios de inclusão e exclusão, foram selecionados seis artigos.
CONCLUSÃO:
O diagnóstico da dor miofascial pode se apresentar como uma tarefa difícil, uma vez que ela pode simular diferentes algias do sistema mastigatório, desde uma odontalgia até uma dor neuropática trigeminal. Isso pode ser minimizado com uma adequada anamnese, exame clínico envolvendo palpação muscular, além da própria experiência e treinamento profissional. A desativação dos pontos-gatilho miofasciais deve ser prioridade na abordagem terapêutica da dor miofascial já que é observada melhora significativa da dor local e referida, quando essa é realizada. Apesar de resultados favoráveis em estudos sobre o agulhamento seco no tratamento da dor miofascial, relacionada à disfunção temporomandibular e a região cervical, ainda faltam na literatura pesquisas com elevado nível de evidência que comprovem a eficácia e a eficiência dessa técnica. Essa é uma terapia minimamente invasiva, de baixo custo, segura e apresenta efeitos locais, segmentares, extrassegmentares e placebo. Diante do exposto, pode-se recomendar seu emprego por diferentes profissionais da área da saúde nos casos da dor miofascial.
Descritores:
Agulhamento seco; Disfunção da articulação temporomandibular; Pontos-gatilho miofasciais; Síndrome de dor miofascial
ABSTRACT
BACKGROUND AND OBJECTIVES:
Dry needling is an interventionist, minimally invasive technique, used in the treatment of myofascial pain. The objective of this study was to describe the use of dry needling and to perform a critical literature analysis about the technical aspects of its use by qualified health care professionals.
CONTENTS:
A search in the literature was carried out for books in English, review articles, randomized controlled or quasi-randomized clinical trials, blind or double-blind and published case studies series in Portuguese or in English. The following databases were used: Cochrane, LILACS, and Pubmed. Articles published from September 1996 to January 2017 were selected according to the following keywords: dry needling versus myofascial pain syndrome versus temporomandibular joint dysfunction syndrome) versus trigger points versus musculoskeletal manipulations versus trapezius muscle, superficial back muscles versus masseter muscle versus secular muscle versus pterygoid muscles versus digastric muscle, neck muscles. Reports of clinical cases, “open-label” studies, studies with animal models and articles not related to DN were excluded. After the matching descriptors and the implementation of inclusion and exclusion criteria, we selected six articles.
CONCLUSION:
The diagnosis of myofascial pain can be a difficult task since it can simulate different masticatory system pain, from a toothache to a trigeminal neuropathic pain. This can be minimized with proper history taking, clinical examination involving muscle palpation, as well as the own experience and professional training. The deactivation of myofascial trigger points should be a priority in myofascial pain therapy since there is a significant improvement of local and referred pain when we use this approach. Despite the favorable results of studies about the use of dry needling in myofascial pain treatment related to temporomandibular joint dysfunction and the cervical region, the literature still lacks studies with a high level of evidence proving the effectiveness and efficacy of this technique. This is a minimally invasive, low cost, and safe therapy that provides local, segmental, extra segmental and placebo effects. Therefore, its use should be recommended by different health professionals in cases of myofascial pain.
Keywords:
Dry needling; Myofascial pain syndrome; Myofascial trigger points; Temporomandibular joint dysfunction
INTRODUÇÃO
O agulhamento seco (AS), utilizado para tratamento da dor miofascial (DM), apesar de ser confundido com a acupuntura tradicional chinesa, é uma técnica ocidental baseada em princípios neurofisiológicos distintos. Descrito pela primeira vez por Travell na década de 1960, o AS foi utilizado em maior escala após a publicação dos estudos de Lewits e amplamente difundido na última década11 Unverzagt C, Berglund K, Thomas JJ. Dry needling for myofascial trigger point pain: a clinical commentary. Int J Sports Phys Ther. 2015;10(3):402-18.,22 Butts R, Dunning J, Perreault T, Mourad F, Grubb M. Peripheral and spinal mechanisms of pain and dry needling mediated analgesia: a clinical resource guide for health care professionals. Int J Phys Med Rehabil. 2016;4(2):2-18..
O AS foi desenvolvido originalmente com o objetivo de desativar pontos-gatilho miofasciais (PGM). Esses são caracterizados por um ponto hiperirritável, localizado em uma banda tensa de um músculo, ou fáscia muscular associado à dor local e/ou referida. Estão também associados às manifestações clínicas da DM e fonte de sensibilização periférica e central33 Vulfsons S, Ratmansky M, Kalichman L. Trigger point needling: techniques and outcome. Curr Pain Headache Rep. 2012;16(5):407-12.,44 Dunning J, Butts R, Mourad F, Young I, Flannagan S, Perreault T. Dry needling: a literature review with implications for clinical practice guidelines. Phys Ther Rev. 2014;19(4):252-65..
Além de intimamente ligados à fisiopatologia da DM os PGM estão relacionados à fraqueza muscular, à irritabilidade local, ao desequilíbrio muscular e à incoordenação motora no músculo afetado e nos grupos sinérgicos a ele55 Lucas KR, Rich PA, Polus BI. Muscle activation patterns in the scapular positioning muscles during loaded scapular plane elevation: the effects of latent myofascial trigger points. Clin Biomech. 2010;25(8):765-70.,66 Dommertholt J, Grieve R, Layton M, Hooks T. Myofascial trigger points: an evidence-informed review. J Man Manip Ther. 2006;14(4):203-21..
Wrigth e North77 Wrigth EF, North SL. Management and treatment of temporomandibular disorders: a clinical perspective. J Man Manip Ther. 2009;17(4):247-54. analisaram 190 pacientes com dor temporomandibular para demonstrarem quais músculos mastigatórios e cervicais relacionados à disfunção temporomandibular (DTM) mais afetados e mais capazes de gerar dor referida na região craniofacial. Encontraram uma prevalência do músculo trapézio superior em 60% dos pacientes, o pterigoideo lateral em 50% e o masseter, feixe superficial, em 47%.
Outro estudo epidemiológico, conduzido por Fernández-de-las-Penas et al.88 Fernández-de-las-Penas C, Ge HY, Alonso-Blanco C, González-Inglesias, Arendt-Nielsen L. Referred pain areas of active myofascial trigger points in head, neck, and shoulder muscles, in chronic tension type headache. J Bodyw Mov Ther. 2010;14(4):391-6. investigou o número, a localização e a área de referência da dor de PGM ativo nos músculos trapézio superior, esplênio da cabeça, esternocleidomastoideo, masseter, oblíquo superior, levantador da escápula e suboccipitais em 13 mulheres, com idade entre 30 e 50 anos, com diagnóstico de cefaleia do tipo tensional. Encontrou-se a média de sete pontos-gatilho ativo (PGMA) em cada paciente com a seguinte prevalência de localização: músculos suboccipitais (92%), músculo oblíquo superior (85%), músculo trapézio superior (85%) e músculo masseter (69%). A maior área de referência de dor pelos PGMA foi à região frontal (5,9 cm2), seguida das regiões occipital (4,1 cm2), lateral esquerda (3,3 cm2) e direita (2,8 cm2).
O objetivo deste estudo foi descrever o emprego do AS e realizar a análise crítica da literatura sobre os aspectos técnicos de sua utilização por profissionais capacitados da área da saúde.
MODELOS TEÓRICOS
Nos últimos 30 anos, várias escolas e modelos conceituais foram desenvolvidos em relação ao AS. O modelo dos PGM proposto por Simons, Travell e Simons99 Simons DG, Travell JG, Simons LS. Myofascial pain and dysfunction: the trigger point manual. Baltimore: Willians e Wilkins; 1999;1(2):1-1056. mais utilizado na prática clínica, preconiza que o agulhamento seja realizado diretamente nos PGM ativos e latentes, pois esses são postulados como o fator hegemônico da DM11 Unverzagt C, Berglund K, Thomas JJ. Dry needling for myofascial trigger point pain: a clinical commentary. Int J Sports Phys Ther. 2015;10(3):402-18.. A intenção é que o AS provoque um efeito conhecido como “resposta de contração rápida” (RCR), que se caracteriza por um reflexo espinal, resultante da contração súbita e involuntária das fibras musculares presentes na banda muscular tensa, que contém o PGM99 Simons DG, Travell JG, Simons LS. Myofascial pain and dysfunction: the trigger point manual. Baltimore: Willians e Wilkins; 1999;1(2):1-1056.,1010 Chaitow L, Fritz S. A massage therapist's guide understanding, locating and treating myofascial trigger points. Churchill Livingstone: Elsevier; 2006;9(1):1-192.. Esse efeito é considerado necessário nesse modelo para a eficácia da técnica e, quando atingido indica que a agulha foi inserida corretamente1111 Dommertholt J, Fernandes-de-las-Peñas, C. Trigger point dry needling: an evidenced and clinical-based approach. Churchill Livingstone: Elsevier; 2013;29(1):1-280.,1212 Kalichma L, Vulfsons S. Dry needling in the management of musculoskeletal pain. J Am Board Fam Med. 2010;23(5):640-6..
Gunn1313 Gunn CC. The Gunn approach to the treatment of chronic pain. Churchill Livingstone: 1996;6(2):1-160., um dos pioneiros no uso do AS, propôs a partir de observações empíricas um modelo denominado “Radiculopatia”. Nesse modelo a agulha é inserida na região paraespinal (principalmente nos músculos multífidos) relacionada à musculatura periférica atingida e, na junção musculotendínea dos músculos que contém os PGM. Esse mesmo autor baseou sua técnica no princípio que considera a DM como uma síndrome resultante de uma neuropatia ou radiculopatia periférica. Essa síndrome se caracteriza por alterações neurofisiológicas na região emergente dos nervos espinais, associada às compressões discais, ao estreitamento de forames intervertebrais e às compressões nervosas. Essas alterações podem estar associadas ao comprometimento da função muscular, com consequente aparecimento de PGM em músculos inervados pela raiz atingida66 Dommertholt J, Grieve R, Layton M, Hooks T. Myofascial trigger points: an evidence-informed review. J Man Manip Ther. 2006;14(4):203-21.,1111 Dommertholt J, Fernandes-de-las-Peñas, C. Trigger point dry needling: an evidenced and clinical-based approach. Churchill Livingstone: Elsevier; 2013;29(1):1-280.,1313 Gunn CC. The Gunn approach to the treatment of chronic pain. Churchill Livingstone: 1996;6(2):1-160..
O modelo de sensibilização espinal segmentar foi proposto pelo fisiatra Fischer1414 Fischer AA. Documentation of myofascial trigger points. Arch Phys Med Rehabil. 1988;69(4):286-91.. Nele, o agulhamento é realizado nos ligamentos interespinhosos e supraespinhosos, na musculatura paravertebral e diretamente nos PGM. Segundo esse modelo a sensibilização segmentar resulta de uma hiperativação do corno dorsal medular causada por estímulos nociceptivos oriundos de tecidos lesados. Esse quadro resulta em hipersensibilidade no dermátomo e ativação dolorosa do esclerótomo correspondentes, além da formação de PGM na musculatura relacionada àquele nível espinal33 Vulfsons S, Ratmansky M, Kalichman L. Trigger point needling: techniques and outcome. Curr Pain Headache Rep. 2012;16(5):407-12.,1111 Dommertholt J, Fernandes-de-las-Peñas, C. Trigger point dry needling: an evidenced and clinical-based approach. Churchill Livingstone: Elsevier; 2013;29(1):1-280.,1212 Kalichma L, Vulfsons S. Dry needling in the management of musculoskeletal pain. J Am Board Fam Med. 2010;23(5):640-6.,1515 Baldry P. Management of myofascial trigger point pain. Acupunct Med. 2002;20(1):2-10..
MECANISMOS DE AÇÃO E EFEITOS FISIOLÓGICOS
Os efeitos de diminuição da dor e da tensão muscular, da melhoria da coordenação e do comprimento muscular, além do restabelecimento da mobilidade atribuída ao AS são bastante complexos e estão associados à desinibição dos PGM. Por isso, serão descritos inicialmente a fisiopatologia da formação do ponto-gatilho (PG) e posteriormente os mecanismos que explicam os efeitos dos AS agrupados em locais, segmentares e extrassegmentares, segundo descrições mais atuais da literatura. Esses efeitos se diferenciam conforme a localização, a profundidade e a movimentação da agulha além da presença ou não a RCR.
PONTO-GATILHO MIOFASCIAL
Os PGM podem ser objetivamente observados em exames de ressonância magnética nuclear (RMN), de ultrassonografia (US)11 Unverzagt C, Berglund K, Thomas JJ. Dry needling for myofascial trigger point pain: a clinical commentary. Int J Sports Phys Ther. 2015;10(3):402-18. e de termografia infravermelha (TIN)1616 Skorupska E, Rychlik M, Samborski W. Validation and test-retest reliability of new thermographic technique called thermovison technique of dry needling for gluteus minimums trigger points in sciatica subjects and TrPs-negative healthy volunteers. Biomed Res Int. 2015;2015:546497.,1717 Haddad DS, Brioschi ML, Arita ES. Thermographic and clinical correlation of miofascial trigger points in the masticatory muscles. Dentomaxilofac Radiol. 2012;41(8):621-9.. Os dois primeiros exames são de difícil aplicação na prática clínica pelo alto custo, enquanto que no caso da TIN há falta desse equipamento em serviços especializados e em hospitais. Diante disso, a sua identificação deve ser realizada por meio de palpação manual, ou pelas técnicas de rolamento ou de pinçamento dos músculos afetados, seus sinergistas e seus antagonistas11 Unverzagt C, Berglund K, Thomas JJ. Dry needling for myofascial trigger point pain: a clinical commentary. Int J Sports Phys Ther. 2015;10(3):402-18.,66 Dommertholt J, Grieve R, Layton M, Hooks T. Myofascial trigger points: an evidence-informed review. J Man Manip Ther. 2006;14(4):203-21.. Após a identificação, os PGM podem ser classificados em três subtipos: ativos, latentes e satélites, dos quais os dois primeiros são os mais abordados pela terapia de AS. O PGM ativo é doloroso espontaneamente, produzindo um padrão de dor à distância. O latente caracteriza-se por desencadear dor somente quando estimulado, enquanto o satélite é resultado de PG primários (latente ou ativo) presentes por longos períodos de tempo99 Simons DG, Travell JG, Simons LS. Myofascial pain and dysfunction: the trigger point manual. Baltimore: Willians e Wilkins; 1999;1(2):1-1056.,1515 Baldry P. Management of myofascial trigger point pain. Acupunct Med. 2002;20(1):2-10.,1818 Shah JP, Thaker N, Heimur J, Aredo JV, Sikdar S, Gerber L. Myofascial trigger points then and now: a historical and scientific perspective. PMR. 2015;7(7):746-61..
FISIOPATOLOGIA DO PONTO-GATILHO MIOFASCIAL
Segundo as pesquisas atuais, existem três fatores essenciais envolvidos na formação do PGM: liberação excessiva de acetilcolina, o encurtamento dos sarcômeros e a liberação de substâncias inflamatórias e algogênicas como, por exemplo, a substância P. O aumento de acetilcolina na junção neuromuscular causa elevação da tensão das fibras musculares e, consequentemente, isquemia e hipóxia localizadas que induzem à liberação de substâncias algogênicas (crise energética). Essas substâncias causam maior liberação de acetilcolina completando um ciclo vicioso22 Butts R, Dunning J, Perreault T, Mourad F, Grubb M. Peripheral and spinal mechanisms of pain and dry needling mediated analgesia: a clinical resource guide for health care professionals. Int J Phys Med Rehabil. 2016;4(2):2-18.,1818 Shah JP, Thaker N, Heimur J, Aredo JV, Sikdar S, Gerber L. Myofascial trigger points then and now: a historical and scientific perspective. PMR. 2015;7(7):746-61.,1919 Gerwin RD, Dommerholt J, Shah JP. An expansion of Simons integrated hypothesis of trigger point formation. Curr Pain Headache Rep. 2004;8(6):468-75.. A manutenção dos estímulos nocivos aumenta progressivamente a sensibilização do corno dorsal da medula e neurônios, antes silenciosos, passam também a enviar estímulos ascendentes, ativando sistemas supraespinais que resultam na sensibilização central1818 Shah JP, Thaker N, Heimur J, Aredo JV, Sikdar S, Gerber L. Myofascial trigger points then and now: a historical and scientific perspective. PMR. 2015;7(7):746-61.
19 Gerwin RD, Dommerholt J, Shah JP. An expansion of Simons integrated hypothesis of trigger point formation. Curr Pain Headache Rep. 2004;8(6):468-75.-2020 Cagnie B, Dewitte V, Barbe T, Timmermans F, Delrue N, Meeus M. Physiologic effects of dry needling. Curr Pain Headache Rep. 2013;17(8):348-5..
EFEITOS LOCAIS
A inserção da agulha no PGM lesiona e/ou destrói as placas motoras, com consequente desnervação axônica distal e indução de regeneração fisiológica, que ocorre após 7 a 10 dias. Essa lesão é focal e não causa risco significativo de formação cicatricial66 Dommertholt J, Grieve R, Layton M, Hooks T. Myofascial trigger points: an evidence-informed review. J Man Manip Ther. 2006;14(4):203-21.,1111 Dommertholt J, Fernandes-de-las-Peñas, C. Trigger point dry needling: an evidenced and clinical-based approach. Churchill Livingstone: Elsevier; 2013;29(1):1-280..
A RCR, quando atingida, diminui a ativação elétrica da placa motora afetada (pela diminuição da ação excessiva de acetilcolina), fato observado pela diminuição da atividade elétrica espontânea na zona das bandas tensas2121 Chen JT, Chung KC, Hou CR, Kuan CR, Kuan TS, Chen SM, et al. Inhibitory effect of dry needling on the spontaneous electrical activity recorded form myofascial trigger spots of rabbit skeletal muscle. Am J Phys Med Rehabil. 2001;80(10):729-35..
Outro provável efeito local é o alongamento das estruturas citoesqueléticas, seguido de recuperação do comprimento normal dos sarcômeros devido à diminuição da sobreposição dos filamentos de actina e da miosina66 Dommertholt J, Grieve R, Layton M, Hooks T. Myofascial trigger points: an evidence-informed review. J Man Manip Ther. 2006;14(4):203-21.,2020 Cagnie B, Dewitte V, Barbe T, Timmermans F, Delrue N, Meeus M. Physiologic effects of dry needling. Curr Pain Headache Rep. 2013;17(8):348-5..
A pressão mecânica provocada pela agulha associada à sua rotação, polariza o tecido conjuntivo, que possui a característica intrínseca de pisoeletricidade. Esse estresse mecânico transformado em atividade elétrica parece auxiliar a remodelação tecidual66 Dommertholt J, Grieve R, Layton M, Hooks T. Myofascial trigger points: an evidence-informed review. J Man Manip Ther. 2006;14(4):203-21..
Quando a agulha é inserida, um reflexo axônico é disparado na rede terminal das fibras A delta e fibras C, que está associado à liberação de várias substâncias vasoativas66 Dommertholt J, Grieve R, Layton M, Hooks T. Myofascial trigger points: an evidence-informed review. J Man Manip Ther. 2006;14(4):203-21.,1919 Gerwin RD, Dommerholt J, Shah JP. An expansion of Simons integrated hypothesis of trigger point formation. Curr Pain Headache Rep. 2004;8(6):468-75.,2020 Cagnie B, Dewitte V, Barbe T, Timmermans F, Delrue N, Meeus M. Physiologic effects of dry needling. Curr Pain Headache Rep. 2013;17(8):348-5.. Essas atuam na vasodilatação e no aumento do fluxo sanguíneo local que resulta em redução da concentração das substâncias algogênicas, e diminuição da ativação dos nociceptores culminando na resolução da sensibilização periférica1818 Shah JP, Thaker N, Heimur J, Aredo JV, Sikdar S, Gerber L. Myofascial trigger points then and now: a historical and scientific perspective. PMR. 2015;7(7):746-61.. Além da vasodilatação local, um estudo com a utilização de câmera termográfica demonstrou vasodilatação distal, na região de referência da dor2121 Chen JT, Chung KC, Hou CR, Kuan CR, Kuan TS, Chen SM, et al. Inhibitory effect of dry needling on the spontaneous electrical activity recorded form myofascial trigger spots of rabbit skeletal muscle. Am J Phys Med Rehabil. 2001;80(10):729-35.,2222 Skorupska E, Rychlik M, Samborski W. Intensive vasodilatation in the sciatic pain area after dry needling. BMC Complement Altern Med. 2015;15:72-77..
EFEITOS SEGMENTARES
A inserção da agulha estimula as fibras A delta e A beta presentes nos músculos e na pele, que por sua vez acionam as células intermediárias no corno dorsal da medula espinal, por meio dos terminais colaterais. As células intermediárias liberam a encefalina que bloqueia a transmissão da dor, efeito conhecido como “analgesia segmentar”, o qual leva alguns minutos para se iniciar, mas pode durar por vários dias2323 White A, Cummings M, Fishie J. Introdução à Acupuntura Médica Ocidental. São Paulo: Roca; 2013..
EFEITOS EXTRASSEGMENTARES
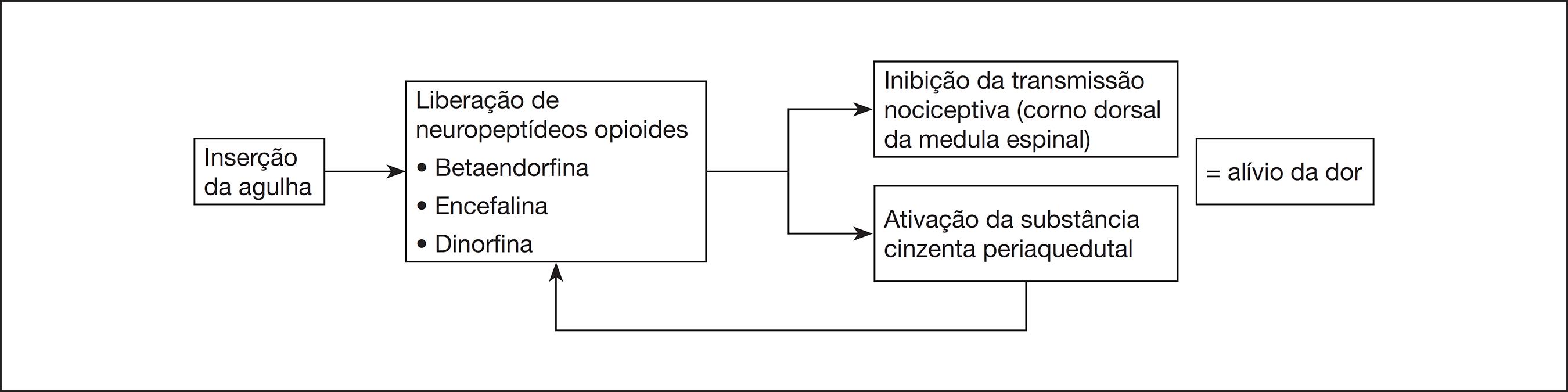
O AS estimula a liberação de neuropeptídios opioides como, por exemplo, betaendorfina, encefalina e dinorfina. Esses opioides são capazes de inibir diretamente a ascendência da transmissão nociceptiva iniciada no corno dorsal medular. A betaendorfina liberada após o agulhamento causa uma supressão na liberação de substância P, inibindo também a transmissão de dor22 Butts R, Dunning J, Perreault T, Mourad F, Grubb M. Peripheral and spinal mechanisms of pain and dry needling mediated analgesia: a clinical resource guide for health care professionals. Int J Phys Med Rehabil. 2016;4(2):2-18.,44 Dunning J, Butts R, Mourad F, Young I, Flannagan S, Perreault T. Dry needling: a literature review with implications for clinical practice guidelines. Phys Ther Rev. 2014;19(4):252-65.. Esses peptídeos também ativam uma área no mesencéfalo, a substância cinzenta periaquedutal (SCP), a partir da qual várias fibras descendem a cada nível da medula espinal até o corno dorsal. A SCP é ativada pela betaendorfina, que é liberada pelas fibras nervosas descendentes do hipotálamo (mais precisamente o núcleo arqueado). O sistema descendente da SCP libera serotonina que estimula as células intermediárias a liberarem encefalina, a qual, por sua vez, inibe as células do corno dorsal espinal, bloqueando a transmissão da dor. Outra via descendente da SCP causa liberação de noradrenalina difusamente em todo corno dorsal, gerando um efeito de bloqueio inibitório pós-sináptico das células de transmissão (Figura 1)2323 White A, Cummings M, Fishie J. Introdução à Acupuntura Médica Ocidental. São Paulo: Roca; 2013..
A estimulação das fibras A delta parece ativar os sistemas inibitórios descendentes mediados por uma relação sinérgica entre a serotonina e a norepinefrina. A norepinefrina possui um efeito inibitório direto sobre a membrana pós-sináptica das células de transmissão22 Butts R, Dunning J, Perreault T, Mourad F, Grubb M. Peripheral and spinal mechanisms of pain and dry needling mediated analgesia: a clinical resource guide for health care professionals. Int J Phys Med Rehabil. 2016;4(2):2-18..
Estudos mais recentes apontam que o AS aumenta o número de opioides via sistema endocanabióide22 Butts R, Dunning J, Perreault T, Mourad F, Grubb M. Peripheral and spinal mechanisms of pain and dry needling mediated analgesia: a clinical resource guide for health care professionals. Int J Phys Med Rehabil. 2016;4(2):2-18.. Esses canabinóides podem inibir a liberação de várias citocinas pró-inflamatórias diminuindo assim, a dor e a inflamação.
EFEITO PLACEBO
A expectativa gerada por procedimentos terapêuticos é capaz de modular a percepção da dor, mecanismo conhecido como “analgesia placebo”1616 Skorupska E, Rychlik M, Samborski W. Validation and test-retest reliability of new thermographic technique called thermovison technique of dry needling for gluteus minimums trigger points in sciatica subjects and TrPs-negative healthy volunteers. Biomed Res Int. 2015;2015:546497.. Exames de neuroimagem demonstram que áreas cerebrais como a substância cinzenta periaquedutal, amígdala, ínsula e tálamo são recrutadas durante a analgesia placebo. Por isso, ressalta-se a consideração desses efeitos ao utilizar a técnica de AS44 Dunning J, Butts R, Mourad F, Young I, Flannagan S, Perreault T. Dry needling: a literature review with implications for clinical practice guidelines. Phys Ther Rev. 2014;19(4):252-65..
TÉCNICA DE APLICAÇÃO
O AS pode ser utilizado com a técnica profunda (ASP) e a superficial (ASS). No ASP a agulha é inserida, através da pele, e se aprofunda em direção ao centro do PGM. Quando o sinal de RCR é provocado, a técnica parece ser mais efetiva, provavelmente pela rápida despolarização das fibras musculares envolvidas, associada à contração reflexa1212 Kalichma L, Vulfsons S. Dry needling in the management of musculoskeletal pain. J Am Board Fam Med. 2010;23(5):640-6..
Um estudo recente22 Butts R, Dunning J, Perreault T, Mourad F, Grubb M. Peripheral and spinal mechanisms of pain and dry needling mediated analgesia: a clinical resource guide for health care professionals. Int J Phys Med Rehabil. 2016;4(2):2-18. de revisão concluiu que a RCR não é um componente crucial no tratamento. O ASP atinge os receptores polimodais das unidades motoras e, estudos sugerem que esses receptores são mais efetivos em induzir analgesia do que os receptores cutâneos1212 Kalichma L, Vulfsons S. Dry needling in the management of musculoskeletal pain. J Am Board Fam Med. 2010;23(5):640-6.,2323 White A, Cummings M, Fishie J. Introdução à Acupuntura Médica Ocidental. São Paulo: Roca; 2013.. Esses receptores respondem a estímulos químicos, térmicos e mecânicos e podem gerar efeitos analgésicos efetivos quando estimulados pelo agulhamento. O ASP está associado à diminuição na ativação das placas motoras terminais envolvidas na redução da dor local e referida, ao aumento da amplitude de movimento e à redução na concentração de substâncias inflamatórias presentes no local do PGM2020 Cagnie B, Dewitte V, Barbe T, Timmermans F, Delrue N, Meeus M. Physiologic effects of dry needling. Curr Pain Headache Rep. 2013;17(8):348-5.,2424 Dommertholt J. Dry needling-peripheral and central considerations. J Man Manip Ther. 2011;19(4):223-7.,2525 Itoh K, Minakawa Y, Kitakoji H. Effect of acupuncture depth on muscle pain. Chin Med. 2011;6(1):1-24..
Este pode ser realizado com diferentes formas de penetração da agulha. Na técnica estacionária, a agulha é inserida no local desejado e mantida sem nenhuma manipulação extra. Na pistonagem, a agulha é inserida e parcialmente retirada, repetidas vezes, no ponto escolhido e ao redor dele. Outra forma de aplicação é realizar rotações da agulha, nos sentidos horário e anti-horário, mantendo-a fixa em um mesmo ponto. Essa rotação parece ativar mais precisamente as fibras C e os mecanorreceptores superficiais e profundos quando comparada à pistonagem22 Butts R, Dunning J, Perreault T, Mourad F, Grubb M. Peripheral and spinal mechanisms of pain and dry needling mediated analgesia: a clinical resource guide for health care professionals. Int J Phys Med Rehabil. 2016;4(2):2-18.. Acredita-se que a pistonagem seja mais efetiva em provocar um relaxamento local das fibras musculares, porém está associada à maior número de efeitos adversos22 Butts R, Dunning J, Perreault T, Mourad F, Grubb M. Peripheral and spinal mechanisms of pain and dry needling mediated analgesia: a clinical resource guide for health care professionals. Int J Phys Med Rehabil. 2016;4(2):2-18.. Já o modo estacionário parece ser mais efetivo como analgesia1212 Kalichma L, Vulfsons S. Dry needling in the management of musculoskeletal pain. J Am Board Fam Med. 2010;23(5):640-6.,2424 Dommertholt J. Dry needling-peripheral and central considerations. J Man Manip Ther. 2011;19(4):223-7.,2626 Srbely JZ, Dickey JP, Lee D, Lowerison M. Dry needling stimulation of myofascial trigger points evokes segmental anti-nociceptive effects. J. Rehabil Med. 2010;42(5):463-8.. Apesar dessas considerações, os estudos não são conclusivos sobre qual abordagem é mais eficaz.
No ASS a agulha é inserida no local do PGM, na camada subcutânea, entre 5mm e 10mm de profundidade, numa angulação entre 20 e 30°. Pode ser mantida fixa no local, ou serem realizados movimentos de rotação da agulha. Por não penetrar no tecido muscular, não é esperada a RCR. O ASS apresenta a vantagem de ser menos doloroso que o ASP, além de ser indicado para aplicação em áreas consideradas de risco como pulmões e grandes vasos. Estudos mostram que o ASS é mais eficaz que o placebo em diminuir quadros dolorosos1212 Kalichma L, Vulfsons S. Dry needling in the management of musculoskeletal pain. J Am Board Fam Med. 2010;23(5):640-6..
O ASP ou ASS podem ser utilizados em músculos situados distalmente em relação ao PGM ativo em um mesmo dermátomo33 Vulfsons S, Ratmansky M, Kalichman L. Trigger point needling: techniques and outcome. Curr Pain Headache Rep. 2012;16(5):407-12.. O efeito analgésico e sedativo alcançado pode ser explicado pelo fenômeno de controle inibitório nocivo difuso. Essa forma de agulhamento pode ser escolhida quando a área principal a ser tratada está muito sensível (hiperalgesia e/ou alodínea).
TEMPO DE APLICAÇÃO E FREQUÊNCIA
Estudos não são conclusivos quanto ao melhor tempo de permanência das agulhas em ambas as técnicas, e nem há consenso em relação à quantidade de sessões necessárias44 Dunning J, Butts R, Mourad F, Young I, Flannagan S, Perreault T. Dry needling: a literature review with implications for clinical practice guidelines. Phys Ther Rev. 2014;19(4):252-65.. Na prática clínica há uma variação de 5 até 30 minutos de duração44 Dunning J, Butts R, Mourad F, Young I, Flannagan S, Perreault T. Dry needling: a literature review with implications for clinical practice guidelines. Phys Ther Rev. 2014;19(4):252-65.. Alguns autores indicam de 2 a 3 sessões para casos agudos e 3 a 5 sessões para casos crônicos11 Unverzagt C, Berglund K, Thomas JJ. Dry needling for myofascial trigger point pain: a clinical commentary. Int J Sports Phys Ther. 2015;10(3):402-18..
CONTRAINDICAÇÕES
As contraindicações absolutas do AS são: fobia à agulha, áreas com linfedema, urgências médicas, histórico de reação anormal a procedimentos anestésicos e estados de inconsciência, ou confusão mental. Já as contraindicações relativas são: terapia com anticoagulante, distúrbios vasculares, epilepsia, alergia ao metal da agulha, gravidez e em crianças11 Unverzagt C, Berglund K, Thomas JJ. Dry needling for myofascial trigger point pain: a clinical commentary. Int J Sports Phys Ther. 2015;10(3):402-18.,1111 Dommertholt J, Fernandes-de-las-Peñas, C. Trigger point dry needling: an evidenced and clinical-based approach. Churchill Livingstone: Elsevier; 2013;29(1):1-280..
CONTEÚDO
Estratégias de busca na literatura
Com a intenção de analisar criticamente as evidências científicas sobre o uso do AS no controle da dor muscular mastigatória e cervical, foi realizada uma busca na literatura por livros em inglês, artigos de revisão, estudos clínicos controlados randomizados ou quase-randomizados, encobertos, ou duplamente encobertos e estudos de séries de casos publicados em português ou inglês. Foram utilizadas as seguintes bases de dados: Cochrane, LILACS e Pubmed. Foram selecionados artigos publicados no período de setembro de 1996 a janeiro de 2017, recrutados após a utilização dos seguintes descritores: agulhamento seco (dry needling) versus síndromes da dor miofascial (myofascial pain syndromes) versus síndrome da disfunção da articulação temporomandibular (temporomandibular joint dysfuction syndrome) versus pontos-gatilho (trigger points) versus manipulações musculoesqueléticas (musculoskeletal manipulations) versus músculo trapézio (trapezius muscle, superficial back muscles) versus músculo masseter (masseter muscle) versus músculo temporal (temporal muscle) versus músculo pterigoideo (pterygoid muscles) versus músculo digástrico (digastric muscle, neck muscles). Foram excluídos relatos de casos clínicos, estudos abertos “open-label”, estudos em modelos animais e artigos não relacionados ao AS.
Após o cruzamento dos descritores e aplicação dos critérios de inclusão e exclusão, foram selecionados seis artigos cujos resultados resumidos estão a seguir:
Agulhamento seco em ponto-gatilho miofascial na região cervical
Ong e Claydon2727 Ong J, Claydon LS. The effect of dry needling for myofascial trigger points in the neck and shoulders: a systematic review and meta-analysis. J Bodyw Mov Ther. 2014;18(3):390-8. em seu estudo de revisão sistemática, com meta-análise, teve como objetivo determinar a eficácia do AS, comparado a outras técnicas (agulhamento com lidocaína e placebo) no tratamento de PGM, na região cervical e do ombro. A escala analógica visual (EAV) foi o instrumento de avaliação escolhido para mensurar a dor desses pacientes. Foi aplicada no início do tratamento, logo após o seu término, 1 e 6 meses após o tratamento. Foram encontrados PGMA no músculo trapézio superior em todos os estudos, mas não houve referência a qual técnica do AS foi aplicada, e se houve aplicação em outros PGMA nas regiões analisadas. Concluíram que o AS é tão efetivo quanto à aplicação de lidocaína nos PGM ativo e destacam as características do primeiro ser minimamente invasivo, de baixo custo e incorrer em menores efeitos adversos do que o anestésico local. Também citaram não haver diferença entre o AS e o placebo.
Ziaeifar et al.2828 Ziaeifar M, Arab AM, Karimi N, Nourbakhsh MR. The effect of dry needling on pain, pressure pain threshold and disability in patients with a myofascial trigger point in the upper trapezius muscle. J Bodyw Mov Ther. 2014;18(2):298-305. conduziram um estudo randomizado, com 33 pacientes, que também apresentavam PGM no músculo trapézio superior. Os pacientes foram divididos em grupo padrão (n=17) e grupo experimental (n=16). O primeiro grupo recebeu a terapia de digito pressão nos PGM e o segundo grupo, agulhamento seco (AS) pela técnica de pistonagem. Foram realizadas 3 sessões em 1 semana de tratamento. A EAV e o algômetro foram utilizados antes e depois de cada procedimento, para a mensuração da intensidade da dor e do limiar de dor à pressão. As medidas foram realizadas novamente 2 dias após o término da 3ª sessão. Os resultados desse estudo sugerem que, tanto a digito pressão como o AS foram eficazes em reduzir a dor e aumentar o limiar de dor à pressão, porém a diferença na medida da EAV no grupo que recebeu o AS foi significativamente maior. Segundo o estudo, esse fato pode ser explicado pelo maior aporte sanguíneo e oxigenação local promovidos pelo AS.
Pecos-Martín et al.2929 Pecos-Martín D, Montanez-Aquilera FJ, Gallego-Izquierdo T, Urraca-Gesto A, Gómez-Conesa A, Romero-Franco N, et al. Effectiveness of dry needling on the lower trapezius in patients with mechanical neck pain: a randomized controlled trial. Arch Phys Med Rehabil. 2015; 96(5):775-81. observaram, em uma pesquisa randomizada com 73 pacientes com dor cervical unilateral, que os pacientes submetidos ao AS sobre o PGM ativo do músculo trapézio inferior, apresentaram redução significativa da intensidade da dor, aumento do limiar de dor à pressão e diminuição do grau de incapacidade quando comparados aos pacientes submetidos ao agulhamento no mesmo músculo só que a uma distância de 1,5cm do PGM ativo.
Agulhamento seco em ponto-gatilho miofascial na musculatura mastigatória
Fernándes-Carnero et al.3030 Fernándes-Carnero J, La Touche R, Ortega-Santiago R, Galan-del-Rio F, Pesquera J, Ge HY, et al. Short-term effects of dry needling of active myofascial trigger points in the masseter muscle in patients with temporomandibular disorders. J Orofac Pain. 2010;24(1):106-12. pesquisaram os efeitos do ASP, comparado ao placebo (falso agulhamento superficial) em 12 pacientes do sexo feminino com DTM, do tipo dor miofascial. O ASP e o placebo foram realizados no PGM ativo do músculo masseter, em 2 sessões com 2 dias de intervalo entre eles. Um algômetro eletrônico foi utilizado para mensuração do limiar de dor à pressão antes da intervenção, 5 minutos depois e 1 semana após. A abertura bucal máxima sem dor foi mensurada da mesma maneira. A técnica utilizada no ASP foi a de pistonagem, realizada no PGM ativo do músculo masseter, até que se obtivessem 5 repostas de contração rápida localizada (RCR). Concluíram que o ASP no masseter foi mais eficaz em aumentar o limiar de dor à pressão e em ganhar amplitude de abertura bucal sem dor, embora o grupo que recebeu o placebo também tenha obtido melhora nessas mensurações.
Outros autores3131 Diraçoglu D, Vural M, Karan A, Aksoy C. Effectiveness of dry needling for the treatment of temporomandibular myofascial pain: a double-blind, randomized, placebo controlled study. J Back Musculoskelet Rehabil. 2012;25(4):285-90., após verificarem que os músculos masseter e temporal anterior são mais comumente afetados na dor miofascial mastigatória, conduziram um estudo randomizado, duplamente encoberto, comparativo entre a técnica de ASP e o agulhamento placebo (Sham) nos PGM ativo desses músculos. Foram incluídos 52 indivíduos (45 mulheres e 7 homens) em idades entre 18 e 57 anos, divididos entre grupo estudo e controle. No grupo-estudo foram realizadas 3 sessões com intervalo de 7 dias cada, onde os PGM ativo receberam o ASP pela técnica de pistonagem. A EAV e a algometria de pressão foram aplicadas imediatamente antes da 1ª intervenção e, novamente uma semana após a última intervenção. Os resultados do estudo apontaram diminuição da dor e, aumento no limiar de dor à pressão em ambos os grupos. Outros estudos já citados também apontaram não haver diferença entre a técnica de AS e o agulhamento Sham (superficial).
Gonzalez-Perez et al.3232 Gonzalez-Perez LM, Infante-Cossio P, Granados-Nunez M, Urresti-Lopez FJ, Lopez-Martos R, Ruiz-Canela-Mendez P. Deep dry needling of trigger points located in the lateral pterygoid muscle: efficacy and safety for treatment for management of myofascial pain and temporomandibular dysfunction. Med Oral Patol Oral Cir Bucal. 2015;20(3):e326-33. realizaram um estudo com 48 pacientes que apresentavam quadro de dor miofascial mastigatória crônica, com envolvimento do músculo pterigoideo lateral. Esse músculo, por ser de difícil acesso para aplicação de outras técnicas como alongamento e massagem profunda, foi selecionado para receber a técnica de AS, por via extraoral no grupo-teste (n=24). Foram realizadas 3 sessões, uma vez por semana, totalizando 3 semanas. O grupo-controle recebeu terapia farmacológica com metocarbamol/paracetamol prescritos a cada 6 horas, por 3 semanas3333 Chou L, Kao MJ, Lin JG. Probable mechanisms of needling therapies for myofascial pain control. Evid Based Complement Alternat Med. 2012;1(1):1-5.. A EAV e as mensurações de amplitude de movimento, como abertura bucal máxima, lateralidade e protrusão da mandíbula, foram mensuradas no início e ao final do tratamento. Os autores concluíram que o AS foi mais eficaz em reduzir a dor, e restaurar a amplitude dos movimentos mensurados do que o grupo tratado farmacologicamente.
CONCLUSÂO
O diagnóstico da dor miofascial pode se apresentar como uma tarefa difícil, uma vez que pode simular diferentes algias do sistema mastigatório, desde uma odontalgia até uma dor neuropática trigeminal. Isso pode ser minimizado frente a uma adequada anamnese, exame clínico envolvendo palpação muscular, além da própria experiência e treinamento profissional. A desativação dos PGM deve ser prioridade na abordagem terapêutica da dor miofascial, já que é observada melhora significativa da dor local e referida, quando essa é realizada. Apesar de resultados favoráveis em estudos sobre o AS no tratamento da dor miofascial relacionada à DTM e à região cervical, ainda faltam na literatura pesquisas com elevado nível de evidência que comprovem a eficácia e a eficiência dessa técnica. Essa é uma terapia minimamente invasiva, de baixo custo, segura e apresenta efeitos locais, segmentares, extrassegmentares e placebo. Diante do exposto, pode-se recomendar seu emprego por diferentes profissionais da área da saúde nos casos da dor miofascial.
-
Fontes de fomento: não há.
REFERENCES
-
1Unverzagt C, Berglund K, Thomas JJ. Dry needling for myofascial trigger point pain: a clinical commentary. Int J Sports Phys Ther. 2015;10(3):402-18.
-
2Butts R, Dunning J, Perreault T, Mourad F, Grubb M. Peripheral and spinal mechanisms of pain and dry needling mediated analgesia: a clinical resource guide for health care professionals. Int J Phys Med Rehabil. 2016;4(2):2-18.
-
3Vulfsons S, Ratmansky M, Kalichman L. Trigger point needling: techniques and outcome. Curr Pain Headache Rep. 2012;16(5):407-12.
-
4Dunning J, Butts R, Mourad F, Young I, Flannagan S, Perreault T. Dry needling: a literature review with implications for clinical practice guidelines. Phys Ther Rev. 2014;19(4):252-65.
-
5Lucas KR, Rich PA, Polus BI. Muscle activation patterns in the scapular positioning muscles during loaded scapular plane elevation: the effects of latent myofascial trigger points. Clin Biomech. 2010;25(8):765-70.
-
6Dommertholt J, Grieve R, Layton M, Hooks T. Myofascial trigger points: an evidence-informed review. J Man Manip Ther. 2006;14(4):203-21.
-
7Wrigth EF, North SL. Management and treatment of temporomandibular disorders: a clinical perspective. J Man Manip Ther. 2009;17(4):247-54.
-
8Fernández-de-las-Penas C, Ge HY, Alonso-Blanco C, González-Inglesias, Arendt-Nielsen L. Referred pain areas of active myofascial trigger points in head, neck, and shoulder muscles, in chronic tension type headache. J Bodyw Mov Ther. 2010;14(4):391-6.
-
9Simons DG, Travell JG, Simons LS. Myofascial pain and dysfunction: the trigger point manual. Baltimore: Willians e Wilkins; 1999;1(2):1-1056.
-
10Chaitow L, Fritz S. A massage therapist's guide understanding, locating and treating myofascial trigger points. Churchill Livingstone: Elsevier; 2006;9(1):1-192.
-
11Dommertholt J, Fernandes-de-las-Peñas, C. Trigger point dry needling: an evidenced and clinical-based approach. Churchill Livingstone: Elsevier; 2013;29(1):1-280.
-
12Kalichma L, Vulfsons S. Dry needling in the management of musculoskeletal pain. J Am Board Fam Med. 2010;23(5):640-6.
-
13Gunn CC. The Gunn approach to the treatment of chronic pain. Churchill Livingstone: 1996;6(2):1-160.
-
14Fischer AA. Documentation of myofascial trigger points. Arch Phys Med Rehabil. 1988;69(4):286-91.
-
15Baldry P. Management of myofascial trigger point pain. Acupunct Med. 2002;20(1):2-10.
-
16Skorupska E, Rychlik M, Samborski W. Validation and test-retest reliability of new thermographic technique called thermovison technique of dry needling for gluteus minimums trigger points in sciatica subjects and TrPs-negative healthy volunteers. Biomed Res Int. 2015;2015:546497.
-
17Haddad DS, Brioschi ML, Arita ES. Thermographic and clinical correlation of miofascial trigger points in the masticatory muscles. Dentomaxilofac Radiol. 2012;41(8):621-9.
-
18Shah JP, Thaker N, Heimur J, Aredo JV, Sikdar S, Gerber L. Myofascial trigger points then and now: a historical and scientific perspective. PMR. 2015;7(7):746-61.
-
19Gerwin RD, Dommerholt J, Shah JP. An expansion of Simons integrated hypothesis of trigger point formation. Curr Pain Headache Rep. 2004;8(6):468-75.
-
20Cagnie B, Dewitte V, Barbe T, Timmermans F, Delrue N, Meeus M. Physiologic effects of dry needling. Curr Pain Headache Rep. 2013;17(8):348-5.
-
21Chen JT, Chung KC, Hou CR, Kuan CR, Kuan TS, Chen SM, et al. Inhibitory effect of dry needling on the spontaneous electrical activity recorded form myofascial trigger spots of rabbit skeletal muscle. Am J Phys Med Rehabil. 2001;80(10):729-35.
-
22Skorupska E, Rychlik M, Samborski W. Intensive vasodilatation in the sciatic pain area after dry needling. BMC Complement Altern Med. 2015;15:72-77.
-
23White A, Cummings M, Fishie J. Introdução à Acupuntura Médica Ocidental. São Paulo: Roca; 2013.
-
24Dommertholt J. Dry needling-peripheral and central considerations. J Man Manip Ther. 2011;19(4):223-7.
-
25Itoh K, Minakawa Y, Kitakoji H. Effect of acupuncture depth on muscle pain. Chin Med. 2011;6(1):1-24.
-
26Srbely JZ, Dickey JP, Lee D, Lowerison M. Dry needling stimulation of myofascial trigger points evokes segmental anti-nociceptive effects. J. Rehabil Med. 2010;42(5):463-8.
-
27Ong J, Claydon LS. The effect of dry needling for myofascial trigger points in the neck and shoulders: a systematic review and meta-analysis. J Bodyw Mov Ther. 2014;18(3):390-8.
-
28Ziaeifar M, Arab AM, Karimi N, Nourbakhsh MR. The effect of dry needling on pain, pressure pain threshold and disability in patients with a myofascial trigger point in the upper trapezius muscle. J Bodyw Mov Ther. 2014;18(2):298-305.
-
29Pecos-Martín D, Montanez-Aquilera FJ, Gallego-Izquierdo T, Urraca-Gesto A, Gómez-Conesa A, Romero-Franco N, et al. Effectiveness of dry needling on the lower trapezius in patients with mechanical neck pain: a randomized controlled trial. Arch Phys Med Rehabil. 2015; 96(5):775-81.
-
30Fernándes-Carnero J, La Touche R, Ortega-Santiago R, Galan-del-Rio F, Pesquera J, Ge HY, et al. Short-term effects of dry needling of active myofascial trigger points in the masseter muscle in patients with temporomandibular disorders. J Orofac Pain. 2010;24(1):106-12.
-
31Diraçoglu D, Vural M, Karan A, Aksoy C. Effectiveness of dry needling for the treatment of temporomandibular myofascial pain: a double-blind, randomized, placebo controlled study. J Back Musculoskelet Rehabil. 2012;25(4):285-90.
-
32Gonzalez-Perez LM, Infante-Cossio P, Granados-Nunez M, Urresti-Lopez FJ, Lopez-Martos R, Ruiz-Canela-Mendez P. Deep dry needling of trigger points located in the lateral pterygoid muscle: efficacy and safety for treatment for management of myofascial pain and temporomandibular dysfunction. Med Oral Patol Oral Cir Bucal. 2015;20(3):e326-33.
-
33Chou L, Kao MJ, Lin JG. Probable mechanisms of needling therapies for myofascial pain control. Evid Based Complement Alternat Med. 2012;1(1):1-5.
Datas de Publicação
-
Publicação nesta coleção
Jul-Sep 2017
Histórico
-
Recebido
20 Abr 2017 -
Aceito
19 Jul 2017