Resumos
Desde o final de 1998, um pequeno bivalve invasor, o "mexilhão dourado", Limnoperna fortunei (Dunker, 1857), oriundo do sudeste asiático, está presente no sul do Brasil. Foi provavelmente transportado, não intencionalmente, através de água de lastro para a Bacia do Guaíba, Rio Grande do Sul, Brasil. Em nosso meio, este molusco vem causando problemas de "macrofouling" com grandes prejuízos econômicos e danos à fauna e flora. As coletas foram qualitativas e quantitativas quinzenais no período de um ano, no lago Guaíba, Praia do Veludo (30°12'35"S, 51°11'68"W), ao sul do município de Porto Alegre. Utilizou-se rede de plâncton com abertura de malha equivalente a 36 mm, filtrando-se a quantidade de 30 litros de água. Descrevem-se brevemente as diferentes fases larvais com parâmetros do comprimento. Primeiramente reconhece-se um estágio ciliado, desenvolvendo-se em trocófora (comprimento de 80 µm a 125 µm) com quatro fases distintas, e valvadas com a larva "D" (120 µm a 150 µm), o veliger de charneira reta (150 µm a 190 µm), o veliger umbonado (190 µm a 220 µm) e o pediveliger (220 µm a 250 µm). Quando pós-larvas ou plantígradas (comprimento em torno de 300 µm), começam a secretar o fio de bisso, permitindo a fixação ao substrato. Constatou-se a presença de larvas durante todos os meses amostrados, com picos nos meses de outubro a dezembro.
Água-doce; América do Sul; invasor; lavar
Since the end of 1998 a small invasive bivalve, the golden mussel Limnoperna fortunei (Dunker, 1857), originating from Southeast Asia, is present in Southern Brazil. It was probably brought not intentionally in ballast water to the Guaíba Basin in Rio Grande do Sul State. In this environment, the golden mussel is causing macrofouling very rapidly with grate financial loss and damages to the native fauna and flora. Quali-quantitative samplings twice a month were performed during one year in the Guaíba lake, at Veludo Beach (30°12'35"S, 51°11'68"W) southward of the municipality of Porto Alegre. Each time, 30 litters of water were filtered through plankton net with a mash opening of 36 mm. The different larval stages with the length parameters were briefly described. Different stages were recognized: five without valves and four valved. The first one recognized as a ciliated stage develops into the trocophora (length from 80 µm to 125 µm) with four distinct stages. The valved stages include: the "D" - shaped (length 120 µm to 150 µm), the straight-hinged veliger (length 150 µm to 190 µm), umbonated-veliger (length 190 µm to 220 µm) and pediveliger (length 220 µm to 250 µm). When pos-larvae or plantigrades (length about 300 µm), they secrete the byssus thread that permit fixation on the subtract. Larvae were present during all the samplings with strong October-December peaks.
Freshwater; invasive; larvae; South-America
Fases larvais do mexilhão dourado Limnoperna fortunei (Dunker) (Mollusca, Bivalvia, Mytilidae) na Bacia do Guaíba, Rio Grande do Sul, Brasil
Larval stages of the golden mussel Limnoperna fortunei (Dunker) (Bivalvia, Mytilidae) in Guaíba Basin, Rio Grande do Sul State, Brazil
Cíntia P. dos SantosI, III; Norma L. WürdigI; Maria C. D. MansurII
ILaboratório de Invertebrados Bentônicos, Universidade Federal do Rio Grande do Sul. Avenida Bento Gonçalves 9500, bloco 4, prédio Zoologia 43435, sala 204, 91501-970 Porto Alegre, Rio Grande do Sul, Brasil. E-mail: wurdignl@ufrgs.br
IIMuseu de Ciências e Tecnologia, Pontifícia Universidade Católica do Rio Grande do Sul. Avenida Ipiranga 6681, 90619-900 Porto Alegre, Rio Grande do Sul, Brasil. E-mail: mcmansur@pucrs.br
IIIPrograma de Pós-Graduação em Ecologia, Universidade Federal do Rio Grande do Sul. Bolsista de Mestrado do CNPq. E-mail: cipinheiro@yahoo.com.br
RESUMO
Desde o final de 1998, um pequeno bivalve invasor, o "mexilhão dourado", Limnoperna fortunei (Dunker, 1857), oriundo do sudeste asiático, está presente no sul do Brasil. Foi provavelmente transportado, não intencionalmente, através de água de lastro para a Bacia do Guaíba, Rio Grande do Sul, Brasil. Em nosso meio, este molusco vem causando problemas de "macrofouling" com grandes prejuízos econômicos e danos à fauna e flora. As coletas foram qualitativas e quantitativas quinzenais no período de um ano, no lago Guaíba, Praia do Veludo (30°12'35"S, 51°11'68"W), ao sul do município de Porto Alegre. Utilizou-se rede de plâncton com abertura de malha equivalente a 36 mm, filtrando-se a quantidade de 30 litros de água. Descrevem-se brevemente as diferentes fases larvais com parâmetros do comprimento. Primeiramente reconhece-se um estágio ciliado, desenvolvendo-se em trocófora (comprimento de 80 µm a 125 µm) com quatro fases distintas, e valvadas com a larva "D" (120 µm a 150 µm), o veliger de charneira reta (150 µm a 190 µm), o veliger umbonado (190 µm a 220 µm) e o pediveliger (220 µm a 250 µm). Quando pós-larvas ou plantígradas (comprimento em torno de 300 µm), começam a secretar o fio de bisso, permitindo a fixação ao substrato. Constatou-se a presença de larvas durante todos os meses amostrados, com picos nos meses de outubro a dezembro.
Palavras chave: Água-doce, América do Sul, invasor, lavar.
ABSTRACT
Since the end of 1998 a small invasive bivalve, the golden mussel Limnoperna fortunei (Dunker, 1857), originating from Southeast Asia, is present in Southern Brazil. It was probably brought not intentionally in ballast water to the Guaíba Basin in Rio Grande do Sul State. In this environment, the golden mussel is causing macrofouling very rapidly with grate financial loss and damages to the native fauna and flora. Quali-quantitative samplings twice a month were performed during one year in the Guaíba lake, at Veludo Beach (30°12'35"S, 51°11'68"W) southward of the municipality of Porto Alegre. Each time, 30 litters of water were filtered through plankton net with a mash opening of 36 mm. The different larval stages with the length parameters were briefly described. Different stages were recognized: five without valves and four valved. The first one recognized as a ciliated stage develops into the trocophora (length from 80 µm to 125 µm) with four distinct stages. The valved stages include: the "D" shaped (length 120 µm to 150 µm), the straight-hinged veliger (length 150 µm to 190 µm), umbonated-veliger (length 190 µm to 220 µm) and pediveliger (length 220 µm to 250 µm). When pos-larvae or plantigrades (length about 300 µm), they secrete the byssus thread that permit fixation on the subtract. Larvae were present during all the samplings with strong October-December peaks.
Key words: Freshwater, invasive, larvae, South-America.
Segundo classificação de NEWELL (1969), o molusco bivalve Limnoperna fortunei (Dunker, 1857) comumente conhecido por mexilhão dourado, pertence à família dos mexilhões marinhos (Mytilidae), ordem Mytiloida e subclasse Pteriomorpha. Originário do sudeste da Ásia, comumente encontrado na Coréia, China, Taiwan e Tailândia, este molusco foi introduzido na Argentina em 1991 e no Japão a partir de 1992 (MAGARA et al. 2001). Assemelha-se a um mexilhão marinho. No entanto, vive somente em água doce ou em águas salobras, com baixíssima salinidade (DARRIGRAN & EZCURRA-DE-DRAGO 2000). Foi coletado no lago Guaíba, Rio Grande do Sul, em fins de 1998, constituindo este o primeiro registro da espécie no Brasil, MANSUR et al. (1999, 2003, 2004a) suspeitaram que sua introdução tenha sido através de água de lastro de navios e mencionaram que após dois anos da invasão do mexilhão dourado no Rio Grande do Sul, foram observadas populações com densidades em torno de 140.000 indivíduos por m2. Citaram também que a espécie vem causando uma série de danos à fauna bentônica nativa e à vegetação ripária, desencadeando a diminuição das mesmas. Prejuízos econômicos, devido ao entupimento de poços de captadoras de água, grades e encanamentos de estações de abastecimento de água e refrigeração de indústrias no entorno do lago, também foram observados pelos mesmos autores (MANSUR et al. 2004a), a partir do segundo ano, após o primeiro registro da espécie no Brasil.
MORTON (1982) foi o primeiro autor a estudar L. fortunei (Dunker, 1857) quanto ao ciclo reprodutivo, com base em populações coletadas em Hong-Kong, concluindo que a espécie é dióica com dois picos reprodutivos anuais.
Os primeiros dados sobre as fases larvais de L. fortunei (Dunker, 1857) constam nos trabalhos de CHOI & SHIN (1985) e CHOI & KIM (1985), correspondentes à populações originárias da Coréia. CHOI & SHIN (1985) descreveram a espécie como gonocorística (dióica), cujo desenvolvimento seria por meio de uma larva muito semelhante à de outras espécies de bivalves marinhos, como segue: após a fecundação do ovo, o embrião passaria por vários estágios de segmentação dos blastômeros e em três horas e trinta minutos atingiria o estágio de trocófora ciliada; após mais cinco a seis horas, transformar-se-ia na larva envolta por uma concha de charneira reta (denominada larva D); esta, após aproximadamente cinco dias, passaria a veliger caracterizado pela presença do véu ou "velum" que possibilita uma atividade intensa de natação e consumo de muitos nutrientes; o último estágio compreenderia uma larva umbonada ou juvenil com um pé bem desenvolvido, pronto para assentar-se e fixar-se ao substrato. CHOI & SHIN (1985) deram grande ênfase ao número de horas que a larva leva para atingir cada estágio, descrevendo detalhadamente a segmentação dos primeiros blastômeros. No entanto, faltam descrições morfológicas da trocófora em si, de suas metamorfoses e das medidas das mesmas. Os autores CHOI & KIM (1985) complementaram o trabalho dos autores citados anteriormente, oferecendo medidas dos estágios larvais e em especial da larva D, separando-se em três tipos: Larva "D" fase inicial (comprimento da concha larval 140 µm), larva D-fase intermediária (167 µm) e larva D-fase final (210 µm).
CATALDO & BOLTOVSKOY (2000), estudando a atividade reprodutiva de populações do mexilhão dourado na Argentina, ilustraram pela primeira vez o veliger das populações locais, citando apenas os nomes das larvas do estágio valvado, "charneira-reta" ("straight hinged"), veliger natante e larva umbonada ou juvenil. Citaram, como base, os trabalhos de CHOI & SHIN (1985) e de CHOI & KIM (1985), sem maiores descrições ou comentários.
Com relação ao ciclo larval de outras espécies de bivalves de água doce, dispõem-se de informações um pouco mais consistentes. Os autores ACKERMAN et al. (1994) ao revisarem a bibliografia sobre as larvas do bivalve Dreissena polymorpha (Pallas, 1771), conhecido popularmente como "mexilhões zebra", comentam terem encontrado vários artigos sobre o tema, com dados que contém diferenças tanto na terminologia como na seqüência de eventos e em relação às medidas. Para resolver o problema, optaram por medir as larvas e redescrevê-las, observando características morfológicas e seu comportamento, o que lhes permitiu determinar o estágio de desenvolvimento de cada fase. Consideraram o comprimento e a altura como essencial para redefinir cada fase larval medindo o tamanho da concha quando presente.
NICHOLS & BLACK (1994) separaram os estágios larvais de várias espécies de água doce pertencentes à ordem Veneroida, como Dreissena polymorpha, Dreissena rosteriformis bugensis Andrusov, 1897 (Dreissenidae) e Corbicula fluminea (Müller, 1774) (Corbiculidae), utilizando características como comprimento da charneira, comprimento, altura e forma da concha, e a presença ou ausência de um pé e/ou de um véu. Apresentaram também um glossário definindo a terminologia das características morfológicas das larvas.
KASYANOV et al. (1998) desenvolveram amplo trabalho sobre larvas de várias espécies marinhas, desde a fase de ovo, e estabeleceram padrões de orientação e medidas das conchas dos moluscos. Segundo os mesmos autores citados acima, o ovo dos bivalves em geral contém relativamente pouco vitelo que se distribui uniformemente no citoplasma da célula ovo; A posição do pólo animal seria indicada pela extrusão dos corpúsculos polares da célula ovo; Os ovos de bivalves apresentam um diâmetro de 40-360 µm, semelhante aos ovos de outros bilateria com fertilização externa, e são envolvidos por uma membrana vitelínica e uma gelatinosa; A espessura dessa membrana vitelínica é de 1-2 µm. Segundo DROZDOV & KASYANOV (1985b), a membrana gelatinosa é geralmente transparente, delicada e pobremente definida após a fixação. KASYANOV et al. (1998) distinguiram, no contorno da concha larval, as margens, anterior, posterior, dorsal e ventral. Para a orientação das larvas valvadas, consideraram na margem anterior do veliger a presença do véu e do músculo adutor anterior, e o véu e o pé na veliconcha. A margem posterior seria onde se desenvolveriam mais tarde os sifões e a margem dorsal, onde as duas valvas se uniriam e se formaria a charneira. A margem oposta à charneira é chamada de margem ventral. Distinguiram também a margem dorsal, anterior ao umbo e a margem dorsal, posterior ao umbo. Ainda segundo KASYANOV et al. (1998) a trocófora quando totalmente envolvida pela concha passa ao estágio valvado, que possui uma estrutura interna que evolui de simples a complexa. O pólo animal da trocófora, ou seja, a prototroca, desenvolve-se em um véu, constituído por um disco coroado de cílios alongados, cujo formato lembra um botão de contorno ovalado, sobressaindo às bordas da concha larval e servindo como estrutura para natação.
Frente à escassez de publicações disponíveis sobre as larvas do mexilhão dourado e de dados que possibilitem o reconhecimento de fases larvais, principalmente as desprovidas de concha, este trabalho têm por objetivo auxiliar o reconhecimento das fases larvais de L. fortunei, como base aos trabalhos de monitoramento e controle dessa espécie invasora na América do Sul.
MATERIAL E MÉTODOS
Foram realizadas coletas quinzenais, no período setembro de 2002 à dezembro de 2003, em uma estação de coleta situada na praia do Veludo (30º12'35"S, 51º11'68"W), Bairro do Belém Novo, junto ao trapiche da Associação dos Pescadores (APESCA), na margem esquerda do lago Guaíba, ao sul do município de Porto Alegre, Rio Grande do Sul (Fig. 1). Para observação de fases que ocorrem logo após a fecundação e que se desenvolvem muito rapidamente, foram realizadas seis coletas adicionais nos meses de outubro a dezembro de 2002 e 2003.
Para coleta das larvas, foi utilizada uma rede de plâncton com abertura de malha equivalente a 36 µm, filtrando-se sempre a quantidade de 30 litros de água.
As diferentes fases larvais foram identificadas, separadas quanto ao tamanho e tipo de concha larval e quantificadas. Cada fase larvas foi definida com base no desenvolvimento da charneira, formato e tamanho da concha e a ausência ou presença de um véu e de um pé. Com o auxílio de microscópio óptico Zeiss standart 25, equipado com câmara clara e ocular milimetrada, grande parte das larvas valvadas foram medidas quanto ao comprimento e altura da concha. Considerou-se comprimento como a medida da maior distância entre a região anterior e a posterior, paralela à linha da charneira, segundo KASYANOV et al. (1998).
As larvas foram fotografadas com vida, em suas diferentes fases, através de uma câmara fotográfica automatizada, acoplada ao microscópio óptico Zeiss Axioplan MC80 em aumentos de 200 vezes. Para diminuir os movimentos das larvas, utilizaram-se alguns filamentos de nicotina (cigarro) que foram colocados uma hora antes da tomada de fotografias, diretamente no líquido da lâmina montada. As amostras foram preservadas em álcool 70% e encontram-se tombadas na coleção de moluscos do Museu de Ciências e Tecnologia da Pontifícia Universidade Católica do Rio Grande do Sul, Porto Alegre.
Foram também observadas e fotografadas póslarvas vivas em fase de fixação sobre a superfície de amostradores colocados no local de coleta. Para obtenção de maior contraste na fotografia (Fig. 11) utilizou-se filtro colorido.
RESULTADOS
Através do material observado foi possível distinguir fases diferenciadas e reconstruir a seqüência de estágios e que estão descritos e representados por meio de ilustrações (Figs 2-10). Compreendem basicamente duas etapas: estágios não valvados e valvados. As medidas com cálculos de comprimento médio das fases valvadas constam na tabela I.
Estágios larvais não valvados: desde o ovo a trocófora. (Figs 2-6).
Ovo: não foi observado. Segundo os autores CHOI & SHIN (1985) este é esférico, compacto, circundado por material viscoso, medindo em torno de 80 µm de diâmetro.
Larva ciliada (Fig. 2): Foi possível distinguir embriões na fase inicial, que considerou-se de mórula ciliada pelo formato circular, cujo diâmetro variou em torno de 80 µm, e devido à presença de cílios esparsos sobre toda a superfície externa.
Este "estágio ciliado" (termo encontrado apenas no trabalho de NICHOLS & BLACK (1994) para D. rosteriformis bugensis) foi observado em abundância nas amostras de outubro e novembro de 2003.
Trocófora fase 1 (Fig. 3): este estágio inicia-se quando o embrião perde o formato circular, tornando-se levemente alongado. Os cílios concentram-se numa extremidade, o polo animal, formando a prototroca, caracterizada por uma coroa de cílios cujo centro apresenta um tufo apical que direciona a locomoção da larva. A trocófora, fase 1, possui um comprimento máximo que varia de 80 µm a 100 µm por 85 µm de largura. Constitui-se numa estrutura compacta de células, sem ser translúcida.
Trocófora fase 2 (Fig. 4): nesta fase a extremidade oral torna-se mais afilada e toda a estrutura da larva toma o formato de pêra, muito semelhante a trocófora de Mactra chinensis Philippi, 1846 (KASYANOV 1998). Ao lado da extremidade oral, abaixo da prototroca, observa-se uma leve reentrância que constitui o protostômio. Este estágio mede em torno 110 µm de comprimento.
Trocófora fase 3 (Fig. 5): a larva aumenta visivelmente de tamanho, atingindo 125 µm de comprimento e aproximadamente 100 µm de largura, torna-se levemente translúcida e o polo aboral, mais deprimido e largo. Surge um pequeno achatamento lateral deste polo, onde mais tarde irá se desenvolver a concha larval.
Este estágio também se assemelha a trocófora de M. chinensis, segundo de KASYANOV (1998).
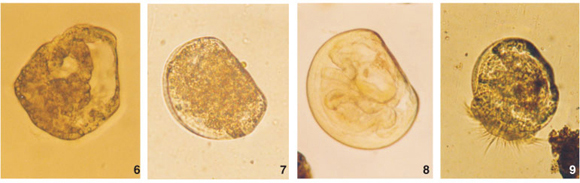
Trocófora fase 4, com primórdios de concha (Fig. 6). A larva se desenvolve sem aumentar de tamanho (125 µm de comprimento), mas muda sua forma devido ao crescimento da concha junto ao pequeno achatamento lateral. Este representa a área da charneira da concha em formação. Distingue-se internamente o intestino rudimentar em fundo cego, que se movimenta esporadicamente, deixando espaços vazios no interior do polo oral.
Estágios larvais valvados: da larva D ao Pediveliger (Figs 7-10). Os quatro estágios podem ser reconhecidos pela forma, pelo tamanho e desenvolvimento da charneira das conchas larvais e pela presença e/ou ausências de algumas estruturas do corpo larval, como o véu e o pé, segundo descrição a seguir:
Larva D (Fig. 7): concha, em forma de D, envolvendo totalmente a larva. A charneira reta e a estrutura interna larval ainda pouco definida. O comprimento variou de 100 µm a 130 µm. Presença de véu ainda em formação ou rudimentar, formado apenas por cílios que mal ultrapassam as bordas da concha. Seria a prototroca ainda não totalmente transformada em véu. (Este, na próxima fase, irá se desenvolver sob a forma de botão e sobressair às bordas da concha larval). Ausência de pé. Fase denominada de "Early D-shaped", com comprimento de 120 µm a 150 µm, segundo CHOI & KIM (1985).
Veliger de charneira reta (Fig. 8): possui concha de contorno mais arredondado, com crescimento das valvas no sentido ventral e os umbos ainda não projetados. Comprimento variando de 140 µm a 180 µm. A charneira apresenta-se reta com leve espessamento interno. Véu presente, bem desenvolvido além das bordas valvares. O véu apresenta um comprimento um pouco maior que a metade do comprimento das valvas. O restante do corpo larval é coberto com concha completamente translúcida, possibilitando a visualização dos órgãos internos. As larvas desta fase são natantes muito ativas e facilmente reconhecidas no plâncton em função de seus movimentos uniformemente circulares. Algumas vezes disparam em movimentos rotatórios rápidos sobre o próprio eixo. Ausência de pé.
Conforme CHOI & KIM (1985), trata-se do estágio "Middle D-shaped", com comprimento larval de 150 µm a 190 µm.
Veliger umbonado (Fig. 9): a concha apresenta umbos centrados distintos, ou seja, levemente elevados, tornando o contorno dorsal das valvas abaulado. O comprimento varia de 190 µm a 230 µm. A charneira apresenta-se mais densa e mais espessa, o véu bem definido e podem ser visualizados rudimentos do pé na parte ventral posterior ao véu. Movimentos e atividade semelhantes à fase anterior.
CHOI & KIM (1985) denominaram este estágio de "late D-shaped", cujo comprimento larval varia de 190 µm a 220 µm.
Pediveliger (Fig. 10): neste estágio a larva alcança seu tamanho máximo que varia de 240 µm a 270 µm, tendo como característica um pé funcional com o qual pode rastejar, enquanto mantém simultaneamente a habilidade de nadar, geralmente em círculos, com auxílio do véu. Conforme CHOI & KIM (1985) esta fase foi denominada "umbonal stage", e o comprimento da concha larval variando de 220 µm a 250 µm.
Estágio de pós-Larva ou Plantígrada (Fig. 11): comprimento em torno de 300 µm, empregando o pé para rastejar e fixando-se ao substrato com o auxílio do bisso. Freqüentemente descolam o bisso, seguem caminhando e logo se fixam novamente ao substrato. Este estágio foi denominado de "Metamorphosing" por CHOI & KIM (1985), que definiram o comprimento pós-larval superando os 250 µm.
Nos juvenis a concha passa gradativamente a uma forma mitilóide alongada, com os umbos direcionados para frente, ou seja, o crescimento torna-se mais reduzido na região anterior e proporcionalmente mais acentuado na região pós-umbonal, tanto em altura como comprimento. Este crescimento diferenciado propicia a formação da concha do adulto cuja região anterior é tão diminuta que se reduz ao limite anterior dos umbos.
DISCUSSÃO
Optou-se por uma nomenclatura dos estágios larvais distintas dos autores CHOI & SHIN (1985) e CHOI & KIM (1985), porém semelhante à de ACKERMAN et al. (1994) e KASIANOV et al. (1998). ACKERMAN et al. (1994) ofereceram a descrição do ciclo completo larval de D. polymorpha comparado ao das larvas descritas de várias espécies, de famílias distintas, de moluscos marinhos. Os autores CHOI & SHIN (1985) e CHOI & KIM (1985) enfocaram o embrião em segmentação e passaram quase que diretamente às larvas veliger, denominadas por eles de larva do tipo "D" (D early, D middle e D late).
As medidas e ilustrações das três fases larvais de L. fortunei ("stright-hinged", veliger e "umbonated") apresentadas segundo CATALDO & BOLTOVSKOY (2000) pela primeira vez para uma população da espécie invasora na América do Sul, não se enquadram nos parâmetros fornecidos por CHOI & KIM (1985) nem nas medidas observados para as fases larvais correspondentes, observadas no material coletado no Guaíba.
NICHOLS & BLACK (1994) observaram maior semelhança anatômica e morfométrica das larvas de L. fortunei com as de Dreissena spp. (D. polymorpha, D. rosteriformis bugensis) provenientes da Europa oriental do que com as larvas de C. fluminea do sudeste asiático. É interessante observar que L. fortunei pertence à ordem Mytiloida, que é distinta da ordem Veneroida da qual fazem parte Dreissena Beneden, 1835 e Corbicula (Mergele von Mühlfeld,1811). Convém esclarecer ainda que D. polymorpha conhecido popularmente como "mexilhão zebra" é bivalve invasor dulcícola, encontrado no hemisfério norte e ainda ausente na América do Sul. Segundo MORTON (1982), a única afinidade entre Dreissena e Limnoperna Rochebrune, 1882 seria apenas funcional, ou seja, os embriões não são incubados no interior das brânquias, mas se desenvolvem no plâncton. Este mesmo autor, ainda chama atenção para o fato de que L. fortunei possui brânquias filamentosas unidas apenas por junções ciliares, o que não lhes permitiria sustentação de ovos, embriões ou incubação marsupial.
Durante os trabalhos de observação das amostras de plâncton do Guaíba, encontrou-se, algumas vezes além das larvas do mexilhão dourado, trocóforas e veliger de Corbicula spp. Trata-se de larvas muito semelhantes, com diferenciações morfológicas inter-específicas muito sutis. A distinção das mesmas muitas vezes só foi possível por meio da aferição e comparação do tamanho das larvas. Os parâmetros de Corbicula são comparativamente maiores, conforme apresentado por NICHOLS & BLACK (1994): larva D com 240 µm, véliger umbonado 280 µm e pediveliger em torno de 500 µm. Além disto, observou-se que no estágio de veliger, Corbicula apresenta um véu mais projetado, circular e de maior diâmetro que o de L. fortunei. Pode-se aqui mencionar que Corbicula spp. constitui um complexo de espécies invasoras de água doce ainda pouco definidas, presentes nas águas do Guaíba desde a década de 70 (MANSUR et al. 2004b), com estágios larvais facilmente confundidos com o de L. fortunei, se não forem utilizados parâmetros métricos na identificação.
Apesar dos escassos estudos sobre a vida larval da espécie L. fortunei, CHOI & SHIN (1985) citaram em seu trabalho que o desenvolvimento larval é semelhante para Limnoperna e Dreissena, porém a diferença entre esses gêneros estaria no período de permanência no plâncton. As larvas de Dreissena viveriam em torno de uma semana, enquanto que o mexilhão dourado permaneceria em torno de um mês. Porém, segundo o trabalho de NEUMANN & JENNER (1992), Dreissena viveria no plâncton entre três a cinco semanas e portanto o período de permanência no plâncton seria semelhante entre as duas espécies. Estudos comparativos sobre a duração das fases larvais no plâncton dos mananciais hídricos invadidos por L. fortunei na América do Sul, não foram ainda desenvolvidos. DARRIGRAN (2002) comenta que o desenvolvimento larval, com uma fase longa no plâncton, favorece a dispersão de Limnoperna e Dreissena, das suas áreas de origem, através da água de lastro. As larvas de ambos gêneros suportam o transporte por longo período, e ao serem descarregadas em áreas com condições adequadas, completariam seu desenvolvimento.
CONSIDERAÇÕES FINAIS
A identificação das formas larvais de L. fortunei é uma etapa básica e imprescindível ao desenvolvimento de estudos sobre a densidade e crescimento do mexilhão dourado. Sabe-se também que é na fase larval que a espécie se dispersa, invadindo novos ambientes, especialmente em áreas onde a água apresenta boa oxigenação, como nos sistemas coletores de água de estações de tratamento, canalizações, bombas de sucção, sistemas de irrigação, refrigeração de indústrias e nos trocadores de calor de unidades hidroelétricas (MANSUR et al. 2003, DARRIGRAN & PASTORINO 1995). O trabalho básico de monitoramento e de qualquer tipo de controle do animal, a ser efetivado em ambientes antrópicos, fundamenta-se no conhecimento da larva. Este possibilitaria também as avaliações prévias de rios e lagos, que estariam na rota de dispersão do mexilhão dourado, facilitando o desenvolvimento de estratégias preventivas, como a instalação de barreiras sanitárias para evitar a contaminação de novos ambientes. Todo planejamento e gestão de bacias hidrográficas deveriam sugerir um sistema constante de monitoramento do mexilhão dourado através do exame periódico do plâncton. Outra contribuição seria a possibilidade de detectar a presença das larvas na água de lastro das embarcações vindas de outros ambientes hídricos, já contaminados pelo molusco, e assim poder oferecer subsídios à implantação de uma gestão da água de lastro e mesmo de áreas portuárias para evitar a contaminação de novos ambientes.
Como uma maneira de reforçar e dar continuidade ao trabalho desenvolvido até o presente, sugere-se ainda um estudo para determinar o tempo de duração das larvas de L. fortunei, no plâncton.
AGRADECIMENTOS
Ao Conselho Nacional de Desenvolvimento Científico e Tecnológico pelas bolsas de mestrado e produtividade em pesquisa (CNPq-132206/2002-1,CNPq-302584/2002-1). Este trabalho é parte da dissertação de mestrado do autor sênior, desenvolvida no Programa de Pós-Graduação em Ecologia, Universidade Federal do Rio Grande do Sul (UFRGS), e financiada pela The Nature Conservancy do Brasil-TNC, doação nº 018/03. Ao Sr. Nei de Souza Antunes presidente da APESCA Associação dos Pescadores do Rio Grande do Sul, por ter permitido a realização dos trabalhos de campo na Sede da Associação e por ter auxiliado em muitas atividades durante a coleta. Aos colegas Felipe Rossoni Cardoso e Bruno Mitidiero Thormann pelo auxílio nos trabalhos de campo. Ao Prof. Dr. Jeter J. Bertoletti Diretor do Museu de Ciências e Tecnologia da Pontifícia Universidade Católica do Rio Grande do Sul pela compreensão e permissão da realização de muitas atividades de pesquisa junto aos laboratórios desse Museu.
Recebido em 06.XII.2004; aceito em 16.VIII.2005.
- ACKERMAN, J.D.; B. SIM; S.J. NICHOLS & R. CLAUDI. 1994. A review of the early life history of zebra mussels (Dreissena polymorpha): comparisons with marine bivalves. Canadian Journal of Zoology, Ottawa, 72: 1169-1179.
- CATALDO, D.H. & D. BOLTOVSKOY. 2000. Yearly reproductive activity of Limnoperna fortunei (Bivalvia) as inferred from the occurrence of its larvae in the plankton of the lower Paraná river and the Rio de la Plata estuary (Argentina). Aquactic Ecology, Dordrecht, 34: 307-317.
- CHOI, S.S. & J.S. KIM. 1985. Studies on the metamorphosis and the growth of larva in Limnoperna fortunei. Korean Journal of Limnology, Seoul, 1: 13-18.
- CHOI, S.S. & C.N. SHIN. 1985. Study on the early development and larvae of Limnoperna fortunei Korean Journal of Limnology, Seoul, 1: 5 -12.
- DARRIGRAN, G. 2002. Potential impact of filter-feeding invaders on temperate inland fresh water environments. Biological Invasions, Knoxville, 4: 145-156.
- DARRIGRAN, G. & I. EZCURRA DE DRAGO. 2000. Distribucion el Limnoperna fortunei (Dunker, 1857) (Mytilidae), en la cuenca del Plata. Region Neotropical. Medio Ambiente, Buenos Aires, 13 (2): 75-79.
- DARRIGRAN, G.& G. PASTORINO. 1995. The recent introduction of a freshwater asiatic bivalve Limnoperna fortunei (Mytilidae) into South America. The Veliger, Berkeley, 32 (2): 171-175.
- DROZDOV, A.L. & V.A. KASYANOV. 1985. Razmery i forma gamet u morskikh dvustvorchatykh mollyuskov (Shape and size of gametes of marine bivalves). Biologiya Morya, Moscow, 4: 33-40.
- KASYANOV, V.L.; G.A. KRYUCHKOVA; V.A. KULIKOVA & L.A. MEDVEDEVA. 1998. Larvae of marine bivalves and equinoderms. Washington, Smithsonian Institution Libraries, V+288p.
- MAGARA, Y.; Y. MATSUI; Y. GOTO & A. YUASA. 2001. Invasion of the non-indigenous nuisance mussel, Limnoperna fortunei, into water supply facilities in Japan. Journal of Water Supply: Research and Tecnology, London, 50 (3):113-124.
- MANSUR, M.C.D.; L.M.Z. RICHINITTI & C.P. DOS SANTOS. 1999. Limnoperna fortunei (Dunker, 1857) molusco bivalve invasor na Bacia do Guaíba, Rio Grande do Sul, Brasil. Biociências, Porto Alegre, 7 (2): 147-149.
- MANSUR, M.C.D.; C.P. DOS SANTOS; G. DARRIGRAN; I. HEYDRICH; C.T. CALLIL & F.R. CARDOSO. 2003. Primeiros dados quali-quantitativos do mexilhão dourado, Limnoperna fortunei (Dunker, 1857), no Delta do Jacuí, no Lago Guaíba e na Laguna do Patos, Rio Grande do Sul, Brasil e alguns aspectos de sua invasão no novo ambiente. Revista Brasileira de Zoologia, Curitiba, 20 (1): 75-84.
- MANSUR, M.C.D.; C.B. QUEVEDO; C.P. SANTOS; C.T. CALLIL. 2004a. Prováveis vias da introdução de Limnoperna fortunei (Dunker, 1857) (Mollusca, Bivalvia, Mytilidae) na bacia da laguna dos Patos, Rio Grande do Sul e novos registros de invasão no Brasil pelas bacias do Paraná e Paraguai, p. 33-38. In: J.S.V. Silva & R.C.C.L. Souza (Eds). Água de lastro e Bioinvasão. Rio de Janeiro, Interciências, XVIII+224p.
- MANSUR, M.C.D.; C.T. CALLIL; F.R. CARDOSO & J.A.A. IBARRA. 2004b. Uma retrospectiva e mapeamento da invasão de espécies de Corbicula (Mollusca, Bivalvia, Veneroida, Corbiculidae) oriundas do sudeste asiático, na América do Sul, p. 39-58. In: J.S.V. Silva & R.C.C.L. Souza (Eds). Água de lastro e Bioinvasão. Rio de Janeiro, Interciências, XVIII+224p.
- MORTON, B.S. 1982. The reproductive cycle of Limnoperna fortunei (Dunker, 1857) (Bivalvia: Mytilidae) fouling Hong Kong's raw watter supply system. Oceanologia et Limnologia Sinica, Hong Kong, 13: 312-325.
- NEWELL, N.D. 1969. Classification of Bivalvia, p. 205-223. In: R. MOORE. (Ed.). Treatise on Invertebrate Paleontology. Lawrence, University of Kansas, Part N, vol. 1, XXXVIII+489.
- NEUMANN, D. & H.A. JENNER. 1992. Studies on the Ecology and Ecotoxicology of the zebra mussel Dreissena polymorpha, p. 1-4. In: D. NEUMANN & H.A. JENNER (Eds). Limnologie aktuell. Stuttgart, Gustav Fischer Verlag, vol. 4, X+262.
- NICHOLS, S.J. & M.G. BLACK. 1994. Identification of larvae: the zebra mussel (Dreissena polymorpha), quagga mussel (Dreissena rosteriformes bugensis), and Asiam clam (Corbicula fluminea). Canadian Journal of Zoology, Ottawa, 72: 406-416.
Datas de Publicação
-
Publicação nesta coleção
31 Out 2005 -
Data do Fascículo
Set 2005
Histórico
-
Aceito
16 Ago 2005 -
Recebido
06 Dez 2004