DIRETRIZES EM FOCO
Hirsutismo: diagnóstico
Autoria: Sociedade Brasileira de Endocrinologia e Metabologia Sociedade Brasileira de Dermatologia
Elaboração Final: 23 de junho de 2006
Participante: Poli Mara Spritzer
Descrição do método de coleta de evidência: Revisão da literatura.
Graus de recomendação e força de evidência:
A: Estudos experimentais ou observacionais de melhor consistência.
B: Estudos experimentais ou observacionais de menor consistência.
C: Relatos de casos (estudos não controlados).
D: Opinião desprovida de avaliação crítica, baseada em consensos, estudos fisiológicos ou modelos animais.
Objetivo: Descrever as apresentações clínicas das doenças associadas com hirsutismo, sua prevalência, bem como as estratégias reconhecidas para a abordagem diagnóstica.
Conflito de interesse: Nenhum conflito de interesse declarado.
Introdução
O hirsutismo é definido como a presença de pêlos terminais na mulher, em áreas anatômicas características de distribuição masculina. Pode manifestar-se como queixa isolada, ou como parte de um quadro clínico mais amplo, acompanhado de outros sinais de hiperandrogenismo, virilização, distúrbios menstruais e/ou infertilidade.
Crescimento normal dos pêlos corporais, hipertricose e hirsutismo
A maior parte dos pêlos corporais pode ser classificada como velus ou terminal. Os pêlos velus são finos e não-pigmentados. Os pêlos terminais são mais grossos e escuros e podem ser dependentes de hormônios sexuais, como os pêlos da região torácica e abdominal dos homens, ou não, como os cílios e sobrancelhas.Os androgênios promovem a conversão dos pêlos velus em terminais, na maioria das regiões dependentes de hormônios sexuais. Uma exceção é a região do escalpo, onde por ação de androgênios ocorre a involução do folículo piloso1(D).
A diferenciação entre hipertricose e hirsutismo é importante, pois decorrem de etiologias diferentes e o manejo clínico será também diferenciado. A hipertricose é a transformação de pêlos velus, de textura fina e distribuídos em todo o corpo, em pêlos terminais. Não é causada por um aumento na produção de androgênios, podendo ser congênita ou adquirida. A hipertricose adquirida pode ser ocasionada por ingestão de medicamentos, algumas doenças metabólicas, como hipotireoidismo e porfirias, ou doenças nutricionais, como anorexia, desnutrição ou síndromes de má absorção2(D).
O hirsutismo é definido como a presença de pêlos terminais na mulher, em áreas anatômicas características de distribuição masculina, como acima dos lábios, no mento, em torno dos mamilos e ao longo da linha alba em abdome inferior. De acordo com a etiologia, o hirsutismo pode manifestar-se como queixa isolada ou acompanhado de outros sinais de hiperandrogenismo (acne, seborréia, alopécia), virilização (hipertrofia do clitóris, aumento da massa muscular, modificação do tom de voz), distúrbios menstruais e/ou infertilidade ou ainda alterações metabólicas.
O hirsutismo decorre da ação dos androgênios circulantes sobre a pele. Esta ação ocorre devido à presença e atividade de enzimas capazes de disponibilizar ou não metabólitos androgênicos mais ativos no interior do folículo pilo-sebáceo3(B)4 (C)5(D).
Etiologia Do Hirsutismo E Quadro Clínico
O hirsutismo pode ser classificado em três categorias: a) excesso de androgênios produzido pelos ovários e/ou adrenais, b) aumento na sensibilidade cutânea aos androgênios circulantes ou c) outras situações que envolvam alterações secundárias no transporte e/ou metabolismo de androgênios. No primeiro caso, estão agrupados a Síndrome dos ovários policísticos (SOP), a hiperplasia adrenal congênita forma não clássica ou de início tardio, a Síndrome de Cushing e os tumores produtores de androgênios ovarianos ou adrenais. O segundo grupo, corresponde ao hirsutismo dito "idiopático", caracterizado por hirsutismo isolado, na presença de ciclos menstruais regulares e ovulatórios.
No terceiro grupo, outras situações como doenças da tireOide, hiperprolactinemia, uso de drogas (fenotiazinas, danazol, metirapona, ciclosporina, entre outras), podem levar secundariamente a um quadro de hirsutismo6(D).
SOP é a causa mais frequente de hirsutismo de origem glandular. A prevalência em mulheres em idade reprodutiva varia de 4% a 8% para a população geral de mulheres7(B)8,9(C ). O quadro clínico associa hirsutismo, oligo/amenorréia e infertilidade. Os sintomas iniciam no período peripuberal e progridem com o tempo. Um número expressivo de pacientes apresenta obesidade e em 30% a 60% dos casos, em especial nas pacientes obesas, a resistência insulínica com hiperinsulinemia compensatória estará presente10,11(B)12(C). Estas pacientes apresentam maior risco para desenvolver tolerância diminuída à glicose e diabetes mellitus10(B)13(C ). Outras manifestações dermatológicas como acne e alopecia são observadas, em um número menor de pacientes14(C). Embora a etiopatogenia da SOP não tenha sido ainda esclarecida, a ocorrência de um padrão familiar sugere um componente genético da doença, possivelmente de herança autossômica dominante15(B).
Os tumores ovarianos secretores de androgênios são relativamente raros, mas devem ser sempre lembrados como causa de hirsutismo, com início recente e progressão rápida com virilização importante. Entre as neoplasias de ovários, devem ser destacados os arrenoblastomas, androblastomas (tumor de células Sertoli-Leydig), tumores de células da teca-granulosa, tumores de células hilares, disgerminomas, teratomas, gonadoblastomas, tecomas luteinizados e luteomas.
A hiperplasia adrenal congênita forma não clássica (HAC-NC) por deficiência da 21-hidroxilase (CYP21) é a causa mais frequente de hirsutismo de origem adrenal, embora sua prevalência, entre mulheres hirsutas como um todo, seja relativamente baixa, variando entre 2% e 10% das pacientes consultando por hirsutismo16,17(C )18(D) No sul do Brasil, a frequência observada foi de 7,4%6(D). A apresentação clínica é variável, incluindo acne, hirsutismo, alopecia androgênica, distúrbio menstrual e anovulação crônica. Alguns casos podem se apresentar como hirsutismo isolado na presença de ciclos regulares. Em geral, o início é peripuberal, mas pode ocorrer mais cedo, como um quadro de pubarca precoce19,20(C).
Ainda em relação às causas de hirsutismo de origem adrenal, deve-se lembrar a síndrome de Cushing, especialmente em pacientes que apresentam obesidade central, estrias purpúreas, hipertensão e diabete. Por outro lado, os tumores virilizantes adrenais são raros, mas graves e o quadro clínico tem início abrupto e progressão rápida.
O hirsutismo idiopático caracteriza-se por maior atividade androgênica no folículo pilosebáceo dos hormônios circulantes em níveis normais, sem outras manifestações clínicas ou alterações laboratoriais21(B)22(D).
Deve ser realizada anamnese e exame físico completos. Pesquisar início e evolução do hirsutismo e sintomas associados (acne, seborréia, alopecia). Determinar data da menarca, padrão menstrual, paridade e antecedentes familiares, incluindo história familiar de diabete. Deve ser igualmente pesquisada a presença de sintomas sugestivos de disfunção tireoideana ou adrenal ou hipoestrogenismo.
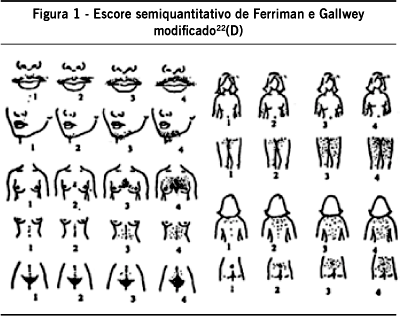
O exame físico deve incluir, entre outros, o índice de massa corporal (IMC: peso/altura2) e a relação cintura/quadril, que permitem de forma simplificada, avaliar pacientes com maior risco metabólico (IMC >25:sobrepeso e >30:obesidade; relação cintura/quadril em mulheres > 0,85); a avaliação da presença de pêlos corporais, sua distribuição corporal, pigmentação e os sinais habituais que podem acompanhar o hirsutismo: acne e seborréia e, eventualmente, alopecia. Sugere-se a utilização de uma classificação semiquantitativa do grau de hirsutismo, escore de Ferriman e Gallwey, para avaliação inicial e evolução clínica23(C). Este escore é definido pela soma da pontuação de nove áreas do corpo (de zero a quatro pontos, cada uma). O ponto de corte para definir hirsutismo é 8 - apenas 5% das mulheres pré-menopáusicas apresenta escore superior a este valor22(D) (Figura 1).
Devem ser pesquisados outros sinais de virilização como: hipertrofia de clitóris, aumento da massa muscular e modificação do tom de voz. Outros aspectos importantes a serem avaliados no exame físico incluem: presença ou não de galactorréia e sinais de distúrbio na função tireoideana ou adrenal. Os exames laboratoriais e de imagem serão solicitados de acordo com as hipóteses diagnósticas apoiadas pela avaliação clínica.
Em termos gerais, serão solicitados: testosterona e prolactina séricas e a determinação da 17 hidroxi-progesterona basal e/ou após o estímulo com ACTH (teste descrito mais adiante). Em pacientes com hirsutismo isolado e ciclos regulares (ciclos menstruais de 25-35 d), a avaliação laboratorial pode ser desnecessária, a não ser que haja infertilidade inexplicada associada. Se houver suspeita de hipoestrogenismo, especialmente nos casos com amenorréia ou sintomas menopáusicos, deve-se solicitar o FSH. Nos casos de SOP, rastrear dislipidemia, diabete e tolerância diminuída à glicose por meio da glicemia em jejum e 2 h após sobrecarga com 75 g de glicose oral e perfil lipídico. Se houver suspeita clínica para tumores secretores de androgênios, exames de imagem serão solicitados para localização da lesão ovariana ou adrenal. Nestes casos, a determinação de DHEA-S pode ser útil. Exames de função tireoide (TSH) ou rastreamento para Síndrome de Cushing serão solicitados apenas em casos específicos.
Critérios para o diagnóstico etiológico sop
Os critérios diagnósticos foram redefinidos recentemente, no consenso de Rotterdam, em reunião conjunta das Sociedades Europeia e Americana de Reprodução Humana. Estes incluem, pelo menos, 2 dos 3 critérios seguintes: 1) disfunção ovulatória; 2) evidência de hiperandrogenismo clínico (sinais e sintomas) ou laboratorial (concentrações aumentadas de androgênios séricos); 3) aparência policística dos ovários à ultrassonografia, ou seja, 12 ou + foliculos 2-9 mm e/ou volume ovariano> 10 cm3. Outras causas reconhecidas de hiperandrogenismo devem ter sido excluídas24(D).
Hirsutismo idiopático
O diagnóstico é estabelecido em pacientes com hirsutismo isolado, com ciclos menstruais regulares, ovulatórios e fertilidade preservada25(C)22(D ).
Nestas pacientes, se solicitados, os níveis de androgênios circulantes são normais.
Hiperplasia adrenal congênita, forma não clássica (hac-nc)
O diagnóstico clínico de HAC-NC por deficiência em 21-hidroxilase é confirmado pela medida da 17-hidroxiprogesterona sérica basal (valores >5 ng/ml) e/ou após teste de estímulo com corticotrofina, em solução aquosa (0,25 mg, IM ou EV), iniciando entre 7 e 9 h da manhã e dosagem da 17OHP e cortisol nos tempos 0 e 60 min, se a administração de cortrosina foi IM ou 0, 30 e 60 min, se EV. Valores plasmáticos de 17OHP pós ACTH > 10-12 ng/ml são diagnósticos de HAC-NC17(C)16,18(D ). Por outro lado, estudos recentes sugerem que o ponto de corte para o teste do ACTH possa ser mais elevado (17,0 ng/ml)26(D). A confirmação do diagnóstico pode ser desnecessária em alguns casos de hirsutismo isolado, uma vez que a resposta terapêutica ao tratamento antiandrogênico é semelhante ao de pacientes com hirsutismo idiopático27(A). No entanto, em mulheres com irregularidade menstrual ou infertilidade, o diagnóstico de hiperplasia adrenal ou sua exclusão tem impacto positivo sobre a decisão da melhor opção terapêutica.
Outras causas
Causas mais raras de hirsutismo devem ser suspeitadas na presença dos seguintes critérios: início abrupto e evolução rápida do hirsutismo ou piora repentina; início mais tardio, após a terceira década de vida; presença de sinais ou sintomas de virilização, incluindo clitoromegalia, aumento de massa muscular e engrossamento da voz. No caso de tumores secretores de androgênios, a testosterona sérica costuma ser > 150 ng/dl e os exames de imagem serão necessários para localizar a origem adrenal ou ovariana do tumor28,29(C). O sulfato de dehidroepiandrosterona poderá estar elevado na presença de neoplasia adrenal. Se houver suspeita clínica para síndrome de Cushing (estrias purpúreas, fascies em lua-cheia, obesidade central, diabete, hipertensão), rastreamento inicial pode ser realizado a partir da determinação da cortisolúria de 24 h (e creatininúria) e/ou teste de supressão com 1 mg VO de dexametasona (às 23 h, e dosagem de cortisol no dia seguinte, às 8 h da manhã). Todos estes casos devem ser encaminhados para serviços de atenção terciária com presteza.
É necessário, também, realizar o diagnóstico diferencial do hirsutismo com outras causas, como distúrbios da função tireóide, hiperprolactinemia e uso de drogas.
O texto completo da Diretriz: Hirsutismo: Diagnóstico está disponível nos sites: www.projetodiretrizes.org.br e www.amb.org.br.
- 1. Thornton MJ, Laing I, Hamada K, Messenger AG, Randall VA. Differences in testosterone metabolism by beard and scalp hair follicle dermal papilla cells. Clin Endocrinol 1993;39:633-9.
- 2. Wendelin DS, Pope DN, Mallory SB. Hypertrichosis. J Am Acad Dermatol 2003;48:161-81.
- 3. Oliveira IO, Lhullier C, Brum IS, Spritzer PM. Gene expression of type 2 17 betahydroxysteroid dehydrogenase in scalp hairs of hirsute women. Steroids 2003;68:641-9.
- 4. Mowszowicz I, Melanitou E, Doukani A, Wright F, Kuttenn F, Mauvais-Jarvis P. Androgen binding capacity and 5 alphareductase activity in pubic skin fibroblasts from hirsute patients. J Clin Endocrinol Metab 1983;56:1209-13.
- 5. Serafini P, Lobo RA. Increased 5 alphareductase activity in idiopathic hirsutism. Fertil Steril 1985;43:74-8.
- 6. Spritzer PM. Revisitando o hirsutismo. Arq Bras Endocrinol Metab 2002;46:127-36.
- 7. Diamanti-Kandarakis E, Kouli CR, Bergiele AT, Filandra FA, Tsianateli TC, Spina GG, et al. A sur vey of the polycystic ovary syndrome in the Greek island of Lesbos: hormonal and metabolic profile. J Clin Endocrinol Metab 1999;84:4006-11.
- 8. Asuncion M, Calvo RM, San Millan JL, Sancho J, Avila S, Escobar-Morreale HF. A prospective study of the prevalence of the polycystic ovary syndrome in unselected Caucasian women from Spain. J Clin Endocrinol Metab 2000;85:2434-8.
- 9. Azziz R, Woods KS, Reyna R, Key TJ, Knochenhauer ES, Yildiz BO. The prevalence and features of the polycystic ovary syndrome in an unselected population. J Clin Endocrinol Metab 2004;89:2745-9.
- 10. Dunaif A, Graf M, Mandeli J, Laumas V, Dobrjansky A. Characterization of groups of hyperandrogenic women with acanthosis nigricans, impaired glucose tolerance and/or hyperinsulinemia. J Clin Endocrinol Metab 1987;65:499-507.
- 11. Nestler JE, Jakubowicz DJ. Decreases in ovarian cytochrome P450c17 alfa activity and serum free testosterone after reduction of insulin secretion in Polycystic Ovary Syndrome. N Engl J Med 1996;335:617-23.
- 12. Morales AJ, Laughlin GA, Butzow T, Maheshwari H, Baumann G, Yen SS. Insulin, somatotropic, and luteinizing hormone axes in lean and obese women with polycystic ovary syndrome: common and distinct features. J Clin Endocrinol Metab 1996;81:2854-64.
- 13. Ehrmann DA, Barnes RB, Rosenfield RL, Cavaghan MK, Imperial J. Prevalence of impaired glucose tolerance and diabetes in women with polycystic ovary syndrome. Diabetes Care 1999;22:141-6.
- 14. Conway GS, Honour JW, Jacobs HS. Heterogeneity of the polycystic ovary syndrome: clinical, endocrine and ultrasound features in 556 patients. Clin Endocrinol 1989;30:459-70.
- 15. Govind A, Obhrai MS, Clayton RN. Polycystic ovaries are inherited as an autosomal dominant trait: analysis of 29 polycystic ovary syndrome and 10 control families. J Clin Endocrinol Metab 1999;84:38-43.
- 16. Kuttenn F, Couillin P, Girard F, Billaud L, Vincens M, Boucekkine C, et al. Lateonset adrenal hyperplasia in hirsutism. N Engl J Med 1985;313:224-31.
- 17. Azziz R, Zacur HA. 21-Hydroxylase deficiency in female hyperandrogenism: screening and diagnosis. J Clin Endocrinol Metab 1989;69:577-84.
- 18. New MI, Lorenzen F, Lerner AJ, Kohn B, Oberfield SE, Pollack MS, et al. Genotyping steroid 21-hydroxylase deficiency: hormonal reference data. J Clin Endocrin Metab 1983;57:320-6.
- 19. Temeck JW, Pang SY, Nelson C, New MI. Genetic defects of steroidogenesis in premature pubarche. J Clin Endocrinol Metab 1987;64:609-17.
- 20. Siegel SF, Finegold DN, Urban MD, McVie R, Lee PA. Premature pubarche: etiological heterogeneity. J Clin Endocrinol Metab 1992;74:239-47.
- 21. Spritzer PM, Poy M, Wiltgen D, Mylius LS, Capp E. Leptin levels in hirsute women with polycystic ovary syndrome or idiopathic hirsutism: influence on LH and relationship with hormonal, metabolic, and anthropometric measurements. Hum Reprod 2001;16:1340-6.
- 22. Azziz R, Carmina E, Sawaya ME. Idiopathic hirsutism. Endocr Rev 2000;21:347-62.
- 23. Ferriman D, Gallwey JD. Clinical assessment of body hair growth in women. J Clin Endocrin Metab 1961;21:1140-7.
- 24. Rotterdam ESHRE/ASRM-Sponsored PCOS Consensus Workshop Group. Revised 2003 consensus on diagnostic criteria and long-term health risks related to polycystic ovary syndrome. Fertil Steril 2004;81:19-25.
- 25 Comim FV, Spritzer PM. Increased growth hormone response to clonidine in nonobese normoinsulinemic patients with polycystic ovary syndrome.Fertil Steril 2004;81:108-13.
- 26. Bachega TA, Billerbeck AE, Madureira G, Marcondes JA, Longui CA, Leite MV, et al. Molecular genotyping in Brazilian patients with the classical and nonclassical forms of 21-hydroxylase deficiency. J Clin Endocrinol Metab 1998;83:4416-9.
- 27. Spritzer P, Billaud L, Thalabard JC, Birman P, Mowszowicz I, Raux-Demay MC, et al. Cyproterone acetate versus hidrocortisone treatment in late-onset adrenal hyperplasia. J Clin Endocrinol Metab 1990;70:642-6.
- 28. Meldrum DR, Abraham GE. Peripheral and ovarian venous concentrations of various steroid hormones in virilizing ovarian tumors. Obstet Gynecol 1979;53:36-43.
- 29. Friedman CI, Schmidt GE, Kim MH, Powell J. Serum testosterone concentrations in the evaluation of androgen-producing tumors. Am J Obstet Gynecol 1985;153:44-9.
Datas de Publicação
-
Publicação nesta coleção
24 Mar 2010 -
Data do Fascículo
2010