Resumos
A utilização de proteínas sarcoplasmáticas junto de proteínas miofibrilares pode ser interessante na tecnologia de filmes comestíveis, pois eliminaria o processo de lavagem do músculo no preparo das proteínas. O objetivo deste trabalho foi estudar propriedades físicas de filmes constituídos de proteínas miofibrilares e sarcoplasmáticas do musculo de tilápia-do-nilo (Oreochromis niloticus), em razão da concentração de proteínas e do plastificante na solução filmogênica. Os filmes foram elaborados a partir de soluções filmogênicas contendo 1 e 2 g de proteínas do músculo/100 g de solução filmogênica e 15 a 65 g de glicerina/100 g de proteínas, com pH igual a 2,7 (ácido acético glacial), tratadas à temperatura de 90C por 30 minutos e desidratadas a 30° C por cerca de 24 horas. Os filmes produzidos com soluções de maior concentração de proteínas apresentaram-se mais coloridos, mais resistentes à perfuração e à tração, com maior capacidade de elongamento quando submetido à tração, e visivelmente mais opacos, embora nesse último caso, sem efeito significativo. As propriedades viscoelásticas e a deformação na perfuração não foram influenciadas pela concentração de proteínas. Todas as propriedades foram influenciadas pela concentração do plastificante.
proteína miofibrilar; proteína sarcoplasmática; cor; propriedade mecânica; viscoelasticidade
The use of sarcoplasmic proteins with myofibrilar proteins might be an interesting alternative in edible films technology, because it would eliminate the muscle washing step during protein extraction. The aim of this work was to study physical properties of films based on muscle proteins, constituted by myofibrilar and sarcoplasmic proteins, from Nile Tilapia (Oreochromis niloticus), as influenced by the protein concentration and the plasticizer content of the filmogenic solution. The films were made from filmogenic solutions with 1 or 2 g of proteins/100 g of solution and 15 to 65 g of glycerin/100 g of proteins, with the pH maintained at 2.7 (acetic acid), thermal treated at 90° C for 30 min, and dehydrated at 30° C for about 24 hours. Films made from solutions with higher protein concentration were more colored, more resistant to puncture and strain, with higher elongation capacity under strain and visibly more opaque, although significant difference was not found for this last property. The viscoelastic properties and the puncture deformation were not influenced by protein concentration. All properties were affected by the plasticizer content.
myofibrillar proteins; sarcoplasmic proteins; colour; mechanical properties; viscoelasticity
TECNOLOGIA DE ALIMENTOS
Propriedades de filmes comestíveis produzidos com diferentes concentrações de plastificantes e de proteínas do músculo de tilápia-do-nilo
Properties of edible films based on different concentrations of plasticizer and Nile Tilapia muscle protein
Paulo José do Amaral SobralI; Farah Trementoza GarcíaI; Ana Mônica Quinta Barbosa HabitanteII; Ednelí Soraya Monterrey-QuinteroI
IUniversidade de São Paulo (USP), Fac. de Zootecnia e Engenharia de Alimentos, Dep. de Engenharia de Alimentos, Av. Duque de Caxias Norte 225, CEP 13639-900 Pirassununga, SP. E-mail: pjsobral@usp.br, farahvet@bol.com.br, edneli@usp.br
IIUSP, Dep. de Zootecnia. E-mail: amonica@usp.br
RESUMO
A utilização de proteínas sarcoplasmáticas junto de proteínas miofibrilares pode ser interessante na tecnologia de filmes comestíveis, pois eliminaria o processo de lavagem do músculo no preparo das proteínas. O objetivo deste trabalho foi estudar propriedades físicas de filmes constituídos de proteínas miofibrilares e sarcoplasmáticas do musculo de tilápia-do-nilo (Oreochromis niloticus), em razão da concentração de proteínas e do plastificante na solução filmogênica. Os filmes foram elaborados a partir de soluções filmogênicas contendo 1 e 2 g de proteínas do músculo/100 g de solução filmogênica e 15 a 65 g de glicerina/100 g de proteínas, com pH igual a 2,7 (ácido acético glacial), tratadas à temperatura de 90C por 30 minutos e desidratadas a 30° C por cerca de 24 horas. Os filmes produzidos com soluções de maior concentração de proteínas apresentaram-se mais coloridos, mais resistentes à perfuração e à tração, com maior capacidade de elongamento quando submetido à tração, e visivelmente mais opacos, embora nesse último caso, sem efeito significativo. As propriedades viscoelásticas e a deformação na perfuração não foram influenciadas pela concentração de proteínas. Todas as propriedades foram influenciadas pela concentração do plastificante.
Termos para indexação: proteína miofibrilar, proteína sarcoplasmática, cor, propriedade mecânica, viscoelasticidade.
ABSTRACT
The use of sarcoplasmic proteins with myofibrilar proteins might be an interesting alternative in edible films technology, because it would eliminate the muscle washing step during protein extraction. The aim of this work was to study physical properties of films based on muscle proteins, constituted by myofibrilar and sarcoplasmic proteins, from Nile Tilapia (Oreochromis niloticus), as influenced by the protein concentration and the plasticizer content of the filmogenic solution. The films were made from filmogenic solutions with 1 or 2 g of proteins/100 g of solution and 15 to 65 g of glycerin/100 g of proteins, with the pH maintained at 2.7 (acetic acid), thermal treated at 90° C for 30 min, and dehydrated at 30° C for about 24 hours. Films made from solutions with higher protein concentration were more colored, more resistant to puncture and strain, with higher elongation capacity under strain and visibly more opaque, although significant difference was not found for this last property. The viscoelastic properties and the puncture deformation were not influenced by protein concentration. All properties were affected by the plasticizer content.
Index terms: myofibrillar proteins, sarcoplasmic proteins, colour, mechanical properties, viscoelasticity.
Introdução
Em meados dos anos 90, Cuq et al. (1995), trabalhando com sardinhas, demonstraram que as proteínas miofibrilares possuem a capacidade de formar filmes transparentes e resistentes. Desde então, vários trabalhos foram realizados com proteínas miofibrilares de músculos post rigor mortis de sardinha do Atlântico (Sardina pilchardus) (Cuq et al., 1996, 1997a, 1997b, 1997c), de músculos ante rigor mortis de tilápia-do-nilo (Oreochromis niloticus) de cultivo (Chandra & Sobral, 2000, Monterrey-Quintero & Sobral, 1999, 2000; Sobral, 2000; Sobral et al., 2002), e de carne bovina (Bos taurus taurus) (Sobral et al., 1998). Mais recentemente, Iwata et al. (2000) e Tanaka et al. (2001) desenvolveram e caracterizaram filmes à base de proteínas sarcoplasmáticas extraídas do músculo de merlin azul (Makaira mazara). Em virtude disso, Paschoalick et al. (2003) desenvolveram filmes flexíveis à base de proteínas do músculo de tilápia-do-nilo (proteínas miofibrilares + proteínas sarcoplasmáticas), sem as proteínas do estroma, considerando desnecessário o processo de lavagem dos músculos de peixes no preparo das proteínas, conforme técnica difundida na tecnologia de filmes comestíveis (Cuq et al., 1995; Sobral et al., 1998; Monterrey-Quintero & Sobral, 2000).
As proteínas miofibrilares são normalmente insolúveis em água, mas podem ser solubilizadas controlando-se o pH da solução. Essas proteínas, que são completamente estendidas, apresentam cadeias de polipeptídeos fortemente associadas entre si, em estruturas paralelas (Iwata et al., 2000). Em razão disso, essas proteínas são capazes de formar uma matriz contínua durante a secagem da solução (Cuq et al., 1995; Monterrey-Quintero & Sobral, 2000). Por outro lado, as proteínas sarcoplasmáticas são proteínas globulares que, geralmente, têm que ser desnaturadas termicamente para formar uma matriz contínua (Iwata et al., 2000). O aquecimento modifica a estrutura tridimensional das proteínas globulares, causando exposição dos grupos SH dos resíduos da cistina, provocando a produção de pontes de enxofre (S-S) entre cadeias de proteínas adjacentes, e também promovendo a exposição de grupos funcionais que proporcionarão interações hidrofóbicas durante a secagem (Perez-Gago & Krochta, 2001).
A concentração de proteínas na solução filmogênica também pode influir na formação da matriz protéica. A elaboração de filmes com isolado protéico de soro do leite, por exemplo, exige uma concentração relativamente elevada (acima de 8%) de proteínas na solução para que ocorra a formação de pontes S-S (Perez-Gago & Krochta, 2001). Entretanto, as proteínas do músculo de peixe, quando solubilizadas pelo abaixamento do pH, proporcionam soluções coloidais extremamente viscosas (Cuq et al., 1995). Assim, é necessário trabalhar com menores concentrações de proteínas na solução formadora do filme.
A elaboração de filmes com essas proteínas exige o uso de plastificantes, geralmente polióis, que reduzem as interações intermoleculares entre cadeias adjacentes do biopolímero, resultando no aumento da mobilidade dessas cadeias e, conseqüentemente, em materiais flexíveis (Gontard et al., 1993; Cuq et al., 1997a). Como conseqüência, percebem-se, em termos macroscópicos, alterações de todas as propriedades físicas ou funcionais dos filmes.
O objetivo deste trabalho foi estudar algumas propriedades físicas de filmes de proteínas miofibrilares e sarcoplasmáticas do músculo de tilápia-do-nilo em razão da concentração de proteínas e do plastificante na solução filmogênica, tratada a 90ºC por 30 minutos.
Material e Métodos
As proteínas do músculo de tilápia-do-nilo (Oreochromis niloticus) foram preparadas, pré rigor mortis, a partir de peixes cultivados no Campus da Universidade de São Paulo (USP), Pirassununga, SP, segundo Paschoalick et al. (2003). Os peixes foram abatidos após insensibilização com água gelada. As proteínas foram liofilizadas em um liofilizador de bancada, após congelamento com nitrogênio líquido. O produto liofilizado foi analisado quanto ao teor de proteínas, pelo método micro-Kjeldhal (AOAC International, 1995).
Os filmes de proteínas do músculo de tilápia-do-nilo foram preparados segundo Monterrey-Quintero & Sobral (2000), a partir de soluções filmogênicas com 1 e 2 g de proteínas/100 g de solução filmogênica e 15 a 65 g do plastificante glicerina/100 g de proteínas, com pH mantido em 2,7 com o emprego de ácido acético glacial, tratamento térmico de 90° C por 30 minutos, e desidratação a 30° C em suportes de plexiglass de 12x12 cm, por cerca de 24 horas. Detalhes dos procedimentos e dos materiais usados estão descritos nos trabalhos de Monterrey-Quintero & Sobral (2000), Sobral (2000) e Paschoalick et al. (2003).
Antes das caracterizações, os filmes foram acondicionados em dessecadores contendo NaBr (umidade relativa de 58%), a 22-25° C, por sete dias. A espessura dos filmes foi então medida com um micrômetro digital (com precisão de 0,001 mm), com sensor de medida de 6,4 mm de diâmetro, em nove pontos diferentes, considerando-se como espessura dos filmes, a média das nove leituras.
A cor dos filmes foi determinada com um colorímetro controlado pelo programa Universal Software 3.2, trabalhando com D65 (luz do dia) e usando-se os padrões CIE Lab: L*, variando de 0 (preto) a 100 (branco); a*, do verde (-) ao vermelho (+); e b*, do azul (-) ao amarelo (+) (Gennadios et al., 1996). Os filmes foram aplicados na superfície de uma placa branca padrão e os padrões L*, a* e b* foram medidos. A diferença de cor (DE*) foi calculada de acordo com a seguinte equação:
em que DL*, Da* e Db* são os diferenciais entre os cromas das amostras e do padrão branco: L* = 94,89; a* = -0,78; b* = 1,43.
A opacidade dos filmes foi calculada (Y = Yp/Yb) de acordo com a relação entre a opacidade da amostra sobre o padrão preto (Yp) e sobre o padrão branco (Yb), determinadas segundo Hunterlab (Sobral, 2000), utilizando-se o mesmo aparelho e programa de computador usados nas medidas de cor.
As propriedades mecânicas dos filmes foram determinadas pelos testes de perfuração e de tração, ambos realizados com um instrumento de medidas físicas TA.XT2i (SMS) com célula de carga de 25 kg. O controle do aparelho e as análises dos dados foram feitos com ajuda do programa Texture Expert 1.15 (Stable Micro Systems).
Nos testes de perfuração, os filmes foram fixados em uma célula com 52,6 cm de diâmetro e perfurados por uma sonda de 3 mm de diâmetro, deslocando-se a 1 mm/s (Gontard et al., 1993). A força na perfuração foi determinada diretamente das curvas de força (N) x deslocamento (mm) da sonda. A deformação na perfuração (%) foi calculada considerando-se que a tensão estava distribuída em toda a superfície do filme e a deformação foi uniforme (Sobral et al., 2001), com a seguinte equação:
em que lo é o comprimento inicial do filme, igual ao raio da célula de medida (26,3 mm) e D é o deslocamento da sonda na perfuração.
Nos testes de tração, os filmes foram cortados em tiras de 16 mm de largura e 100 mm de comprimento, e tracionados a uma velocidade de 0,9 mm/s, partindo-se de uma separação inicial (lo) das garras de 80 mm, até a ruptura (l) (Gennadios et al., 1993). A tensão na ruptura e a deformação na ruptura foram determinadas diretamente das curvas tensão x deformação, e o módulo de elasticidade, calculado como a inclinação da porção linear (inicial) dessa curva (com a deformação expressa em porcentagem).
As propriedades viscoelásticas dos filmes foram caracterizadas por análise dinâmico-mecânica. Empregou-se um aparelho DMA2980, ligado ao controlador TA5000, trabalhando em modo de tração uniaxial senoidal, com varredura de freqüência (0,01-200 Hz), mantendo-se constantes a temperatura (30° C), a amplitude de deformação (0,2%) e o fluxo de N2 na câmara de medida (1.180 mL/min). As amostras retangulares, de cerca de 19x5 mm, foram submetidas à tração oscilatória, obtendo-se como respostas, o módulo de armazenamento (E'), o módulo de perda (E") e o ângulo de fase (tand = E''/E') em função da freqüência. Assim, as propriedades viscoelásticas foram calculadas a 1 Hz (Lazaridou & Biliaderis, 2002) com ajuda do programa Universal Analysis V1.7F.
Todos os testes foram realizados em sala climatizada, a 22° C e 55-65% de umidade relativa, em quadruplicatas. As médias das propriedades dos filmes foram comparadas pelo teste de Duncan a 5% de probabilidade por meio do programa estatístico SAS (SAS Institute, 1989).
Resultados e Discussão
As proteínas liofilizadas do músculo de tilápia-do-nilo apresentaram um teor de proteína de 80%, o qual foi considerado nos cálculos da concentração de proteína e de glicerina na solução filmogênica.
De modo geral, os filmes preparados com 1 e 2 g de proteínas/100 g de solução filmogênica se apresentaram manuseáveis, bastante resistentes (avaliação subjetiva) e com bom aspecto. As espessuras médias (médiadesvio-padrão), calculadas com os dados de todos os filmes foram 0,083±0,006 mm e 0,084±0,007 mm em relação a 1 e 2 g de proteínas, respectivamente.
Os filmes produzidos com 2 g de proteínas foram mais coloridos do que os filmes produzidos com 1 g, exceto no caso dos filmes com 45% de glicerina, em que não se observou diferença significativa (Figura 1). Esses resultados podem indicar que o aumento da concentração de proteínas na solução filmogênica favoreceu alguma reação formadora de base de Schiff, entre a lisina e a glicerina, sob o efeito do tratamento térmico. Paschoalick et al. (2003), trabalhando com 1 g de proteínas do músculo de tilápia-do-nilo/100 g de solução filmogênica, observaram que a coloração dos filmes aumentou com o tratamento térmico (40, 65 e 90° C por 30 minutos).
Os filmes obtidos no presente trabalho apresentaram maior coloração que os filmes obtidos por Sobral (2000), à base de 1 g de proteínas miofibrilares de tilápia-do-nilo/100 g de solução filmogênica tratada a 40° C por 30 minutos (DE* = 7-8; x = 0,077-0,087 mm) e do que os filmes obtidos por Gennadios et al. (1996), de ovoalbuminas (DE* = 1,7-2,3; x = 0,099 mm).
A diferença de cor dos filmes produzidos foi causada pela variação do padrão b* (Figura 1). A similaridade de comportamento e a proximidade dos valores de b* com DE* permitem sugerir que os filmes apresentaram coloração amarelado-clara.
No caso da opacidade, o efeito da concentração de proteína foi significativo apenas nos casos dos filmes com 25% e 45% de glicerina (Figura 1). Esse resultado pode ser explicado considerando-se que a opacidade foi provocada pela desnaturação das proteínas sarcoplasmáticas e miofibrilares, cujas temperaturas de desnaturação são inferiores à temperatura de tratamento térmico (Monterrey-Quintero & Sobral, 2000) e que não devem depender da concentração de proteínas, no domínio estudado.
A opacidade dos filmes obtidos no presente trabalho foi comparável à de filmes obtidos por Paschoalick et al. (2003), elaborados com 1 g de proteínas do músculo de tilápia-do-nilo/100 g de solução filmogênica tratada a 40° C e 65° C por 30 minutos (Y = 2-7, x = 0,077 mm), sendo porém mais opacos que os filmes obtidos por Sobral (2000), à base de proteínas miofibrilares de tilápia-do-nilo (Y<3,5; x<0,090 mm).
Tanto a diferença de cor, quanto a opacidade dos filmes diminuíram com o aumento da concentração de glicerina, provavelmente pelo efeito de diluição provocado pela glicerina (Paschoalick et al., 2003), que é um produto incolor e transparente (Figura 1).
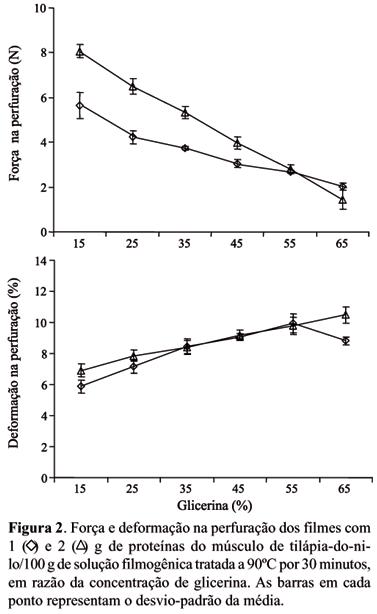
De acordo com os resultados dos testes de perfuração (Figura 2) e de tração (Figura 3), os filmes elaborados com 2 g de proteínas foram mais resistentes que os filmes com 1 g de proteínas, não se observando diferenças significativas apenas nos resultados dos testes de perfuração dos filmes com alta concentração de glicerina (acima de 55%). Isto pode ser explicado pelo possível efeito da concentração de proteínas sobre a cinética de reação dos resíduos sulfurosos da cistina, presentes nas proteínas, isto é, o aumento da concentração de proteínas pode ter favorecido a formação de pontes de sulfeto entre as cadeias de proteínas em virtude do tratamento térmico (Perez-Gago & Krochta, 2001; Choi & Han, 2002). Porém, Iwata et al. (2000) observaram que a redução da concentração de proteínas sarcoplasmáticas de 4% para 2% na solução filmogênica causou um aumento significativo na tensão de ruptura dos filmes, ou seja, efeito contrário ao observado no presente trabalho.
Os filmes produzidos neste trabalho apresentaram valores de força na perfuração equivalentes aos de filmes de proteínas de músculo de tilápia-do-nilo, cuja solução filmogênica foi tratada a 40C e 65° C por 30 minutos (6-2 N, x = 0,077 mm) obtido por Paschoalick et al. (2003) e aos de filmes a base de proteínas miofibrilares de tilápia-do-nilo com 1,25% de proteínas/100 g de solução filmogênica, obtidos por Monterrey-Quintero & Sobral (1999) (7-4 N). Por outro lado, pode-se considerar que a resistência à tração dos filmes do presente trabalho foi superior a dos filmes de proteínas sarcoplasmáticas de merlin azul (em torno de 3,5 MPa, Cp = 3% e pH 10), cuja solução filmogênica foi tratada a 90° C (Iwata et al., 2000), porém inferior a dos filmes de proteínas miofibrilares de sardinhas (17,1 MPa, x = 0,034 mm), cuja solução filmogênica foi tratada a 25° C (Cuq et al., 1995).
A concentração de proteínas praticamente não afetou os resultados do módulo de elasticidade dos filmes, observando-se diferenças significativas apenas em relação aos filmes com 15% e 25% de glicerina (Figura 3). Entretanto, os maiores valores foram obtidos nos filmes feitos com 1 g de proteínas, indicando tratar-se de material mais rígido. Os valores do módulo de elasticidade dos filmes produzidos foram da mesma ordem de grandeza dos resultados obtidos por Perez-Gago & Krochta (2001).
Se por um lado, a capacidade de deformação na perfuração (Figura 2) dos filmes praticamente não foi afetada pela concentração de proteínas (observou-se diferença significativa apenas nos extremos de concentração de glicerina de 15% e 65%), por outro lado, a capacidade de se elongar antes de romper por tracionamento foi fortemente afetada pela concentração de proteínas (Figura 3). Iwata et al. (2000) também observaram que o aumento da concentração de proteínas sarcoplasmáticas de 2% a 4% provocou aumento da deformação na ruptura dos respectivos filmes.
A deformação na perfuração dos filmes obtidos foi superior àquelas determinadas por Paschoalick et al. (2003), com proteínas do músculo de tilápia-do-nilo (menor que 8%), e àquelas de filmes de proteínas miofibrilares de tilápia-do-nilo (em torno de 6%) obtidos por Sobral (2000), com espessura equivalente a dos filmes do presente trabalho. Pode-se considerar que a capacidade de deformar sob tração dos filmes foi superior a dos filmes de proteínas sarcoplasmáticas de merlin azul (em torno de 70%, Cp = 3% e pH 10), cuja solução filmogênica foi tratada a 90° C (Iwata et al., 2000), e a dos filmes de proteínas miofibrilares de sardinhas (22,7%, x = 0,034 mm), cuja solução foi tratada a 25° C (Cuq et al., 1995).
A redução da força na perfuração, da tensão na ruptura e do módulo de elasticidade com o aumento da concentração de glicerina (Figuras 2 e 3) são comportamentos típicos dos filmes à base de biopolímeros (Gontard et al., 1993; Cuq et al., 1997a; Sobral et al., 1998; Monterrey-Quintero & Sobral, 1999). A presença do plastificante diminuiu as interações proteína-proteína, aumentando a mobilidade das cadeias polipeptídicas, tornando os filmes menos resistentes e mais elásticos.
A concentração das proteínas na solução filmogênica não influenciou (P>0,05) as propriedades viscoelásticas calculadas a 1 Hz, a partir dos espectros mecânicos obtidos nas análises dinâmico-mecânicas. Tanto o módulo de armazenamento (E') quanto o módulo de perda (E") diminuíram consideravelmente com o aumento da concentração de glicerina (Figura 4). Por outro lado, o ângulo de fase (tand) aumentou com a concentração de glicerina. Esses resultados estão de acordo com os observados por Paschoalick et al. (2003), com filmes de proteínas do músculo de tilápia-do-nilo. Segundo Ferry (1980), tanto o solvente (glicerina), quanto o soluto (proteínas) contribuem com E", ao passo que apenas o soluto contribui com E'. Assim, uma maior influência da glicerina sobre E" pode ter provocado o aumento do ângulo de fase.
Os valores das propriedades viscoelásticas (E', E" e tand) foram da mesma ordem de grandeza dos valores obtidos por Cuq et al. (1997b, 1997c), que trabalharam com filmes de proteínas miofibrilares de sardinha do Atlântico, e de Cherian et al. (1995) e Gontard & Ring (1996) que trabalharam com filmes de glúten contendo vários plastificantes. De maneira geral, é muito difícil comparar esses tipos de resultados, porque a maioria dos autores trabalhou com varredura da temperatura e, sobretudo, porque se interessaram pelo efeito plastificante da umidade em amostras condicionadas convenientemente, e não necessariamente do plastificante adicionado, como no presente trabalho. Além disso, Cuq et al. (1996) e Chandra & Sobral (2000) trabalharam com propriedades viscoelásticas de filmes comestíveis, porém determinadas com métodos estáticos (relaxamento de tensão).
Conclusões
1. Filmes produzidos a partir de soluções mais concentradas de proteínas do músculo de tilápia-do-nilo são mais coloridos, mais resistentes à perfuração e à tração, e com maior capacidade de elongação quando submetidos à tração.
2. As propriedades viscoelásticas e a deformação na perfuração não são influenciadas pela concentração de proteínas do músculo de tilápia-do-nilo na solução filmogênica.
3. A concentração de plastificante influencia as propriedades físicas do filme.
Agradecimentos
À Fapesp, pelo auxílio (00/14091-8); à Capes, pela bolsa MS de FTG; ao CNPq, pela bolsa PQI de PJAS (522953/95-6).
Recebido em 2 de agosto de 2003 e aprovado em 12 de novembro de 2003
- AOAC INTERNATIONAL (Gaithersburg, Estados Unidos). Official methods of analysis of AOAC international 16thed. Washington, 1995. 2v.
- CHANDRA, P.; SOBRAL, P.J. do A. Calculation of viscoelastic properties of edible films: application of three models. Ciência e Tecnologia de Alimentos, v.20, p.250-256, 2000.
- CHERIAN, G.; GENNADIOS, A.; WELLER, C.; CHINACHOTI, P. Thermomechanical behavior of wheat gluten films: effect of sucrose, glycerin and sorbitol. Cereal Chemistry, v.72, p.1-6, 1995.
- CHOI, W.S.; HAN, J.H. Film-forming mechanism and heat denaturation effects on the physical and chemical properties of pea-protein-isolate edible films. Journal of Food Science, v.67, p.1399-1406, 2002.
- CUQ, B.; AYMARD, C.; CUQ, J.L.; GUILBERT, S. Edible packaging films based on fish myofibrillar proteins: formulation and functional properties. Journal of Food Science, v.60, p.1369-1374, 1995.
- CUQ, B.; GONTARD, N.; CUQ, J.L.; GUILBERT, S. Rheological models for the mechanical properties of myofibrillar protein-based films. Journal of Agricultural and Food Chemistry, v.44, p.1116-1122, 1996.
- CUQ, B.; GONTARD, N.; CUQ, J.L.; GUILBERT, S. Selected functional properties of fish myofibrillar protein-based films as affected by hydrophilic plasticizers. Journal of Agricultural and Food Chemistry, v.45, p.622-626, 1997a.
- CUQ, B.; GONTARD, N.; GUILBERT, S. Thermal properties of fish myofibrillar protein-based films as affected by moisture content. Polymer, v.38, p.2399-2405, 1997b.
- CUQ, B.; GONTARD, N.; GUILBERT, S. Thermoplastic properties of fish myofibrillar proteins: application to biopackaging fabrication. Polymer, v.38, p.4071-4078, 1997c.
- FERRY, J.D. Viscoelastic properties of polymers New York: J. Wiley, 1980. 641p.
- GENNADIOS, A.; PARK, H.J.; WELLER, C.L. Relative humidity and temperature effects on tensile strength of edible protein and cellulose ether films. Transactions of the ASAE, v.36, p.1867-1872, 1993.
- GENNADIOS, A.; WELLER, C.L.; HANNA, M.A.; FRONING, G.W. Mechanical and barrier properties of egg albumen films. Journal of Food Science, v.61, p.585-589, 1996.
- GONTARD, N.; RING, S. Edible wheat gluten film: influence of water content on glass transition temperature. Journal of Agricultural and Food Chemistry, v.44, p.3474-3478, 1996.
- GONTARD, N.; GUILBERT, S.; CUQ, J.L. Water and glycerol as plasticizer affect mechanical and water vapor barrier properties of an edible wheat gluten film. Journal of Food Science, v.58, p.206-211, 1993.
- IWATA, K.; ISHIZAKI, S.; HANDA, A.; TANAKA, M. Preparation and characterization of edible films from fish water-soluble proteins. Fisheries Science, v.66, p.372-378, 2000.
- LAZARIDOU, A.; BILIADERIS, C.G. Thermophysical properties of chitosan, chitosan-starch and chitosan-pullulan films near the glass transition. Carbohydrates Polymers, v.48, p.179-190, 2002.
- MONTERREY-QUINTERO, E.S.; SOBRAL, P.J. do A. Caracterização de propriedades mecânicas e óticas de biofilmes à base de proteínas miofibrilares de tilápia-do-nilo usando uma metodologia de superfície-resposta. Ciência e Tecnologia de Alimentos, v.19, p.294-301, 1999.
- MONTERREY-QUINTERO, E.S.; SOBRAL, P.J. do A. Preparo e caracterização de proteínas miofibrilares de tilápia-do-nilo (Oreochromis niloticus) para elaboração de biofilmes. Pesquisa Agropecuária Brasileira, v.35, p.179-189, 2000.
- PASCHOALICK, T.M.; GARCIA, F.T.; SOBRAL, P.J. do A.; HABITANTE, A.M.Q.B. Characterization of some functional properties of edible films based on muscle proteins of Nile Tilapia. Food Hydrocolloids, v.17, p.419-427, 2003.
- PEREZ-GAGO, M.B.; KROCHTA, J.M. Denaturation time and temperature effects on solubility, tensile properties, and oxygen permeability of whey protein edible films. Journal of Food Science, v.66, p.705-710, 2001.
- SAS INSTITUTE (Cary, Estados Unidos). SAS/STAT user's guide: version 6. 4thed. Cary, 1989. v.2.
- SOBRAL, P.J. do A. Influência da espessura sobre certas propriedades de biofilmes à base de proteínas miofibrilares. Pesquisa Agropecuária Brasileira, v.35, p.1251-1259, 2000.
- SOBRAL, P.J. do A.; MENEGALLI, F.C.; HUBINGER, M.D.; ROQUES, M.A. Mechanical, water vapor barrier and thermal properties of gelatin based edible films. Food Hydrocolloids, v.15, p.423-432, 2001.
- SOBRAL, P.J. do A.; MONTERREY-QUINTERO, E.S.; HABITANTE, A.M.Q.B. Glass transition of Nile tilapia myofibrillar protein films plasticized by glycerin and water. Journal of Thermal Analysis and Calorimetry, v.67, p.499-504, 2002.
- SOBRAL, P.J. do A.; OCUNO, D.; SAVASTANO JÚNIOR, H. Preparo de proteínas miofibrilares de carne e elaboração de biofilmes com dois tipos de ácidos: propriedades mecânicas. Brazilian Journal of Food Technology, v.1, p.44-52, 1998.
- TANAKA, M.; IWATA, K.; SANGUANDEEKUL, R.; HANDA, A.; ISHIZAKI, S. Influence of plasticizers on the properties of edible films prepared from fish water-soluble proteins. Fisheries Science, v.67, p.346-351, 2001.
Datas de Publicação
-
Publicação nesta coleção
22 Jun 2004 -
Data do Fascículo
Mar 2004
Histórico
-
Aceito
12 Nov 2003 -
Recebido
02 Ago 2003