Resumos
A miocardiopatia não compactada isolada é uma doença rara, que provavelmente surge no período embrionário, com a parada intrauterina da compactação miocárdica no início do desenvolvimento fetal, e que determina trabeculações miocárdicas proeminentes com recessos intertrabeculares profundos e espessamento do miocárdio em duas camadas distintas (compactado e não compactado). Embora descrita inicialmente na população pediátrica ou em conjunto com cardiopatia congênita, pode-se compreender que essa doença ocorre de forma isolada, porque o diagnóstico é cada vez mais comum em pacientes adultos que não apresentam outra doença cardíaca. As manifestações clínicas são altamente variáveis, porque partem da ausência de sintomas à insuficiência cardíaca congestiva, arritmias e tromboembolismo sistêmico. A ecocardiografia é o procedimento diagnóstico mais utilizado, porém o pouco conhecimento sobre essa doença, sua semelhança com outras afecções miocárdicas e a limitação da técnica ecocardiográfica empregada fazem com que o diagnóstico seja postergado. Esta revisão objetiva mostrar que outras modalidades de imagem como ressonância magnética, tomografia computadorizada e ventriculografia esquerda são alternativas diagnósticas.
Cardiomiopatias; estruturas embrionárias; feto; cardiopatias congênitas
Isolated non-compaction cardiomyopathy is a rare disease that is likely to develop in the embryonic period. It is caused by the intrauterine arrest of the myocardial compaction process in the beginning of the fetal development. It is characterized by prominent myocardial trabeculations and deep intertrabecular recesses, as well as the thickening of the myocardium into two distinct layers (compacted and not compacted). Even though this disease is said to be prevalent in the pediatric population or together with congenital heart disease, one can understand that this disease occurs in isolation, because the diagnosis is becoming more common in adult patients that have no other heart disease. The clinical manifestations vary greatly, because they range from absence of symptoms to congestive heart failure, arrhythmias and systemic thromboembolism. Echocardiography is the most widely used diagnostic procedure, but the little knowledge about this disease, its similarity to other myocardial diseases and the limitation of the echocardiographic technique used delay the diagnosis. The purpose of this review is to show that that other imaging techniques, such as MRI, CT and left ventriculography have emerged as diagnostic alternatives.
Cardiomyopathies; embryonic structures; fetus; heart defects, congenital
La miocardiopatía no compactada aislada es una enfermedad rara, que probablemente surge en el período embrionario, con la parada intrauterina de la compactación miocárdica en el comienzo del desarrollo fetal, y que determina trabeculaciones miocárdicas prominentes con recesos intertrabeculares profundos y espesamiento del miocardio en dos capas distintas (compactado y no compactado). Aunque descripta inicialmente en la población pediátrica o en conjunto con cardiopatía congénita, se puede comprender que esa enfermedad ocurre de forma aislada, porque el diagnóstico es cada vez más común en pacientes adultos que no presentan otra enfermedad cardíaca. Las manifestaciones clínicas son altamente variables, porque parten de la ausencia de síntomas a la insuficiencia cardíaca congestiva, arritmias y tromboembolismo sistémico. La ecocardiografía es el procedimiento diagnóstico más utilizado, sin embargo el poco conocimiento sobre esa enfermedad, su semejanza con otras afecciones miocárdicas y la limitación de la técnica ecocardiográfica empleada hacen que el diagnóstico sea postergado. Esta revisión pretende mostrar que otras modalidades de imagen como resonancia magnética, tomografía computarizada y ventriculografía izquierda son alternativas diagnósticas.
Cardiomiopatías; estructuras embrionarias; feto; cardiopatías congénitas
ATUALIZAÇÃO CLÍNICA
Miocardiopatia não compactada - uma visão atual
Leonardo Vieira da Rosa; Vera Maria Cury Salemi; Leonardo Machado Alexandre; Charles Mady
Instituto do Coração (InCor) do Hospital das Clínicas da Faculdade de Medicina da Universidade de São Paulo, São Paulo, SP - Brasil
Correspondência Correspondência: Leonardo Vieira da Rosa Rua Alves Guimarães, 518/193 - Pinheiros 05407-000 - São Paulo, SP - Brasil E-mail: vieira27130@yahoo.com.br, vieira27130@hotmail.com
RESUMO
A miocardiopatia não compactada isolada é uma doença rara, que provavelmente surge no período embrionário, com a parada intrauterina da compactação miocárdica no início do desenvolvimento fetal, e que determina trabeculações miocárdicas proeminentes com recessos intertrabeculares profundos e espessamento do miocárdio em duas camadas distintas (compactado e não compactado). Embora descrita inicialmente na população pediátrica ou em conjunto com cardiopatia congênita, pode-se compreender que essa doença ocorre de forma isolada, porque o diagnóstico é cada vez mais comum em pacientes adultos que não apresentam outra doença cardíaca. As manifestações clínicas são altamente variáveis, porque partem da ausência de sintomas à insuficiência cardíaca congestiva, arritmias e tromboembolismo sistêmico. A ecocardiografia é o procedimento diagnóstico mais utilizado, porém o pouco conhecimento sobre essa doença, sua semelhança com outras afecções miocárdicas e a limitação da técnica ecocardiográfica empregada fazem com que o diagnóstico seja postergado. Esta revisão objetiva mostrar que outras modalidades de imagem como ressonância magnética, tomografia computadorizada e ventriculografia esquerda são alternativas diagnósticas.
Palavras-chave: Cardiomiopatias, estruturas embrionárias/anormalidades, feto/anormalidades, cardiopatias congênitas.
Introdução
Os primeiros casos relatados de miocardiopatia não compactada (MNC) foram associados à doença cardíaca congênita com obstruções de via de saída do ventrículo esquerdo e direito, malformações congênitas cianóticas complexas e anomalias coronarianas1. A forma isolada da não compactação miocárdica foi primeiramente relatada por Chin e cols.2 em 1990, que descreveu oito casos da doença2.
A miocardiopatia não compactada é uma desordem rara, classificada como cardiomiopatia primária geneticamente determinada pela Associação Americana de Cardiologia3 ou como miocardiopatia não classificada pela Organização Mundial da Saúde. Caracteriza-se pelos seguintes aspectos:
Alteração na parede miocárdica devido à proeminência de suas trabeculações com recessos intertrabeculares profundos que podem ser secundários à parada intrauterina da compactação miocárdica que ocorre nos primórdios do desenvolvimento fetal; o resultado são duas lâminas apresentadas pelo miocárdio, em que uma é compactada, e a outra, não compactada4,5.
Continuidade entre a cavidade ventricular e os recessos intertrabeculares, que são preenchidos com sangue do ventrículo e que não possuem comunicação com o sistema coronariano epicárdico.
Diminuição da reserva do fluxo coronariano avaliado pelo PET-CT, observado na maioria dos segmentos que apresentam anormalidades de movimento da parede ventricular6.
A prevalência da MNC na população geral ainda não foi determinada. No entanto, em uma população de pacientes submetidos à avaliação ecocardiográfica, identificaram-se 34 casos em 15 anos de acompanhamento, o que representou 0,014% dos ecocardiogramas realizados7. Todavia, esse é um dado provavelmente subestimado, visto que a qualidade de imagem desse método melhorou muito nos últimos anos. Estudos mais recentes determinaram uma prevalência da doença em membros de famílias afetadas em torno de 18% a 50%8.
Patogênese e genética da não compactação
Durante o desenvolvimento embrionário do miocárdio, há uma rede de fibras musculares cardíacas frouxamente entrelaçadas e separadas por profundos recessos que ligam a parede miocárdica com a cavidade ventricular. Aproximadamente entre a 5ª e a 8ª semanas, essa malha esponjosa de fibras e espaços intertrabeculares irão compactar-se da direção do epicárdio ao endocárdio e da base ao ápice cardíaco4,9. Ao mesmo tempo em que ocorre a compactação, a circulação coronariana desenvolve-se com a redução dos recessos intertrabeculares e a formação de capilares. Esse processo envolve a secreção de fatores de crescimento endotelial, tais como neuregulinas e angiopoietinas4,10.
A causa da não compactação ainda não é totalmente compreendida, mas se acredita que a sobrecarga de pressão ou isquemia miocárdica tenham papel na regressão dos sinusoides embrionários. Esse processo resultará na persistência dos espaços intertrabeculares, podendo ter, em alguns casos, comunicação direta com cavidade ventricular e circulação coronariana7.
Em relação aos achados de microscopia eletrônica, não existe um padrão histológico específico, embora alguns estudos tenham descrito presença de necrose e fibrose na biópsia endomiocárdica11-14.
Algumas anormalidades cardíacas podem estar associadas à MNC:
Miocárdio não compactado com sinusóides e fístulas da artéria coronária direita pode apresentar anormalidades congênitas nas vias de saída dos ventrículos esquerdo e direito15.
Presença de anomalia de Ebstein, valva aórtica bivalvular e transposição dos grandes vasos16,17. Pacientes com MNC também podem apresentar defeito no septo ventricular18.
A MNC pode ocorrer em doenças metabólicas e síndromes genéticas, incluindo a síndrome de Barth, a doença de Charco-Marie-Tooth e a síndrome de Melnick-Needles19.
A MNC pode ser geneticamente esporádica ou familiar. Em um estudo, seis de 34 pacientes (18%) apresentavam história familiar de MNC7. Alguns indivíduos afetados podem ser detectados pelo rastreamento dos parentes assintomáticos de pacientes acometidos.
Diferentes genes têm sido identificados:
Mutações no gene G4.5, encontrado nos tafazzins, são responsáveis pela síndrome de Barth.
Mutação (P121L) no gene que codifica a alfadistrobrevina, proteína citoesquelética, e o fator de transcrição NKX2.5 foi encontrada em uma família com MNC e doença cardíaca congênita3,20,21.
Mutação do gene para proteína citoesquelética, CYPHER/ZASP, foi encontrada em uma família e em três casos esporádicos22,23.
O locus no cromossomo 11p15 foi visto em uma família com penetrância autossômica dominante24.
A mutação E101K da actina cardíaca alfa tem sido identificada em famílias com MNC, defeito septal e cardiomiopatia hipertrófica apical25.
Manifestações clínicas
As manifestações clínicas da MNC são muito variáveis (Tabela 1). Os pacientes podem ser assintomáticos ou demonstrar sintomas de insuficiência cardíaca, arritmias ou tromboembolismo25-27. Em uma pequena série de 16 casos, a média de tempo do início dos sintomas, após o diagnóstico, foi de 3,5 anos4. A frequência dessas manifestações foi ilustrada em uma série mais recente de 34 pacientes desses mesmos autores7. Nesse estudo, no momento do diagnóstico, as manifestações clínicas incluíam: dispneia - 27 pacientes (79%); insuficiência cardíaca (IC) classe funcional III e IV - 12 pacientes (35%); dor torácica - 9 pacientes (26%); fibrilação atrial crônica - 9 pacientes (26%).
A maioria dos pacientes com miocardiopatia não compactada apresentarão, ao longo dos anos, sintomas de falência ventricular. A origem da disfunção nesses pacientes ainda é obscura, mas acredita-se que a disfunção microcirculatória e, consequentemente, a hipoperfusão subendocárdica corroboram de forma determinante para esse quadro2.
Os achados eletrocardiográficos são frequentemente anormais, mas nenhuma alteração específica foi identificada7. As anormalidades que podem ser descritas são, basicamente, bloqueios de ramo e arritmias, como fibrilação atrial e taquicardia ventricular. Uma possível associação com bradicardia e Síndrome de Wolff Parkinson White foi descrita em 18% dos pacientes pediátricos com MNC20,28,29.
Diagnóstico
O diagnóstico da miocardiopatia não compactada é frequentemente realizado pela ecocardiografia. Porém, outras modalidades de imagem como a ressonância magnética, o método mais escolhido, tomografia computadorizada e ventriculografia esquerda podem diagnosticar ou confirmar a suspeita clínica.
Os principais diagnósticos diferenciais da MNC incluem: cardiomiopatia dilatada, doença cardíaca hipertensiva, cardiomiopatia hipertrófica apical, cardiomiopatia infiltrativa, e endomiocardiofibrose.
A. Ecocadiograma
É utilizado como método inicial no diagnóstico e acompanhamento7,30. Os critérios ecocardiográficos propostos incluem aqueles baseados em estudos observacionais de três autores: Chin e cols.2, Jenni e cols.30,31 e Stollberger e cols.32:
1. Os critérios propostos por Chin e cols.2
Presença de x / y < 0,5, em que:
X = distância da superfície epicárdica até o recesso trabecular;
Y = distância da superfície epicárdica até o pico das trabeculações.
Esses critérios são aplicados para trabeculações do ápice do ventrículo esquerdo com imagem apical quatro-câmaras ou subxifoide no final da diástole.
2. Critérios propostos por Stollberger e cols.32
Presença de mais de três trabeculações na parede ventricular esquerda, com localização apical dos músculos papilares, visível em um único plano da imagem.
Espaços intertrabeculares perfundidos desde a cavidade ventricular, visualizados por imagem ao Doppler colorido.
3. Critérios propostos por Jenni e cols.30,31
Ausência de anormalidades cardíacas coexistentes.
Espessamento segmentar da parede miocárdica do ventrículo esquerdo com duas lâminas: uma lâmina epicárdica fina e uma lâmina endocárdica espessa com proeminentes trabeculações e recessos profundos. A razão do miocárdico não compactado com miocárdico compactado no final da sistole é > 2:1;
Localização das trabéculas geralmente nas paredes apical/lateral, média/inferior do ventrículo esquerdo. A maioria dos segmentos não compactados é hipocinética.
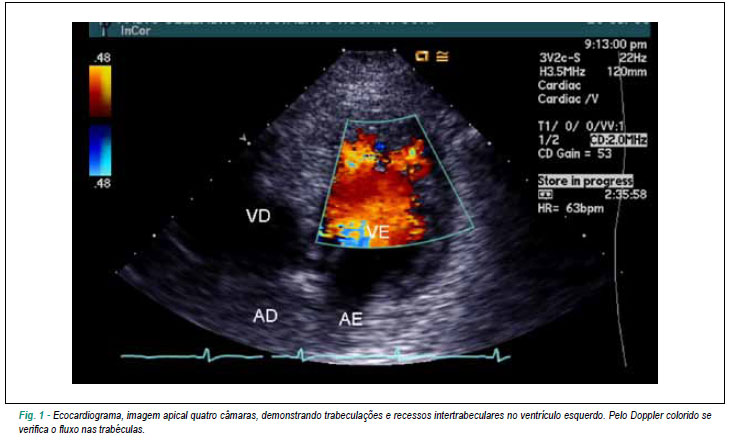
Pelo Doppler colorido pode ser identificado fluxo entre os recessos intertrabeculares (Figura 1).
Os critérios diagnósticos comumente utilizados são aqueles propostos por Jenni e cols.30 e Frischknecht e cols.31. São critérios ecocardiográficos disponíveis com maior acurácia. O estudo realizado por Frischknecht e cols., que fundamentou tais critérios, foi retrospectivo e cego, em que se avaliaram 19 pacientes com miocardiopatia não compactada, 31 com cardiopatia dilatada idiopática, 22 com miocardiopatia hipertensiva e 86 com doença valvar cardíaca grave com disfunção. Dos pacientes com MNC, todos apresentavam as duas estruturas laminares com espessamento da parede do ventrículo esquerdo, recessos perfundidos avaliados pelo Doppler colorido em 95% e segmentos hipocinéticos em 89%.
A localização das trabeculações na parede miocárdica encontra-se mais comumente em ápice e nas paredes lateral e inferior do ventrículo esquerdo33 (Tabela 2).
Ressonância magnética cardíaca
Tradicionalmente, a não compactação do ventrículo esquerdo é diagnosticada pela ecocardiografia, quando a relação do miocárdio não compactado para compactado é superior a dois. Porém, a ecocardiografia não pode, muitas vezes, visibilizar a região apical da melhor maneira, levando à subestimação do grau de não compactação ventricular esquerda. Com isso, a ressonância cardíaca tornou-se o método de escolha para confirmar ou afastar o diagnóstico da MNC, pois fornece uma descrição mais detalhada da morfologia cardíaca em qualquer plano de imagem (Figura 2). Uma relação do miocárdio não compactado ao compactado > 2,3 produz a maior sensibilidade (86%) e especificidade (99%) no diagnóstico34,35. A eficácia do diagnóstico realizado pela ressonância foi avaliada por um estudo com sete pacientes com MNC, comparando-se com 170 pacientes hígidos, atletas, pacientes com miocardiopatia hipertrófica, doença cardíaca, hipertensiva e estenose aórtica35 e observou-se:
1. Áreas de não compactação são mais comumente encontradas nas porções apical e lateral do ventrículo esquerdo35.
2. A relação miocárdico não compactado e compactado deve ser maior que 2,3 durante a diástole (sensibilidade de 86% e especificidade de 99%)35.
Limitações dos critérios dos diagnósticos
Já existem evidências suficientes que apoiam o conceito de miocardiopatia não compactada como uma doença real e que pode, em alguns casos, ter associação com outras anomalias cardíacas e sistêmicas, principalmente desordens neuromusculares. Entretanto, estudo recente36 demonstrou que uma grande proporção de pacientes com diagnóstico de insuficiência cardíaca sistólica preenche os critérios utilizados para MNC, pelo menos quando esses critérios são aplicados a posteriori. Também verificou-se que 8,3% dos controles normais arrolados nesse estudo preenchiam tais critérios, sugerindo que trabeculações proeminentes poderiam ser mais um achado incidental. Isso é particularmente verdadeiro em pessoas da raça negra, que têm uma maior incidência de hipertrabeculação que cumprem os atuais critérios de diagnóstico, independentemente da presença da doença ventricular esquerda.
Para se evitar um excesso de diagnósticos de MNC, recomenda-se a confirmação da suspeita diagnóstica com o uso da ressonância cardíaca, justamente para se diferenciar as trabéculas de bandas aberrantes, falsos tendões e inserção anormal de músculos papilares. Considerar diagnóstico diferencial com trombos, cardiomiopatia hipertrófica apical, fibroma, processo obliterante, hematoma intramiocárdico, metástases cardíacas ou abscesso intramiocárdico (Tabela 3)37,38.
Em crianças, essa cardiomiopatia deve ser diferenciada da atresia valvar pulmonar, com septo interventricular intacto e de patologias que possam induzir obstrução do fluxo de via de saída do ventrículo esquerdo. Alguns tumores cardíacos como os hemangiomas, que são caracterizados pela proliferação de vasos sanguíneos, podem ter a aparência de recessos26.
Tratamento
As principais complicações relacionadas à miocardiopatia não compactada são tromboembolismo, arritmias e insuficiência cardíaca progressiva. A prevenção das complicações tromboembólicas tem sido alvo de intensos debates, alguns autores recomendam anticoagulação profilática, em longo prazo, para todos pacientes com o diagnóstico de não compactação ventricular, independentemente da função ventricular4,7. No entanto, o risco de tromboembolismo é provavelmente menor do que se acreditava anteriormente, com isso algumas diretrizes, incluindo a brasileira39, recomendam anticoagulação aos pacientes que apresentam função sistólica diminuída com fração de ejeção inferior a 40%, história de tromboembolismo ou fibrilação atrial8. Preconiza-se o uso da aspirina em pacientes assintomáticos e com função sistólica normal. Em relação aos betabloqueadores, a sua utilização na disfunção ventricular esquerda promovida pela não compactação é feita por extrapolação das indicações de manejo na insuficiência cardíaca. Embora os resultados sejam escassos, devem ser utilizados, juntamente com inibidores da enzima de conversão do angiotensinogênio (IECAS). Existe apenas um único estudo que avaliou o uso de betabloqueador em crianças com MNC40.
Devido à frequencia aumentada de taquicardia ventricular e risco significativo de morte súbita, a avaliação de arritmias atriais e ventriculares pela monitorização ambulatorial do ECG deve ser realizada anualmente. No caso de arritmia ventricular sintomática e no contexto da função sistólica prejudicada, a prevenção de um evento sustentado e de arritmia potencialmente letal é indicada por meio de agentes antiarrítmicos ou de desfibriladores cardíacos implantáveis, de acordo com as diretrizes internacionais. Rastreamento ecocardiográfico dos familiares tem sido preconizado. Devido à grande prevalência de desordens neuromusculares relatadas em pacientes com MNC, avaliações neurológicas e musculoesqueléticas são também recomendadas.
O motivo pelo qual existe uma associação frequente entre não compactação e desordens neuromusculares é desconhecido. A prevalência de desordens neuromusculares foi de 82% em 49 pacientes com MNC que foram investigados neurologicamente32. Em alguns desses casos, o distúrbio neuromuscular ainda não tinha se manifestado clinicamente. Em tais casos, o diagnóstico da MNC pode levar ao diagnóstico neurológico, por isso, recomenda-se que os pacientes com MNC sejam submetidos a exames neurológicos, independentemente de terem ou não sintomas.
Oechslin e cols.7 relataram que certas características clínicas eram observadas mais frequentemente nos pacientes que foram a óbito, comparados aos sobreviventes com MNC, incluindo maior diâmetro diastólico final do ventrículo esquerdo, baixa fração de ejeção, classe funcional III ou IV (Nova York Heart Association), fibrilação atrial persistente ou permanente e bloqueio de ramo. Pacientes com essas características são de alto risco e candidatos precocemente às intervenções agressivas, incluindo consideração de cardiodesfibrilador implantável e avaliação para transplante.
O prognóstico dos pacientes com miocardiopatia não compactada é determinado pelo grau e progressão da insuficiência cardíaca, presença de eventos tromboembólicos e arritmias. Em uma série inicial, aproximadamente 60% dos pacientes sofreram morte súbita ou foram submetidos a transplante cardíaco, no prazo de seis anos após o diagnóstico4. De forma similar, em outra série de 34 adultos com MNC isolada, 47% daqueles pacientes morreram ou foram submetidos a transplante cardíaco, em um período de follow-up de 44 ± 39 meses7. A ocorrência de eventos embólicos, arritmias ventriculares e morte súbita parece ser consideravelmente menor nos doentes pediátricos26 quando comparada à subpopulação de adultos na descrição inicial de Chin e cols.2, apesar de aproximadamente 90% dos doentes seguidos em um período de dez anos desenvolverem disfunção ventricular esquerda. Recentemente, Murphy e cols.8 observaram melhoria no prognóstico, comparando-se ao que fora relatado em estudos prévios. Durante um período médio de 46 meses, encontrou-se uma morte em uma coorte de 45 pacientes com não compactação ventricular, que passou por um estreito acompanhamento clínico com intervalos regulares a cada seis meses em centro especializado.
Conclusão
A miocardiopatia não compactada é uma doença com diagnóstico crescente na prática clínica e que pode, em alguns casos, ter associação com outras anomalias cardíacas e sistêmicas, principalmente desordens neuromusculares. Sua apresentação clínica é altamente variável e pode ser assintomática em muitos casos, ou levar à insuficiência cardíaca grave e morte súbita em outros. A alta incidência de miocardiopatia não compactada verificada nos últimos anos, principalmente devido à melhora das técnicas ecocardiográficas e utilização da ressonância cardíaca, sugere que a hipertrabeculação ocorre também em outras comorbidades e que pode ser falsamente diagnosticada como não compactação ventricular41. Assim sendo, sugerimos que o diagnóstico de suspeita de não compactação miocárdica seja criteriosamente avaliado pelos métodos de imagem para evitar o diagnóstico inapropriado e exagerado.
Potencial Conflito de Interesses
Declaro não haver conflito de interesses pertinentes.
Fontes de Financiamento
O presente estudo não teve fontes de financiamento externas.
Vinculação Acadêmica
Não há vinculação deste estudo a programas de pós-graduação.
Artigo recebido em 09/11/09; revisado recebido em 16/03/10; aceito em 28/04/10.
- 1. Bellet S, Gouley BA. Congenital heart disease with multiple cardiac anomalies: report of a case showing aortic atresia, fibrous scar in myocardium and embryonal sinusoidal remains. Am J Med Sci. 1932,183:458-65.
- 2. Chin TK, Perloff JK, Williams RG, Jue J, Mohrmann R. Isolated noncompaction of left ventricular myocardium: a study of eight cases. Circulation. 1990,82(2):507-13.
- 3. Maron BJ, Towbin JA, Thiene G, Antzelevitch C, Corrado D, Arnett D, et al. Contemporary definitions and classification of the cardiomyopathies: an American Heart Association Scientific Statement from the Council on Clinical Cardiology, Heart Failure and Transplantation Committee; Quality of Care and Outcomes Research and Functional Genomics and Translational Biology Interdisciplinary Working Groups; and Council on Epidemiology and Prevention. Circulation. 2006;113(14):1807-16.
- 4. Ritter M, Oechslin E, Sutsch G, Attenhofer C, Schneider J, Jenni R. Isolated noncompaction of the myocardium in adults. Mayo Clin Proc. 1997;72(1):26-31.
- 5. Weiford BC, Subbarao VD, Mulhern KM. Noncompaction of the ventricular myocardium. Circulation. 2004;109(24):2965-71.
- 6. Jenni R, Wyss CA, Oechslin EN, Kaurmann PA. Isolated ventricular noncompaction is associated with coronary microcirculatory dysfunction. J Am Coll Cardiol. 2002;39(3):450-4.
- 7. Oechslin EN, Attenhofer Jost CH, Rojas JR, Kaufmann PA, Jenni R. Long-term follow-up of 34 adults with isolated left ventricular noncompaction: a distinct cardiomyopathy with poor prognosis. J Am Coll Cardiol. 2000;36(2):493-500.
- 8. Murphy RT, Thaman R, Blanes JG, Ward D, Sevdalis E, Papra E, et al. Natural history and familial characteristics of isolated left ventricular non-compaction. Eur Heart J. 2005;26(2):187-92.
- 9. Taylor GP. Cardiovascular system. In: Dimmick JE, Kalousek DK, eds. Developmental pathology of the embryo and fetus. Philadelphia, Pa: Lippincott; 1992. p. 467 508.
- 10. Zambrano E, Marshalko SJ, Jaffe CC, Hui P. Isolated noncompaction of the ventricular myocardium: clinical and molecular aspects of a rare cardiomyopathy. Lab Invest. 2002;82(2):117-22.
- 11. Finsterer J, Stollberger C, Feichtinger H. Histological appearance of left ventricular hypertrabeculation/noncompaction. Cardiology. 2002;98(3):162-4.
- 12. Conraads V, Paelinck B, Vorlat A, Goethals M, Jacobs W, Vrints C. Isolated non-compaction of the left ventricle: a rare indication for transplantation. J Heart Lung Transplant. 2001;20(8):904-7.
- 13. Daimon Y, Watanabe S, Takeda S, Hijikata Y, Komuro I. Two-layered appearance of noncompaction of the ventricular myocardium on magnetic resonance imaging. Circ J.2002;66(6):619-21.
- 14. Hamamichi Y, Ichida F, Hashimoto I, Uese KH, Miyawaki T, Tsukano S, et al. Isolated noncompaction of the ventricular myocardium: ultrafast computer tomography and magnetic resonance imaging. Int J Cardiovasc Imaging. 2001;17(4):305-14.
- 15. Lauer RM, Fink HP, Petry EL, Dunn MI, Diehl AM. Angiographic demonstration of intramyocardial sinusoids in pulmonary-valve atresia with intact ventricular septum and hypoplastic right ventricle. N Engl J Med. 1964;271:68-72.
- 16. Attenhofer Jost CH, Connolly HM, O'Leary PW, Warnes CA, Tajik AJ, Seward JB. Left heart lesions in patients with Ebstein anomaly. Mayo Clin Proc. 2005;80(3):361-8.
- 17. Friedberg MK, Ursell PC, Silverman NH. Isomerism of the left atrial appendage associated with ventricular noncompaction. Am J Cardiol. 2005;96(7):985-90.
- 18. Lilje C, Razek V, Joyce JJ, Rau T, Finckh BF, Weiss F, et al. Complications of non-compaction of the left ventricular myocardium in a paediatric population: a prospective study. Eur Heart J. 2006;27(15):1855-60.
- 19. Zaragoza MV, Arbustini E, Narula J. Noncompaction of the left ventricle: primary cardiomyopathy with an elusive genetic etiology. Curr Opin Pediatr. 2007;19(6):619-27.
- 20. Ichida F, Tsubata S, Bowles KR, Haneda N, Uese K, Miyawaki T, et al. Novel gene mutations in patients with left ventricular noncompaction or Barth syndrome. Circulation. 2001;103(9):1256-63.
- 21. Xing Y, Ichida F, Matsuoka T, Isobe T, Ikemoto Y, Higaki T, et al. Genetic analysis in patients with left ventricular noncompaction and evidence for genetic heterogeneity. Mol Genet Metab. 2006;88(1):71-7.
- 22. Vatta M, Mohapatra B, Jimenez S, Sanchez X, Faulkner G, Perles Z, et al. Mutations in cypher/ZASP in patients with dilated cardiomyopathy and left ventricular non-compaction. J Am Coll Cardiol. 2003;42(11):2014-27.
- 23. Sasse-Klaassen S, Probst S, Gerull B, Oechslin E, Nürnberg P, Heuser A, et al. Novel gene locus for autosomal dominant left ventricular noncompaction maps to chromosome 11p15. Circulation. 2004;109(22):2720-3.
- 24. Monserrat L, Hermida-Prieto M, Fernandez X, Rodríguez I, Dumont C, Cazón L, et al. Mutation in the alpha-cardiac actin gene associated with apical hypertrophic cardiomyopathy, left ventricular non-compaction, and septal defects. Eur Heart J. 2007;28(16):1953-61.
- 25. Conces DJ Jr, Ryan T, Tarver RD. Noncompaction of ventricular myocardium: CT appearance. Am J Roentgenol. 1991;156(4):717-8.
- 26. Ichida F, Hanamichi Y, Miyawaki T, Ono Y, Kamiya T, Akagi T, et al. Clinical features of isolated noncompaction of the ventricular myocardium: long-term clinical course, hemodynamic properties, and genetic background. J Am Coll Cardiol. 1999;34(1):233-40.
- 27. Hook S, Ratliff NB, Rosenkranz E, Sterba R. Isolated noncompaction of the ventricular myocardium. Pediatr Cardiol. 1996;17(1):43-5.
- 28. Pignatelli RH, McMahon CJ, Dreyer WJ, Denfield SW, Price J, Belmont JW, et al. Clinical characterization of left ventricular noncompaction in children: a relatively common form of cardiomyopathy. Circulation. 2003;108(21):2672-8.
- 29. Salerno JC, Chun TU, Rutledge JC. Sinus bradycardia, Wolff Parkinson White, and left ventricular noncompaction: an embrylogic connection? Pediatr Cardiol. 2008;29(3):679-82.
- 30. Jenni R, Oechslin E, Schneider J, Attenhofer Jost C, Kaufmann PA. Echocardiographic and pathoanatomical characteristics of isolated left ventricular non-compaction: a step towards classification as a distinct cardiomyopathy. Heart. 2001;86(6):666-71.
- 31. Frischknecht BS, Jost CH, Oechslin EN, Seifert B, Hoigné P, Roos M, et al. Validation of noncompaction criteria in dilated cardiomyopathy, and valvular and hypertensive heart disease. J Am Soc Echocardiogr. 2005;18(8):865-72.
- 32. Stollberger C, Finsterer J, Blazek G. Left ventricular hypertrabeculation/noncompaction and association with additional cardiac abnormalities and neuromuscular disorders. Am J Cardiol. 2002;90(8):899-902.
- 33. Rigopoulos A, Rizos IK, Aggeli C, Kloufetos P, Papacharalampous X, Stefanadis C, et al. Isolated left ventricular noncompaction: an unclassified cardiomyopathy with severe prognosis in adults. Cardiology. 2002;98(1-2):25-32.
- 34. Daimon Y, Watanabe S, Takeda S, Higikata Y, Komuro I. Two-layered appearance of noncompaction of the ventricular myocardium on magnetic resonance imaging. Circ J. 2002;66(6):619-21.
- 35. Petersen SE, Selvanayagam JB, Wiesmann F, Robson MD, Francis JM, Andersen RH, et al. Left ventricular non-compaction: insights from cardiovascular magnetic resonance imaging. J Am Coll Cardiol. 2005;46(1):101-5.
- 36. Kohli SK, Pantazis AA, Shah JS, Adeyemi B, Jackson G, McKenna WJ, et al. Diagnosis of left-ventricular noncompaction in patients with left-ventricular systolic dysfunction: time for a reappraisal of diagnostic criteria? Eur Heart J. 2008;29(1):89-95.
- 37. Stollberger C, Finsterer J. Pitfalls in the diagnosis of left ventricular hypertrabeculation/non-compaction. Postgrad Med J. 2006;82(972):679-83.
- 38. Alhabshan F, Smallhorn JF, Golding F, Musewe N, Freedom RM, Yoo SJ. Extent of myocardial non-compaction: comparison between MRI and echocardiographic evaluation. Pediatr Radiol. 2005;35(11):1147-51.
- 39. Bocchi EA, Braga FGM, Ferreira SMA, Rohde LEP, Oliveira WA, Almeida DR, et al/Sociedade Brasileira de Cardiologia. III Diretriz brasileira de insuficiência cardíaca crônica. Arq Bras Cardiol. 2009;93(1 supl.1):1-71.
- 40. Toyono M, Kondo C, Nakajima Y, Nakazawa M, Momma K, Kusakabe K. Effects of carvedilol on left ventricular function, mass, and scintigraphic findings in isolated left ventricular non-compaction. Heart. 2001;86(1):E4.
- 41. Sengupta PP, Mohan JC, Mehta V, Jain V, Arora R, Pandian NG, et al. Comparison of echocardiographic features of noncompaction of the left ventricle in adults versus idiopathic dilated cardiomyopathy in adults. Am J Cardiol. 2004;94(3):389-91.
Correspondência:
Datas de Publicação
-
Publicação nesta coleção
30 Ago 2011 -
Data do Fascículo
Jul 2011
Histórico
-
Revisado
16 Mar 2010 -
Recebido
09 Nov 2009 -
Aceito
28 Abr 2010