Resumos
O objetivo deste estudo é avaliar os efeitos do extrato de levedura (EPL) em dietas úmidas sobre a microbiota fecal, a produção de gás e a morfologia intestinal de gatos adultos. Foram utilizados 20 gatos adultos, de ambos os sexos, distribuídos ao acaso em quatro tratamentos: 1) dieta comercial úmida (controle); 2) controle + 0,2% de extrato de levedura em matéria seca; 3) controle + 0,4%; e 4) controle + 0,6%. Foram realizadas a microbiologia fecal, a avaliação da morfologia intestinal por meio de exames radiográficos, ultrassonográficos e de colonoscopia, bem como a biópsia para histologia intestinal. Não foram observadas diferenças significativas (p>0,05) para contagem de bactérias do ácido lático e de clostrídio sulfito redutor, área de gás em alças intestinais (avaliação radiográfica), espessura da parede do cólon (ultrassonografia intestinal) e contagem de colonócitos/células caliciformes (histologia). Por meio da colonoscopia, notaram-se alterações em características de mucosa em animais submetidos ao tratamento 4. Conclui-se que a adição de até 0,6% de EPL não teve efeito sobre os parâmetros avaliados, mas novos estudos são necessários para compreender os mecanismos de ação e os efeitos desse aditivo para gatos domésticos.
felinos; mucosa intestinal; clostrídios; lactobacilos; diagnóstico por imagem
The aim of this study is to evaluate the effects of yeast extract (EPL) in the moist diet on the fecal microbiotal, gas production and intestinal morphology of adult cats. Twenty adult cats from both sexes were randomly assigned to four treatments: 1) moist commercial diet (control); 2) control + 0,2% yeast extract dry matter; 3) control + 0,4%; and 4) control + 0,6%. Fecal microbiology and intestinal morphology were performed by radiographic, ultrasound, colonoscopy and intestinal biopsy exams for histology. There were no significant differences (P>0,05) for lactic acid bacteria counts and clostridium-reductor, gas area in the bowel (radiographic), wall thickness of the colon (ultrasound) and colonocytes count/globet cells (histology). Through colonoscopy, changes in characteristics of the intestinal mucosa in animals receiving treatment 4 were noticed. It is concluded that the addition of up to 0.6% EPL had no effect on the parameters evaluated, but further studies are needed to understand the action mechanisms and additive effects for domestic cats.
feline; intestinal mucosa; lactobacillus; clostridium; image diagnosis
MEDICINA VETERINÁRIA VETERINARY MEDICINE
A.A. AquinoI; F.M.O.B. SaadII; J.P.F. SantosI; C.A.L. LeiteII; G.R. SampaioII; M.A.R. FelicianoIII
IUniversidade de São Paulo - USP - São Paulo, SP
IIUniversidade Federal de Lavras - UFLA - Lavras, MG
IIIUniversidade Estadual Paulista - FCAV-Unesp - Jaboticabal, SP
RESUMO
O objetivo deste estudo é avaliar os efeitos do extrato de levedura (EPL) em dietas úmidas sobre a microbiota fecal, a produção de gás e a morfologia intestinal de gatos adultos. Foram utilizados 20 gatos adultos, de ambos os sexos, distribuídos ao acaso em quatro tratamentos: 1) dieta comercial úmida (controle); 2) controle + 0,2% de extrato de levedura em matéria seca; 3) controle + 0,4%; e 4) controle + 0,6%. Foram realizadas a microbiologia fecal, a avaliação da morfologia intestinal por meio de exames radiográficos, ultrassonográficos e de colonoscopia, bem como a biópsia para histologia intestinal. Não foram observadas diferenças significativas (p>0,05) para contagem de bactérias do ácido lático e de clostrídio sulfito redutor, área de gás em alças intestinais (avaliação radiográfica), espessura da parede do cólon (ultrassonografia intestinal) e contagem de colonócitos/células caliciformes (histologia). Por meio da colonoscopia, notaram-se alterações em características de mucosa em animais submetidos ao tratamento 4. Conclui-se que a adição de até 0,6% de EPL não teve efeito sobre os parâmetros avaliados, mas novos estudos são necessários para compreender os mecanismos de ação e os efeitos desse aditivo para gatos domésticos.
Palavras-chave: felinos, mucosa intestinal, clostrídios, lactobacilos, diagnóstico por imagem
ABSTRACT
The aim of this study is to evaluate the effects of yeast extract (EPL) in the moist diet on the fecal microbiotal, gas production and intestinal morphology of adult cats. Twenty adult cats from both sexes were randomly assigned to four treatments: 1) moist commercial diet (control); 2) control + 0,2% yeast extract dry matter; 3) control + 0,4%; and 4) control + 0,6%. Fecal microbiology and intestinal morphology were performed by radiographic, ultrasound, colonoscopy and intestinal biopsy exams for histology. There were no significant differences (P>0,05) for lactic acid bacteria counts and clostridium-reductor, gas area in the bowel (radiographic), wall thickness of the colon (ultrasound) and colonocytes count/globet cells (histology). Through colonoscopy, changes in characteristics of the intestinal mucosa in animals receiving treatment 4 were noticed. It is concluded that the addition of up to 0.6% EPL had no effect on the parameters evaluated, but further studies are needed to understand the action mechanisms and additive effects for domestic cats.
Keywords: feline, intestinal mucosa, lactobacillus, clostridium, image diagnosis
INTRODUÇÃO
A parede celular de levedura é dividida em duas frações: uma mais interna (constituída por quitina e 1,3 betaglucano), que corresponde a 50-60% do peso desta, e outra mais externa, contendo manoproteínas glicosiladas, das quais 50% são formadas pelo mananoligossacarídeo-MOS (Klis et al., 2002; Shetty e Jespersen, 2006). Essa constituição particular faz com que ela tenha capacidade de modular a microbiota intestinal com geração de benefícios, como melhoria do fluxo sanguíneo intestinal e hipertrofia dos colonócitos.
Sua atuação principal é como um sítio de ligação para determinadas bactérias Gram-negativas que apresentem resíduos de D-manose em suas fímbrias. Patógenos com fímbrias tipo 1 manose-específicas adsorvem o mananoligossacarídeo prontamente e deixam o intestino sem possibilidade de colonizá-lo (Ferket et al., 2002).
Estudos demonstram a efetividade desse prebiótico na modulação da microbiota de cães saudáveis e doentes (Swanson et al., 2002; Grieshop, 2003; Gouveia, 2006), mas há carência de pesquisas com gatos domésticos.
Dessa forma, os objetivos deste trabalho foram avaliar o efeito da inclusão de extrato da parede de levedura (nos níveis de 0; 0,2; 0,4 e 0,6% da matéria seca da dieta) na dieta úmida sobre a microbiota fecal (bactérias láticas e clostrídios), a produção de gás intestinal mensurada pela radiografia e a hipertrofia dos colonócitos da mucosa intestinal de gatos adultos.
MATERIAL E MÉTODOS
Foram utilizados 20 gatos adultos, sem raça definida, machos e fêmeas, com peso médio de 3,71±0,84kg, alojados em gaiolas metabólicas durante todo o período experimental. Os animais selecionados foram avaliados por meio de exame clínico antes e durante o ensaio experimental. O procedimento teve aprovação da Comissão de Ética em Experimentação Animal da Universidade Federal de Lavras.
O delineamento experimental foi o inteiramente ao acaso, com quatro tratamentos e cinco repetições, totalizando 20 unidades experimentais. A duração total do ensaio foi de 33 dias, sendo 23 dias de adaptação e os 10 últimos para coleta de dados. Os tratamentos fornecidos a cada um dos grupos foram: dieta comercial úmida padrão (controle) ou dieta comercial úmida + inclusão de 0,2; 0,4 ou 0,6% de EPL na matéria seca da dieta.
As quantidades de alimento oferecidas foram baseadas nas necessidades energéticas estimadas pela equação 100 x PV 0,67 (National..., 2006). O EPL foi misturado individualmente em cada um dos potes para alimentação, e a água foi fornecida à vontade.
A partir de 25º dia do período experimental, alíquotas de fezes frescas (coletadas até 15 minutos após a defecação) foram reservadas para mensuração de pH e análises microbiológicas.
A mensuração do pH de fezes recém-coletadas foi realizada por meio de potenciômetro digital Digimed após introdução direta do eletrodo nas fezes. Foram realizadas três medidas para cada uma das amostras, e o resultado médio foi utilizado segundo metodologia realizada por Swanson et al. (2002).
As análises microbiológicas da água, alimentos e fezes foram efetuadas no laboratório de microbiologia de alimentos do Departamento de Ciência dos Alimentos da Universidade Federal de Lavras.
A água foi avaliada quanto a sua potabilidade segundo a resolução número 518 de 2004 (Brasil, 2004). Tanto para água como para o alimento foram coletadas amostras para análises de coliformes totais e termotolerantes, seguindo metodologia descrita por Silva et al. (2001).
A análise das fezes procedeu-se com a contagem total de bactérias do ácido lático e de clostrídio sulfito redutor. Utilizou-se o meio de cultura ágar de Man, Rogosa e Sharpe (MRS) para avaliação das bactérias do ácido lático, e para clostrídios sulfito redutores utilizou-se o meio de cultura sulfito polimixina sulfadiazina ágar (SPS). A metodologia a que se procedeu é descrita por Silva et al. (2001). Após os procedimentos, realizou-se a contagem de colônias, e os resultados foram expressos em log de UFC/g de fezes.
Após o término do período de coleta de fezes, os gatos começaram a ser preparados para o exame de colonoscopia, por meio do qual foram feitas biópsias e obtidas amostras de tecido do cólon ascendente (porção mais proximal do intestino grosso e provavelmente mais susceptível à ação da parede de levedura suplementada e íntegra). Os animais receberam as suas dietas diluídas durante dois dias consecutivos, tendo sido submetidos a jejum alimentar um dia antes da realização do exame.
Para a colonoscopia, os gatos foram anestesiados com a associação de cloridrato de cetamina (Cetamin 10%, Syntec) e midazolam (Dormonid injetável, Roche). O exame foi realizado com o auxílio de endoscópio gradiente (Olympus modelo XQ10, com 9,8mm de diâmetro, canal de trabalho de 1,8mm e comprimento de 120cm). A técnica consistiu na introdução do endoscópio no reto do animal. Por meio da insuflação cautelosa das porções intestinais, respeitando-se os movimentos peristálticos, avaliou-se a mucosa quanto à coloração, ao aspecto, às lesões e às alterações morfológicas da porção examinada. O exame iniciou-se no reto, evoluindo até a porção da válvula ileocólica, com retorno do aparelho para a reavaliação da mucosa e a aspiração de ar.
As biópsias foram realizadas com auxílio de pinças, que coletavam fragmentos da mucosa intestinal dos gatos de aproximadamente 1,5cm2. As amostras foram imediatamente fixadas em dois frascos diferentes contendo solução de Karnovsky modificada segundo Alves (2004) e encaminhadas para a confecção de lâminas histológicas.
Os animais foram acompanhados até a recuperação da anestesia para serem conduzidos novamente ao gatil experimental, onde foram medicados por três dias consecutivos com 0,05mL/kg de sulfatrimetropim e meloxicam 0,2% via subcutânea.
As amostras do cólon ascendente foram coradas com hematoxilina e eosina (HE) conforme metodologia descrita por Fieri et al. (1997). As lâminas foram avaliadas em microscópio de luz Ken-a-vision T-110, com câmera acoplada a um sistema multimídia Q capture, em um computador, utilizando-se objetiva de 40x (aumento de 400x).
Foram selecionadas, de forma aleatória, 20 criptas intestinais por animal, sendo contadas todas as células epiteliais (colonócitos) e caliciformes presentes. O número total de cada um desses tipos celulares, a relação entre elas e suas características morfológicas foram avaliados.
No 30º dia do período experimental, os animais foram submetidos aos exames radiográficos e ultrassonográficos. Para o exame radiográfico, foram utilizados o aparelho Meditronix BR-200 e filmes Kodak® tamanho 24x30cm. Os animais foram radiografados na projeção laterolateral, sendo as radiografias reveladas, fixadas e interpretadas imediatamente após os exames.
Por meio das radiografias, avaliaram-se a área de produção de gás e o espessamento das alças intestinais utilizando-se medidas qualitativas (sistema de escore) e quantitativas (mensuração das áreas de gás).
Para a análise qualitativa, as radiografias foram classificadas em um sistema de pontuação de 1 a 3, em que 1 correspondia à pequena; 2, moderada; e 3, grande quantidade de gás nas alças intestinais, conforme descrito por Feliciano (2008), utilizando-se o software Image Processing and Analyses in Java (Image J®).
O exame ultrassonográfico foi realizado com o equipamento Toshiba SSH-140ª e transdutor de 5MHz. Os animais foram tricotomizados e, então, contidos em decúbito dorsal, sendo aplicado o gel acoplador específico, segundo a metodologia descrita por Biller et al. (1994). Por meio das imagens ultrassonográficas, avaliou-se a espessura da parede intestinal, mediante três mensurações, e a média delas foi utilizada para as análises estatísticas posteriores.
Os resultados foram analisados por meio do programa computacional SAS (Statistical..., 2004), sendo previamente verificada a normalidade dos resíduos pelo teste de Shapiro-Wilk (PROC UNIVARIATE) e as variâncias comparadas pelo teste de Hartley. Para dados não paramétricos, utilizou-se teste de Kruskal-Wallis, pelo PROC NPAR1WAY do SAS. Em todas as análises considerou-se um nível de significância de 5%.
RESULTADOS E DISCUSSÃO
A análise de coliformes totais e termotolerantes da água e a análise das dietas experimentais não acusaram a presença de microrganismos contaminantes.
Os resultados para o pH fecal, o número de bactérias láticas, a concentração de clostrídio sulfito redutor e a relação bactérias láticas/ clostrídio sulfito redutor nas fezes dos gatos estão demonstrados na Tab. 1.
No presente estudo, não houve diferença significativa da inclusão de EPL sobre os valores de pH, de bactérias ácido-láticas e clostrídio sulfito redutor nas fezes dos gatos (p>0,05). A relação entre bactérias láticas e clostrídio sulfito redutor também não foi afetada.
Sugere-se que as bactérias láticas da microbiota intestinal não utilizaram de maneira eficiente o extrato de parede de levedura, ou seja, não houve fermentação direta com condições metabólicas e bioquímicas adequadas para a redução do pH intestinal. Esses resultados contrariam os estudos desenvolvidos em cães por Zentek et al. (2002) e Middelbos et al. (2007), os quais verificaram diminuição significativa no pH fecal de animais alimentados com parede de levedura, entretanto ressalta-se que, nos dois ensaios, a dieta fornecida aos animais foi seca (concentração de proteína bruta menor). Dessa forma, a concentração de proteína bruta no alimento úmido utilizado neste estudo pôde alterar o metabolismo bacteriano, influenciando o estabelecimento da microbiota, conforme constatado por Zentek et al. (2004), ao estudarem o crescimento de Clostridium perfringens em cães, e por Backus et al. (2002) em felinos.
Outro ponto importante referente à composição do alimento fornecido consiste no fato de que as concentrações menores de carboidrato em alimentos úmidos podem interferir no padrão de fermentação, sendo que as bactérias láticas utilizam carboidratos como substrato para o seu crescimento e os teores são reduzidos (cerca de 25% da matéria seca) nas dietas úmidas.
De acordo com Swanson e Fahey Jr. (2001) e Vickers et al. (2001), o MOS seria moderadamente fermentado pelas bactérias intestinais. O principal mecanismo de ação do mananoligossacarídeo seria a eliminação das bactérias fímbrias tipo 1, o que diminui a competição desses microrganismos pela adesão na parede intestinal, facilitando o estabelecimento das bactérias láticas. No presente estudo, pôde-se observar crescimento satisfatório de bactérias láticas em todos os tratamentos.
A média de escores obtidos na avaliação colonoscópica foi mais alta com a utilização de 0,6% (2,8). Para o tratamento controle e 0,2%, as médias foram de 1,2, e para o tratamento 0,4% foi de 1,4 (P=0,0106). Esses resultados sugerem que uma resposta inflamatória não associada à modulação de microbiota ou a produtos secundários do metabolismo bacteriano foi induzida nos gatos que receberam o tratamento 0,6%.
Sabe-se que, normalmente, quando se utilizam níveis elevados de prebióticos fermentados pela microbiota intestinal, a agressão à mucosa é causada pelo excesso na produção de ácidos graxos de cadeia curta, especialmente o butirato. O sistema imune inato desempenha um papel na manutenção da integridade do intestino e na proteção contra uma ampla variedade de antígenos. Além de funcionar como uma primeira linha de defesa, também desencadeia uma série de sinais biológicos que estimula a resposta imune adaptativa a elaborar uma defesa contra o agente agressor (Turner et al., 2003; Nascimento et al., 2007). Corroborando essas afirmações, os resultados estão relacionados com mecanismos imunológicos que podem provocar vasodilatação, hiperemia e edema, vistos na mucosa dos gatos. Um estudo mais amplo dessas respostas imunológicas deve ser feito para confirmar essa hipótese.
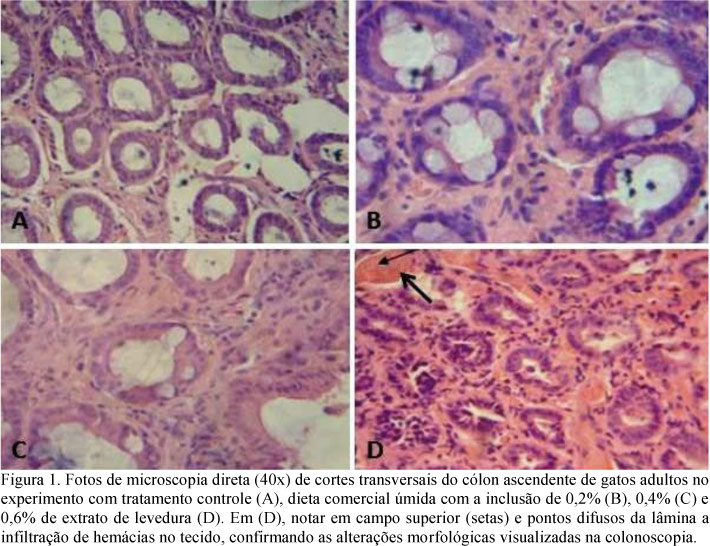
Por meio da avaliação histológica dos fragmentos intestinais, verificou-se que os animais que receberam o tratamento com 0,6% de EPL apresentaram infiltração de hemácias, corroborando a hiperemia observada durante a avaliação macroscópica pela colonoscopia (Fig. 1).
O número de colonócitos e o de células caliciformes, bem como a relação células caliciformes/colonócitos, são apresentados na Tab. 2.
Não houve diferença significativa (P>0,05) no número de células epiteliais com a inclusão de EPL na dieta. Observou-se um efeito desvio para o número de células caliciformes, tendo sido os maiores valores obtidos nos tratamentos 0,2 e 0,6%. O aumento no tratamento de 0,6% em relação ao controle e ao de 0,4% confirma a resposta inflamatória verificada, já que esse grupo celular (responsável pela síntese de muco) aumenta em situações em que a mucosa intestinal é agredida (Deplancke e Gaskins, 2001).
A relação entre colonócitos e células caliciformes apresentou-se com as mesmas características de efeito desvio, o que era esperado, já que as células epiteliais não sofreram efeito dos tratamentos.
As médias das áreas para as radiografias classificadas como escore 1,2 e 3 foram 10,34, 11,71 e 14,73cm2, respectivamente. Trabalhos anteriores realizados por Feliciano (2008) e Maia (2008) haviam demonstrado que as medidas apresentavam um alto coeficiente de variação (em torno de 70%), em parte pela falta de acurácia do programa em separar as áreas de gás (radiotransparentes) das regiões de tecidos moles. Neste sentido, uma delimitação prévia nas radiografias possibilitou a diminuição significativa do coeficiente de variação dos dados para cerca da metade do observado anteriormente.
Por tratar-se de uma metodologia nova, a medida em cm2 dificulta a comparação com outras pesquisas em que a avaliação da produção de gás foi realizada em volume (cm3). Conforme Feliciano (2008), os exames radiográficos em projeções ortogonais (laterolateral e ventrodorsal) podem oferecer a visualização mais ampla das alças intestinais, avaliando-se de forma mais efetiva a formação de gás nesses animais. A técnica de mensuração de gás via radiografia é promissora, no entanto alguns ajustes ainda precisam ser realizados para maior precisão dos resultados. As áreas de gás intestinal, bem como os respectivos escores, são apresentados na Tab. 3.
Não foram encontradas diferenças significativas para o escore em função da adição de EPL à dieta (P>0,05). A média geral de 1,95 indicou que houve produção moderada de gás intestinal em todos os animais. Tais resultados estão de acordo com os obtidos por Feliciano et al. (2010), que encontraram média geral de 1,75 ao verificarem o efeito de probióticos na produção de gás intestinal de cães, sem influência de tratamentos.
As áreas de gás em cm2 não se alteraram, o que difere dos resultados encontrados por Feliciano et al. (2010). É preciso considerar que a produção de gás é dependente da taxa de fermentação bacteriana, sendo que, no presente estudo, houve alteração nessa relação.
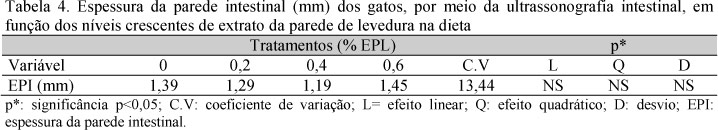
Os resultados deste experimento estão em discordância dos obtidos por Zentek et al. (2002) ao utilizar a metodologia in vitro para verificar a produção de gás pela microbiota intestinal de cães, exposta a diversos oligossacarídeos. Neste trabalho verificou-se o aumento na produção de gás com a suplementação de MOS quando comparadas a dietas padrão. No entanto, a ampla diversidade de metodologias empregadas não possibilita uma comparação fiel das duas pesquisas. As médias para as mensurações da parede do cólon dos gatos são apresentadas na Tab. 4.
As medidas verificadas apresentam-se dentro da normalidade para a espécie Newell (1994). Não foi observado efeito significativo da adição de EPL à dieta sobre a espessura da parede do cólon (P>0,05).
A ultrassonografia foi uma ferramenta diagnóstica auxiliar importante para a observação das camadas murais, pois trouxe informações iniciais sobre a saúde intestinal. Por tratar-se de um exame não invasivo, é uma alternativa vantajosa e poderia ser utilizada em novos estudos para avaliação do intestino de gatos domésticos. Essas características também foram descritas por Feliciano et al. (2010) em estudo com cães.
CONCLUSÃO
A inclusão de até 0,6% de EPL na dieta úmida não alterou a concentração fecal de clostrídios redutores e lactobacilos, bem como a produção de gás intestinal mensurado por técnicas radiográficas. A morfologia intestinal também não foi afetada, embora uma pequena reação inflamatória tenha sido notada nos animais submetidos à concentração mais alta de EPL na dieta (0,6% na matéria seca). Medidas alternativas para a mensuração de gás e coleta de amostras intestinais são promissoras na nutrição de pequenos animais devido a sua característica pouco invasiva, embora ajustes sejam necessários. São recomendados mais estudos para confirmação de efeitos, mecanismos de ação e doses ideais desse aditivo para felinos domésticos.
AGRADECIMENTOS
Ao Conselho Nacional de Desenvolvimento Científico e Tecnológico-CNPq, pela concessão da bolsa de doutorado; à Alltech do Brasil, pelo apoio financeiro à pesquisa.
Recebido em 21 de março de 2012
Aceito em 7 de maio de 2013
E-mail: marcusfeliciano@yahoo.com.br
- ALVES, E. Introdução a microscopia eletrônica de varredura. Lavras: UFLA, 2004. 43p.
- BACKUS, R.C.; PURYEAR, L.M.; CROUSE, B.A. et al Breath hydrogen concentrations of cats given commercial canned and extruded diets indicate gastrointestinal microbial activity vary with diet type. J. Nutr., v.132, p.1763-1766, 2002.
- BILLER, D.S.; PARTINGTON, B.P.; MIYABAYIASHI, T. et al Ultrasonographic appearance of the chronic hypertrophic pyloric gastropathy in the dog. Vet. Radiol. Ultrasound, v.35, p.30-33, 1994.
- BRASIL. Portaria Anvisa nº 518, de 25 de março de 2004. Estabelece os procedimentos e responsabilidades relativas ao controle e vigilância da qualidade da água para o consumo humano e seu padrão de potabilidade e outras providências. In: Diário Oficial [da] República Federativa do Brasil, Brasília, DF, n.59, p.266-270, 26 mar. 2004. Sessão 1.
- DEPLANCKE, B.; GASKINS, H.R.; Microbial modulation of innate defense: globet cells and the intestinal mucus layer. Am. J. Clinical Nutr., v.73, p.1131S-1141S, 2001.
- FELICIANO, M.A.R. Suplementação de probióticos para cães filhotes da raça Beagle recebendo alimentos comerciais. 2008. 105f. Dissertação (Mestrado em Zootecnia)- Universidade Federal de Lavras, Lavras.
- FELICIANO, M.A.R.; SAAD, F.M.O.B.; LEITE, C.A.L. et al Avaliações ultrassonográfica e radiográfica dos efeitos da suplementação com dois tipos de probióticos sobre o intestino de cães filhotes. Arq. Bras. Med. Vet. Zootec., v.62, p.1109 - 1116, 2010.
- FERKET, P.R.; PARKS, C.W.; GRIMES, J.L. Benefits of dietary antibiotic and mannanoligosaccharide supplementation for poultry. In: MULTI-STATE POULTRY FEEDING AND NUTRITION CONFERENCE, 16., 2002, Indianapolis. Proceedings... Indianapolis: University of Illinois, 2002. p.22.
- FIERI, W.J.; LEVADA, M.M.O.; PIVESSO, M.S.G. Apontamentos teóricos de citologia, histologia e embriologia. São Paulo: Catálise, 1997. 416p.
- GOUVEIA, E.M.S.; SILVA, I.S.; VAN ONSELEM, V.J. et al Use of mannanoligosaccharides as na adjuvant treatment of gastrointestinal diseases and this effects on E. coli inactivated in dogs. Acta. Cir. Bras., v.21, p.23-26, 2006.
- GRIESHOP, C.M. Diet may affect nutrition, immune system of pets. Feedstuffs, v.75, p.1-5, 2003.
- KLIS, F.M.; MOL, P.; HELLINGWERF, K. et al Dynamics of cell wall structure in Saccharomyces cerevisiae FEMS Microbiology Reviews, v.26, p.239-256, 2002.
- MAIA, G.V.C.; SAAD, F.M.O.B.; ROQUE, N.C. et al Zeólitas e Yucca schidigera em rações para cães: palatabilidade, digestibilidade, e redução de odores fecais. RBZ, v.39, p.2442-2446, 2010.
- MIDDELBOS, I.S.; GODOY, M.R.; FASTINGER, N.D. et al A dose-response evaluation of spray-dried yeast cell wall supplementation of dietsfed to adult dogs: effects on nutrient digestibility, immune indices, and fecal microbial populations. J. Anim. Sci., v.85, p.3022-3032, 2007.
- NASCIMENTO, D.B.D.; JUNQUEIRA, K.; NASCIMENTO, J.E.A Rapid restoration of colonic goblet cells induced by a hydrolyzed diet containing probiotics in experimental malnutrition. Acta Cir. Bras., v.22, p.72-76, 2007.
- NATIONAL Research Council. Nutrients requirements of dogs and cats. Washington: National Academy of Science, 2006. 398p.
- NEWELL, S.M.; GRAHAM, J.P.; ROBERTS, G.D. et al Sonography of the normal feline gastrointestinal tract. Vet. Radiol. Ultrasound, v.40, p.40-43, 1999.
- STATISTICAL Analysis Sistem - SAS INTITUTE. SAS user's guide: statistics. Version 9.1.1. Cary, 2004. Software.
- SHETTY, P.H.; JESPERSEN, L. Saccharomyces cerevisiae and lactic acid bacteria as potential mycotoxin decontaminating agents. Trends in Food Sci. Technol., v.17, p.48-55, 2006.
- SILVA, N.; JUNQUEIRA, V.C.A.; SILVEIRA, N.F.A. Manual de Métodos de Análises Microbiológicas de Alimentos 2. ed. São Paulo: Varela, 2001. 295p.
- SWANSON, K.S; FAHEY JUNIOR, G.C. Prebiotics in companion animal nutrition. In: BIOTECHNOLOGY IN THE FEED INDUSTRY, 18., 2002, Nottingham. Proceedings... Nottingham: Nottingham University, 2002. p.461-473.
- SWANSON, K.S.; GRIESHOP, C.M.; FLICKINGER, E.A. et al Supplemental fructoligossaccharides and mannanoligossacharides influence immune function, ileal and total tract nutrients digestibilities, microbial populations and concentrations of protein catabolites in the large bowel of dogs. J. Nutr., v.132, p.980-989, 2002.
- TURNER, M.W. The role of mannose-binding lectin in health and disease. Mol. Immunol., v.40, p.423-429, 2003.
- VICKERS, R.J.; SUNVOLD, G.D.; KELLEY, R.L. et al Comparison of fermentation of selected fructooligosaccharides and other fiber substrates by canine colonic microbiota. Am. J. Vet. Res., v.62, p.609-615, 2001.
- ZENTEK, J.; MARQUART, B.; PIETRZAK, T. Intestinal effects of mannanoligosaccharides, transgalactoligosaccharides, lactose and lactulose in dogs. JN, v.132, p.1682S-1684S, 2002.
- ZENTEK, J.; FRICKIE, S.; HEWICKER-TRAUTWEIN, M. et al Dietary protein source and manufacturing processes affect macronutrient digestibility, fecal consistency and presence of fecal Clostridium perfringens in adult dogs. J. Nutr., v.134, p.2158S-2161S, 2004.
Efeitos da parede de levedura em dieta úmida na microbiota fecal, na produção de gás e na morfologia intestinal de gatos adultos
Datas de Publicação
-
Publicação nesta coleção
07 Jan 2014 -
Data do Fascículo
Dez 2013
Histórico
-
Recebido
21 Mar 2012 -
Aceito
07 Maio 2013