Resumos
No Brasil, o desenvolvimento de medicamentos nanotecnológicos eficazes, seguros e com alta relação custo/benefício é estratégico para a Saúde Coletiva. A falta de informações requer uma regulação sanitária voltada à proteção da saúde e do ambiente. Objetiva-se identificar o estágio de desenvolvimento e o marco regulatório dos medicamentos nanotecnológicos e seus desafios no Brasil, enfatizando a segurança sanitária. Foi realizada uma análise documental em sítios de agências reguladoras, nacional e internacionais. Apesar da incipiente regulação destes medicamentos, foram encontrados 7 registrados, no Brasil, sem identificação clara na bula e na embalagem quanto às suas constituições nanotecnológicas, e 4 como medicamentos similares. A avaliação de risco e a regulação desses medicamentos exigem pessoas e equipamentos especializados, bem como a participação da sociedade na definição e implementação das políticas regulatórias. Sugere-se que a regulação considere o princípio da precaução, sendo o registro feito como medicamento novo e com informação na rotulagem e uso monitorado, de forma que sejam obtidos novos resultados sobre a avaliação de seu risco.
Nanotecnologia; Medicamentos nanotecnológicos; Inovação em saúde; Regulação sanitária; Vigilância sanitária
The development of effective and safe nanotechnology medication with a high cost-benefit ratio is a strategic imperative for public health in Brazil. The lack of information demands sanitary regulation geared to protecting health and the environment. This study seeks to assess the current stage of development, the regulatory framework and the challenges facing nanotechnology medication in Brazil, emphasizing sanitary surveillance. Document analysis was conducted in national and international regulatory agency sites. Despite the incipient regulation for this type of medication, 7 registered nanotechnology products were found in Brazil, without clear identification on leaflets or packaging regarding their nanotechnology composition, as well as 4 similar products. Risk assessment and regulation of such medication requires specialized personnel and equipment, as well as the participation of society in the formulation and implementation of regulatory policies. The suggestion proposed is that the regulatory framework should follow the precautionary principle, whereby products are registered as new medication with clear information on the labeling and controlled usage, until further results on the assessment of risk are obtained.
Nanotechnology; Nanotechnology medication; Innovation in health; Sanitary regulation; Sanitary surveillance
Introdução
A nanotecnologia consiste na utilização de materiais ou processos em que ao menos um de seus componentes possua uma de suas dimensões na escala nanométrica11. Melo CP, Pimenta M. Nanociências e nanotecnologia. Parcerias estratégicas 2004; 18:9-21.. A princípio, qualquer material pode ser reduzido ao tamanho nanométrico e essa nova tecnologia pode ser aplicada, de forma transdisciplinar, em qualquer campo de atuação, podendo influenciar toda a economia mundial22. Medeiros ES, Paterno LG, Mattoso LHC. Nanotecnologia. In: Durán N, Mattoso LHC, Morais PC, organizadores. Nanotecnologia Introdução, preparação e caracterização de nanomateriais e exemplos de aplicação. São Paulo: Artliber; 2006. p. 13-29..
Há acelerado crescimento e desenvolvimento dessa tecnologia e, atualmente, podem ser encontrados no mercado diversos produtos nanotecnológicos. A expectativa é que em 2015 o mercado da nanotecnologia atinja US$ 3,5 trilhões33. Agência Brasileira de Desenvolvimento Industrial (ABDI). Cartilha sobre nanotecnologia. 2010. [acessado 2010 dez 13]. Disponível em: http://www.abdi. com.br/?q=system/files/Cartilha.pdf.
http://www.abdi. com.br/?q=system/files/...
.
Uma das áreas de crescente desenvolvimento da nanotecnologia é a relacionada aos medicamentos, mais especificamente no desenvolvimento de novos sistemas de liberação de fármacos, tendo em vista as vantagens que apresentam em relação à liberação convencional e à projeção de seu crescimento. Acredita-se que, em 2015, os produtos terapêuticos nanotecnológicos representarão um mercado de US$ 3,4 bilhões44. Agência Brasileira de Desenvolvimento Industrial (ABDI). Nanotecnologia. Estudo Prospectivo Nanotecnologia: 2008-2025. (Sem Data). [acessado 2010 dez 14] Disponível em: http://www.abdi.com.br/?q=system/files/Relatorio_INI_ Nanotecnologia_Estudo+Prospectivo.pdf.
http://www.abdi.com.br/?q=system/files/R...
.
O Brasil tem interesse estratégico na nanotecnologia e muito já se tem investido em seu desenvolvimento. Na contramão dos países centrais, entretanto, pouco avançou na apropriada regulação dos medicamentos nanotecnológicos que já começam a entrar no mercado44. Agência Brasileira de Desenvolvimento Industrial (ABDI). Nanotecnologia. Estudo Prospectivo Nanotecnologia: 2008-2025. (Sem Data). [acessado 2010 dez 14] Disponível em: http://www.abdi.com.br/?q=system/files/Relatorio_INI_ Nanotecnologia_Estudo+Prospectivo.pdf.
http://www.abdi.com.br/?q=system/files/R...
. Foladori et al.55. Foladori G, Figueroa S, Edgard Z, Invernizz i N. Características distintivas del desarrollo de las nanotecnologias en América Latina. Sociologias 2012; 14(30):330-363. identificaram duas características no desenvolvimento da nanotecnologia na América Latina: a busca de melhor competitividade internacional com a criação de centros de excelência científica integrados com a indústria e a falta de atenção no que diz respeito à questão social, tais como a proteção de consumidores e trabalhadores frente a seus riscos potenciais e a não participação da sociedade nas decisões de política pública. Para os autores, não fazem parte das agendas da nanotecnologia na América Latina, mais especificamente México, Argentina e Brasil, três temas chaves de um desenvolvimento voltado à promoção da equidade e redução da pobreza, quais sejam: a participação dos movimentos sociais, a qualificação da força de trabalho e a confiança do consumidor. A participação de movimentos sociais na definição da Política de Ciência e Tecnologia a ser adotada neste âmbito, para além do Estado, empresários e pesquisadores, é importante para incorporar objetivos que estimulem o desenvolvimento de áreas com impacto mais direto no nível de vida da população. No que diz respeito à área farmacêutica, os profissionais devem conhecer como se faz a correta manipulação, quais os procedimentos de segurança e qual a infraestrutura adequada, de forma a evitar riscos à saúde e ao ambiente. O risco à saúde deve ser abordado igualmente no que diz respeito aos consumidores, já que apesar do conhecimento científico produzido, desde a década de noventa, sobre os riscos da nanotecnologia para a saúde humana e para o ambiente ter crescido, ainda permanece insuficiente55. Foladori G, Figueroa S, Edgard Z, Invernizz i N. Características distintivas del desarrollo de las nanotecnologias en América Latina. Sociologias 2012; 14(30):330-363..
No Brasil, as ações de regulação sanitária, visando à redução da nocividade ou risco para a saúde da população e do meio ambiente são atribuições do Sistema Nacional de Vigilância Sanitária (Visa), que tem o papel de regular a entrada deste tipo de medicamento no mercado, assim como fiscalizar e monitorar suas condições de produção, prescrição, comercialização, transporte, armazenamento e a ocorrência de eventos adversos advindos de seu uso66. Almeida Filho NA. O conceito de saúde e a Vigilância Sanitária: notas para a compreensão de um conjunto organizado de práticas de saúde. In: Costa AE, organizadora. Vigilância Sanitária desvendando o enigma. Salvador: EDUFBA; 2008. p. 19-43..
O objetivo deste trabalho foi identificar o estágio de desenvolvimento e o marco regulatório dos medicamentos nanotecnológicos e seus desafios no Brasil, enfatizando a segurança sanitária. Foi realizada análise documental, tendo como fonte de dados os sítios de agências reguladoras nacional (Agência Nacional de Vigilância Sanitária - Anvisa) e internacionais americana (Food and Drug Administration - FDA) e europeia (European Medicines Agency - EMA), bem como do Ministério da Ciência, Tecnologia e Inovação (MCTI), responsável pelo desenvolvimento da nanotecnologia no Brasil. Foi, também, realizada revisão bibliográfica de artigos científicos e legislações encontradas nas bases de dados PubMed, SciELO, Web of Science e Biblioteca Virtual em Saúde (BVS), utilizando as palavras chave: efeito adverso nano*, farmacovigilância, farmacovigilância limitações, farmacovigilância nano*, nano$ risco fármaco, nano$ risco, nanobiotecnologia, nano* fármacos, nano* segurança, nano* toxicidade, nanofármacos, nanomedicina, nanotecnologia, nanotoxicologia, pós comercialização nano*, vigilância pós comercialização nano*, regulamentação nano* e reação adversa nano*. A existência de medicamento nanotecnológico registrada na Anvisa foi considerada quando relatado em artigos e/ou quando constatado, no banco de registros da Anvisa, medicamento com a presença de um constituinte nanométrico. A busca do medicamento foi realizada pelo nome comercial, a partir de informação de medicamentos nanotecnológicos registrados no exterior.
Principais aspectos do desenvolvimento de medicamentos nanotecnológicos
A nanotecnologia baseia-se em materiais na nanoescala, sendo tão pequenos que podem apresentar propriedades químicas, físicas, biológicas e/ou comportamentais diferentes daquelas existentes nas macroescalas11. Melo CP, Pimenta M. Nanociências e nanotecnologia. Parcerias estratégicas 2004; 18:9-21.,22. Medeiros ES, Paterno LG, Mattoso LHC. Nanotecnologia. In: Durán N, Mattoso LHC, Morais PC, organizadores. Nanotecnologia Introdução, preparação e caracterização de nanomateriais e exemplos de aplicação. São Paulo: Artliber; 2006. p. 13-29.. Pode ser aplicada em praticamente todas as áreas da sociedade, sendo necessária para sua elaboração a integração de diversas disciplinas, ou seja, trata-se de uma tecnologia que envolve o conhecimento de forma transdisciplinar e multidisciplinar, respectivamente. Por essas características ela é considerada a via para a resolução de muitos dos problemas da atualidade22. Medeiros ES, Paterno LG, Mattoso LHC. Nanotecnologia. In: Durán N, Mattoso LHC, Morais PC, organizadores. Nanotecnologia Introdução, preparação e caracterização de nanomateriais e exemplos de aplicação. São Paulo: Artliber; 2006. p. 13-29.,77. Centro Ecológico. Nanotecnologia: A manipulação do invisível. Novas Tecnologias 2009; 44p.. Seu crescimento pode ser acompanhado pelo aumento do número de artigos e patentes sobre o assunto, já sendo o setor com o maior crescimento na quantidade de depósitos de patentes nas áreas de eletrônica e de medicamentos88. Nunes J. Pedidos de Patente sobre Nanotecnologia publicados no 1º semestre de 2010. INPI/DART/CEDIN/DIESPRO. Alerta Tecnológico nº 29; 2010. [acessado 2010 dez 14]. Disponível em: www.inpi. gov.br/menu-esquerdo/...em.../alerta_nano_jan_jun_2010.pdf.
www.inpi. gov.br/menu-esquerdo/...em.../...
,99. Nunes J, Rohem-Santos P. Pedidos de Patente sobre Nanotecnologia publicados no 2º semestre de 2009. INPI/DART/CEDIN/DIESPRO. Alerta Tecnológico nº 20; 2010. [acessado 14 dez. 2010]. Disponível em: http://www.inpi.gov.br/menu-esquerdo/informacao/alerta_nano_20.pdf.
http://www.inpi.gov.br/menu-esquerdo/inf...
. As patentes são depositadas a partir de seus países de origem ou naqueles com maior mercado para a tecnologia, sendo os de maior desenvolvimento e/ou mercado os Estados Unidos das Américas (EUA), o Japão, a China, a Coreia e a Alemanha88. Nunes J. Pedidos de Patente sobre Nanotecnologia publicados no 1º semestre de 2010. INPI/DART/CEDIN/DIESPRO. Alerta Tecnológico nº 29; 2010. [acessado 2010 dez 14]. Disponível em: www.inpi. gov.br/menu-esquerdo/...em.../alerta_nano_jan_jun_2010.pdf.
www.inpi. gov.br/menu-esquerdo/...em.../...
,99. Nunes J, Rohem-Santos P. Pedidos de Patente sobre Nanotecnologia publicados no 2º semestre de 2009. INPI/DART/CEDIN/DIESPRO. Alerta Tecnológico nº 20; 2010. [acessado 14 dez. 2010]. Disponível em: http://www.inpi.gov.br/menu-esquerdo/informacao/alerta_nano_20.pdf.
http://www.inpi.gov.br/menu-esquerdo/inf...
. Acredita-se que, em 2015, metade do setor farmacêutico mundial dependerá da nanotecnologia1010. Rossi-Bergman, B. A nanotecnologia: da saúde para além do determinismo tecnológico. Cienc Cult 2008; 60(2):54-57.. O Brasil, a partir de 2010, aparece em 13º lugar no ranking de países que tem prioridade para depósito de patentes relacionadas à nanotecnologia e desde 2008 ocupa essa mesma posição entre aqueles com prioridade para depósito de patentes relacionadas à nanobiotecnologia. Isso demonstra a presença brasileira no desenvolvimento de produtos ou processos relacionados à nanotecnologia e à nanobiotecnologia ou o interesse das firmas estrangeiras no mercado nacional88. Nunes J. Pedidos de Patente sobre Nanotecnologia publicados no 1º semestre de 2010. INPI/DART/CEDIN/DIESPRO. Alerta Tecnológico nº 29; 2010. [acessado 2010 dez 14]. Disponível em: www.inpi. gov.br/menu-esquerdo/...em.../alerta_nano_jan_jun_2010.pdf.
www.inpi. gov.br/menu-esquerdo/...em.../...
,99. Nunes J, Rohem-Santos P. Pedidos de Patente sobre Nanotecnologia publicados no 2º semestre de 2009. INPI/DART/CEDIN/DIESPRO. Alerta Tecnológico nº 20; 2010. [acessado 14 dez. 2010]. Disponível em: http://www.inpi.gov.br/menu-esquerdo/informacao/alerta_nano_20.pdf.
http://www.inpi.gov.br/menu-esquerdo/inf...
,1111. Nunes J, Rohem-Santos P. Pedidos de Patente sobre Nanobiotecnologia publicados no 2º semestre de 2008. INPI/DART/CEDIN/DIESPRO. Alerta Tecnológico nº 18; 2010. [acessado 14 dez. 2010]. Disponível em: http://www.inpi.gov.br/menu-esquerdo/ informacao/alerta_nanobio_n18.pdf.
http://www.inpi.gov.br/menu-esquerdo/ in...
.
A nanociência e a nanotecnologia (N&N), ou seja, o estudo e a aplicação dessa tecnologia, respectivamente, adquiriram maior notoriedade no Brasil a partir dos anos 2000, quando ocorreram as primeiras iniciativas do MCTI de reunir pesquisadores que já atuavam ou que tinham interesse na área1212. Fernandes MFM, Filgueiras CAL. Um panorama da nanotecnologia no Brasil (e seus macro-desa fios). Quim. Nova 2008; 31(8):2205-2213.. Em 2001, o governo criou quatro redes de pesquisa, que entre 2002 e 2005 envolveram 300 pesquisadores, 77 instituições de ensino e pesquisa, 13 empresas e resultaram na publicação de mais de 1000 artigos científicos e no depósito de mais de 90 patentes1212. Fernandes MFM, Filgueiras CAL. Um panorama da nanotecnologia no Brasil (e seus macro-desa fios). Quim. Nova 2008; 31(8):2205-2213.,1313. Brasil. Ministério da Ciência e Tecnologia (MCT). Nanotecnologia. Investimentos, Resultados e Demandas. 2006. [acessado 2010 dez 12]. Disponível em: http://www.mct.gov.br/upd_blob/0019/19536.pdf.
http://www.mct.gov.br/upd_blob/0019/1953...
. Nessa mesma época foi instituído o Programa de "Desenvolvimento da Nanociência e da Nanotecnologia" com o objetivo de desenvolver a competitividade da indústria nacional nesse setor1212. Fernandes MFM, Filgueiras CAL. Um panorama da nanotecnologia no Brasil (e seus macro-desa fios). Quim. Nova 2008; 31(8):2205-2213.,1313. Brasil. Ministério da Ciência e Tecnologia (MCT). Nanotecnologia. Investimentos, Resultados e Demandas. 2006. [acessado 2010 dez 12]. Disponível em: http://www.mct.gov.br/upd_blob/0019/19536.pdf.
http://www.mct.gov.br/upd_blob/0019/1953...
. Em 2005, esse programa foi fortalecido com o lançamento da Política Industrial, Tecnológica e do Comércio Exterior (PITCE) e com a criação da Ação Transversal de Nanotecnologia dos Fundos Setoriais. Suas ações foram inseridas em outro programa mais abrangente: Programa de "Ciência, Tecnologia e Inovação para a Política Industrial, Tecnológica e de Comércio Exterior" com o objetivo de fortalecer a PITCE. Nesse mesmo ano, com o objetivo de desenvolver a N&N, foi lançado o Programa Nacional de Nanotecnologia (PNN)1212. Fernandes MFM, Filgueiras CAL. Um panorama da nanotecnologia no Brasil (e seus macro-desa fios). Quim. Nova 2008; 31(8):2205-2213.. A partir de 2008, o investimento em pesquisa e desenvolvimento (P&D) da nanotecnologia foi considerado fundamental para elevar a competitividade da economia, uma vez que se espera que contribua de forma significativa para o desenvolvimento industrial do Brasil1414. Brasil. Ministério do Planejamento, Orçamento e Gestão (MPOG), Secretaria de Planejamento e Investimentos Estratégicos. Plano plurianual 2008-2011: projeto de lei. Brasília. MP 2007; 2: 540 p. [acessado 2010 dez 14]. Disponível em: http://www. sigplan.gov.br/download/avisos/001mensagempresidencial_internet.pdf.
http://www. sigplan.gov.br/download/avis...
,1515. Brasil. Ministério do Planejamento, Orçamento e Gestão (MPOG), Secretaria de Planejamento e Investimentos Estratégicos. Plano plurianual 2012-2015: projeto de lei. Brasília. MP 2011; 278 p. [acessado 2012 jul 19]. Disponível em: http://www. planejamento.gov.br/secretarias/upload/Arquivos/spi/PPA/2012/mensagem_presidencial_ppa.pdf
http://www. planejamento.gov.br/secretar...
.
Em julho de 2012 foi criado um Comitê Interministerial de Nanotecnologias com o intuito de subsidiar a criação de um Programa de Iniciativas Brasileira em Nanotecnologia, com o objetivo de promover seu desenvolvimento no país, principalmente pela integração das universidades com as indústrias. Acredita-se que a partir de 2013 cerca de R$ 40 milhões por ano serão destinados para esse programa1616. Martins C. MCTI prepara lançamento do programa Iniciativa Brasileira em Nanotecnologia. Boletim Eletrônico de Notícias da Sociedade Brasileira de Química de 19 de julho de 2012 - Nº 1034. [acessado 2012 jul 19]. Disponível em: http://boletim.sbq. org.br/noticias/n464.php
http://boletim.sbq. org.br/noticias/n464...
.
O Brasil prioriza o desenvolvimento da nanotecnologia em três mercados específicos: produtos farmacêuticos, químicos e cosméticos, levando em consideração as características de consumo do mercado interno, do desenvolvimento interno do setor químico e farmacêutico e de sua grande biodiversidade1717. Agência Brasileira de Desenvolvimento Industrial (ABDI). Panorama Nanotecnologia. Série Cadernos da Indústria ABDI. Volume XIX. Brasília; 2010. [acessado 2010 dez 14]. Disponível em: http://www.abdi .com.br/Estudo/PanoramadeNanotecnologia.pdf.
http://www.abdi .com.br/Estudo/Panoramad...
.
As indústrias farmacêuticas têm investido na pesquisa e no desenvolvimento de novos medicamentos nanotecnológicos, que possuem sistemas nanoestruturados de liberação de fármacos. Como resultante dessas novas possibilidades de liberação dos fármacos, tem-se como vantagens a redução dos efeitos adversos e da toxicidade do fármaco, proporcionando maior conforto ao paciente e consequentemente, maior adesão ao tratamento. Contudo, esses sistemas também podem apresentar algumas desvantagens, como: 1) toxicidade dos produtos ou dos metabólitos oriundos da sua biodegradação; 2) preço mais elevado, devido ao custo do processo tecnológico, que pode ser compensado pela redução das doses; e, 3) possibilidade de permear barreiras biológicas e atingir órgãos nobres como o cérebro1010. Rossi-Bergman, B. A nanotecnologia: da saúde para além do determinismo tecnológico. Cienc Cult 2008; 60(2):54-57..
Os benefícios das N&N têm sido estudados e bem caracterizados, mas seus riscos ainda permanecem uma questão em aberto1818. Chuankrerkkul N, Sangsuk S. Current Status of Nanotechnology Consumer Products and Nano-Safety Issues. JOM 2008, 18(1):75-79.. Essa falta de informações sobre os riscos advindos desta nova tecnologia é um dificultador para a tomada das decisões governamentais e a regulação da nanotecnologia1919. Barreto ML. O conhecimento científico e tecnológico como evidência para políticas e atividades regulatórias em saúde. In: Costa AE, organizadora. Vigilância Sanitária desvendando o enigma. Salvador: EDUFBA; 2008. p. 91-106..
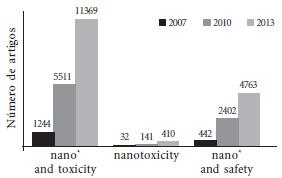
O interesse em estudar os riscos da N&N tem aumentado e isto pode ser comprovado pelo aumento no número de publicações referentes ao assunto, como pode ser visualizado na Figura 1 1818. Chuankrerkkul N, Sangsuk S. Current Status of Nanotechnology Consumer Products and Nano-Safety Issues. JOM 2008, 18(1):75-79..
Comparação de publicações referentes ao risco entre os anos de 2007, 2010 e 2013. Fonte: Chuankrerkkul e Sangsuk(18) e Web of Science(22).
Entretanto, estudar e pesquisar sobre os riscos da N&N não é uma tarefa fácil, já que é extremamente complicado definir quais características serão usadas para avaliação, pois muitas delas são importantes e podem influenciar nos seus efeitos, como: natureza do material, tamanho, forma, fisicoquímica de superfície, solubilidade, carga e outras2020. Williams RA, Kulinowski KM, White R, Louis G. Risk Characterization for Nanotechnology. Risk Anal 2010; 30(11):1671-1679..
A atual grande questão a ser resolvida em relação à nanotecnologia é como usufruir dos benefícios sem estar exposto aos seus riscos ainda pouco conhecidos.
Medicamentos Nanotecnológicos: regulação necessária?
Apesar de já existir muitos produtos nanotecnológicos no mercado, inclusive medicamentos, nem todos os países possuem uma regulação específica para esses produtos. Assim, a questão sobre a regulação da nanotecnologia não é se ela ocorrerá e sim quando e de qual forma2121. Marchant GE, Sylvester DJ, Abbott KW. What Does the History of Technology Regulation Teach Us about Nano Oversight? J Law Med Ethics 2009; 37(4):724-731..
Nos Estados Unidos da América, o FDA é o responsável pela regulação dos medicamentos. Um Grupo de Trabalho foi instituído em 2006, a fim de identificar formas de avaliar os riscos e os benefícios potenciais dos produtos nanotecnológicos que são regulamentados pelo FDA e recomendou a elaboração de um guia para orientar a indústria2323. Food and Drug Administration (FDA). FDA Continues Dialogue on 'Nano' Regulation. FDA Consumer Health Information / U. S. Food and Drug Administration. 2012. [acessado 2012 jul 20]. Disponível em: http://www.fda.gov/downloads/For Consumers/ConsumerUpdates/UCM258691.pdf
http://www.fda.gov/downloads/For Consume...
. A regulação dos produtos nanotecnológicos segue uma política focada nos produtos e com base científica, na qual as análises técnicas e as normas legais são específicas por produto. Além disso, o FDA tem fornecido orientações e assessoria técnica para as indústrias, bem como o controle dos produtos na pós-comercialização2424. Food and Drug Administration (FDA). Fact Sheet: Nanotechnology. Nanotechnology Overview. 2012. [acessado 2012 jul 20]. Disponível em: http:// www.fda.gov/Food/GuidanceComplianceRegulatoryInformation/GuidanceDocuments/ucm300914.htm-12k-2012-04-20
http:// www.fda.gov/Food/GuidanceComplia...
. A análise de risco varia de acordo com a classe do produto e leva em conta a segurança, a eficácia e o impacto na Saúde Pública. Essa é a mesma lógica de análise de outros produtos, pois se considera que a avaliação de segurança é suficientemente robusta. Entretanto, o FDA está investindo em um amplo programa de regulação da nanotecnologia a fim de reforçar suas capacidades científicas em avaliar as propriedades dos nanomateriais e o impacto que elas podem ter sobre os produtos2424. Food and Drug Administration (FDA). Fact Sheet: Nanotechnology. Nanotechnology Overview. 2012. [acessado 2012 jul 20]. Disponível em: http:// www.fda.gov/Food/GuidanceComplianceRegulatoryInformation/GuidanceDocuments/ucm300914.htm-12k-2012-04-20
http:// www.fda.gov/Food/GuidanceComplia...
. Também tem se buscado obter dados e orquestrar abordagens políticas para garantir a segurança e a eficácia dos produtos nanotecnológicos por meio da Iniciativa Nacional em Nanotecnologia (National Nanotechnology Initiative - NNI), em colaboração com a Casa Branca, com outras agências governamentais norte-americanas e com agências internacio nais de regulação2323. Food and Drug Administration (FDA). FDA Continues Dialogue on 'Nano' Regulation. FDA Consumer Health Information / U. S. Food and Drug Administration. 2012. [acessado 2012 jul 20]. Disponível em: http://www.fda.gov/downloads/For Consumers/ConsumerUpdates/UCM258691.pdf
http://www.fda.gov/downloads/For Consume...
.
Na União Europeia, a regulação dos medicamentos nanotecnológicos ocorre de forma semelhante pela EMA. Diversos documentos foram publicados visando a padronizar os conceitos e orientar as indústrias e pesquisadores a trabalhar conscientemente com a nanotecnologia. Alguns grupos estão se organizando para pesquisar sobre os riscos da nanotecnologia e as formas de avaliá-los. O Comitê Científico sobre Riscos à Saúde Emergentes e Recentemente Identificados (Scientific Committee on Emerging and Newly Identified Health Risks - SCENIHR) identificou a necessidade de uma análise caso a caso na avaliação dos riscos dos nanomateriais2525. European Union (UE). Commission Staff Working Paper. Types and uses of nanomaterials, including safety aspects. Accompanying the Communication from the Commission to the European Parliament, the Council and the European Economic and Social Committee on the Second Regulatory Review on Nanomaterials. Brussels: EU; 2012.. Desde 2006 a EMA tem analisado a aprovação de medicamentos nanotecnológicos e até o momento 20 já foram aprovados2525. European Union (UE). Commission Staff Working Paper. Types and uses of nanomaterials, including safety aspects. Accompanying the Communication from the Commission to the European Parliament, the Council and the European Economic and Social Committee on the Second Regulatory Review on Nanomaterials. Brussels: EU; 2012.. Esses medicamentos são analisados de acordo com a legislação farmacêutica vigente que se baseia na relação benefício/risco, sendo acompanhados após a comercialização2626. European Union (UE). Commission Staff Working Paper. Accompanying document to the Communication From The Commission To The European Parliament, The Council And The European Economic And Social Committee Regulatory Aspects Of Nanomaterials. Summary of legislation in relation to health, safety and environment aspects of nanomaterials, regulatory research needs and related measures. Brussels: EU; 2008..
No Brasil, a responsabilidade de aprovar a entrada no mercado e de regular este medicamentos é do Sistema Nacional de Vigilância Sanitária, em sua esfera federal, a Anvisa. É uma de suas principais e mais antigas áreas de atuação, estando envolvida em todas as etapas do desenvolvimento de medicamentos2727. Pepe VLE, Reis LGC, Noronha MF, Schramm JM. Avaliação em Saúde e Vigilância Sanitária: conceitos, estratégias e metodologias. In: De Seta MH, Pepe VLE, Oliveira GO, organizadores. Gestão e Vigilância Sanitária: modos atuais do pensar e fazer. Rio de Janeiro: Fiocruz; 2006. p. 251-276.. As iniciativas legislativas brasileiras iniciaram com o Projeto de Lei nº 5.076, de 2005, que procurou regulamentar a pesquisa e o uso da nanotecnologia no País, criar uma Comissão Técnica Nacional de Nanossegurança (CTNano), e instituir um Fundo de Desenvolvimento de Nanotecnologia (FDNano), entre outras providências2828. Brasil. Projeto de Lei No 5.076, de 2005. Deputado Edson Duarte. Brasília, DF. 2005. [acessado 2011 mar 25]. Disponível em: http://www.camara.gov.br/sileg/integras/297210.pdf.
http://www.camara.gov.br/sileg/integras/...
. Esse projeto foi elaborado, em colaboração com dezenas de especialistas, contemplando o desenvolvimento da nanotecnologia em diferentes campos e também sob diferentes aspectos. Recomendava medidas como o monitoramento dos produtos pelos detentores de seu registro após comercialização, a necessidade de identificação no rótulo do produto como nanotecnológico e o incentivo às pesquisas de avaliação de risco; dentre outras medidas que, se implementadas, facilitariam de forma acentuada o trabalho de regulação dos medicamentos nanotecnológicos2828. Brasil. Projeto de Lei No 5.076, de 2005. Deputado Edson Duarte. Brasília, DF. 2005. [acessado 2011 mar 25]. Disponível em: http://www.camara.gov.br/sileg/integras/297210.pdf.
http://www.camara.gov.br/sileg/integras/...
.
Esse projeto foi avaliado por três comissões diferentes da Câmara Federal, a saber: Comissão de Finanças e Tributação, Comissão de Desenvolvimento Econômico, Indústria e Comércio e Comissão de Ciência e Tecnologia, Comunicação e Informática. Todos os relatores deram pareceres desfavoráveis, seja por incompatibilidade e inadequação orçamentária e financeira, por falta de consenso entre o Executivo e o setor privado sobre como regulamentar a nanotecnologia no país ou por receio de que o controle de risco do projeto pudesse inibir os investimentos na área2929. Brasil. Câmara dos Deputados Comissão de Finanças e Tributação. Relatório do Projeto de Lei No 5.076, de 2005. Relator Deputado Duarte Nogueira. Brasília, DF. 2008a. [acessado 2011 mar 25]. Disponível em: http://www.camara.gov.br/sileg/integras/602144. pdf
http://www.camara.gov.br/sileg/integras/...
30. Brasil. Comissão de Ciência e Tecnologia, Comunicação e Informática. Relatório do Projeto de Lei No 5.076, de 2005. Relatora Deputada Luiza Erundina. Brasília, DF. 2008b. [acessado 2011 mar 25]. Disponível em: http://www.camara.gov.br/sileg/integras/567046.pdf
http://www.camara.gov.br/sileg/integras/...
-3131. Brasil. Comissão de Desenvolvimento Econômico, Indústria e Comércio. Relatório do Projeto de Lei No 5.076, de 2005. Relator Deputado Léo Alcântara. Brasília, DF. 2005. [acessado 2011 mar 25]. Disponível em: http://www.camara.gov.br/sileg/integras/315967.pdf
http://www.camara.gov.br/sileg/integras/...
. Os relatores ainda sugeriram que as preocupações com a questão do risco estariam contempladas em outros arcabouços regulatório-legais no país, como a Lei de Biossegurança, Lei nº 11.105, de 24 de Março de 2005, sendo que esta se restringe às pesquisas de organismos geneticamente modificados (OGM)3030. Brasil. Comissão de Ciência e Tecnologia, Comunicação e Informática. Relatório do Projeto de Lei No 5.076, de 2005. Relatora Deputada Luiza Erundina. Brasília, DF. 2008b. [acessado 2011 mar 25]. Disponível em: http://www.camara.gov.br/sileg/integras/567046.pdf
http://www.camara.gov.br/sileg/integras/...
31. Brasil. Comissão de Desenvolvimento Econômico, Indústria e Comércio. Relatório do Projeto de Lei No 5.076, de 2005. Relator Deputado Léo Alcântara. Brasília, DF. 2005. [acessado 2011 mar 25]. Disponível em: http://www.camara.gov.br/sileg/integras/315967.pdf
http://www.camara.gov.br/sileg/integras/...
-3232. Silva RP. A nova lei brasileira de biossegurança e o instituto da responsabilidade civil. Biblioteca juridical virtual del instituto de investigaciones jurídicas de la UNAM. 2007. [acessado 2010 dez 26]. Disponível em: http://www.juridicas.unam.mx.
http://www.juridicas.unam.mx...
. Também cita a Anvisa como responsável pela regulação no campo da saúde, ainda que não possa avaliar os riscos dos medicamentos nanotecnológicos e estabelecer, de forma precisa, sua segurança no momento de seu registro2929. Brasil. Câmara dos Deputados Comissão de Finanças e Tributação. Relatório do Projeto de Lei No 5.076, de 2005. Relator Deputado Duarte Nogueira. Brasília, DF. 2008a. [acessado 2011 mar 25]. Disponível em: http://www.camara.gov.br/sileg/integras/602144. pdf
http://www.camara.gov.br/sileg/integras/...
,3333. Caballero NED. Debate: Propaganda de produtos com nanopartículas. In: Emerick ME, Montenegro KBM, Degrave W, organizadores. Novas Tecnolo gias na Genética Humana: Avanços e Impactos para a Saúde. Rio de Janeiro: Fiocruz; 2007..
No caso da rotulagem, os relatores se basearam no Código de Defesa do Consumidor, Lei nº 8.078/91, e no Decreto nº 4.680/03 que determina os critérios para rotulagem de alimentos que possuam OGM para inferir que por analogia os produtos nanotecnológicos sejam corretamente identificados3030. Brasil. Comissão de Ciência e Tecnologia, Comunicação e Informática. Relatório do Projeto de Lei No 5.076, de 2005. Relatora Deputada Luiza Erundina. Brasília, DF. 2008b. [acessado 2011 mar 25]. Disponível em: http://www.camara.gov.br/sileg/integras/567046.pdf
http://www.camara.gov.br/sileg/integras/...
. Entretanto, observa-se que infelizmente essa analogia não está funcionando e que atualmente há, no mercado, produtos nanotecnológicos sem identificação.
Em 2010, foi elaborado o Projeto de Lei do Senado nº 131, que prevê a identificação por meio de símbolos e expressões a constituição nanotecnológica de alimentos, cosméticos, saneantes, medicamentos e correlatos3434. Brasil. Senado Federal. Projeto de Lei do Senado Nº 131, de 2010. Secretaria-Geral da Mesa. [acessado 2012 ago 14]. Disponível em: http://www.senado. gov.br/atividade/materia/detalhes.asp?p_cod_mate=96840.
http://www.senado. gov.br/atividade/mate...
. Em 2013 esse projeto foi rejeitado pela Comissão de Assuntos Sociais (CAS) e pela Comissão de Meio Ambiente, Defesa do Consumidor e Fiscalização e Controle (CMA)3535. Brasil. Senado Federal. Comissão de Assuntos Sociais. Parecer sobre o Projeto de Lei do Senado Nº 131, de 2010. Relator Senador Cícero Lucena. 2013. [acessado 2013 mar 27]. Disponível em: http://www. senado.gov.br/atividade/materia/getPDF.asp?t=124324&tp=1.
http://www. senado.gov.br/atividade/mate...
.
O registro desses medicamentos nanotecnológicos, como quaisquer outros novos medicamentos, deve ser feito pela Anvisa e constitui uma etapa fundamental na qual se deve avaliar a eficácia, a segurança e também o ganho terapêutico3636. Gava CM, Bermudez JAZ, Pepe VLE, Reis ALA. Novos medicamentos registrados no Brasil: podem ser considerados como avanço terapêutico? Cien Saude Colet 2010; 15(3):3403-3412.. Entretanto, a falta de regulamentação é um dificultador para a regulação dos medicamentos nanotecnológicos pela Anvisa, que por conse quência não tem como saber quais testes devem ser feitos a fim de garantir a segurança desses medicamentos, dificultando seu registro3333. Caballero NED. Debate: Propaganda de produtos com nanopartículas. In: Emerick ME, Montenegro KBM, Degrave W, organizadores. Novas Tecnolo gias na Genética Humana: Avanços e Impactos para a Saúde. Rio de Janeiro: Fiocruz; 2007..
Apesar disso, foi possível identificar ao menos 7 medicamentos nanotecnológicos registrados no Brasil até dezembro de 2012 (Quadro 1).
Quatro desses medicamentos, a despeito de serem nanotecnológicos, foram registrados na Anvisa como similares. É considerado medicamento similar, pelo Decreto nº 3.961 de 10 de outubro de 20013737. Brasil. Decreto nº 3.961, de 10 de outubro de 2001. Altera o Decreto no 79.094, de 5 de janeiro de 1977, que regulamenta a Lei no 6.360, de 23 de setembro de 1976. Diário Oficial da União 2001; 11 out., quando for equivalente ao registrado. O processo de encapsulação/complexação dos fármacos, seja por lipossomas, polímeros ou ciclodextrina, altera a biodisponibilidade desses medicamentos nanotecnológicos quando comparados com o de referência e é justamente essa diferença tida como sua vantagem. Assim, deveriam possuir atenção especial para o seu registro ou, no mínimo, serem registrados como medicamentos novos, já que este conceito, na Resolução RDC MS/ANVISA nº 136 de 20033838. Brasil. Ministério da Saúde (MS). Agência Nacional de Vigilância Sanitária (Anvisa). Resolução RDC nº 136, de 29 de maio de 2003. Dispõe sobre o registro de medicamento novo. Diário Oficial da União 2003; 12 ago., abrange o registro de produtos que possuam alteração na forma farmacêutica, concentração, via de administração e propriedades farmacocinéticas.
Outro agravante é a falta de uma identificação clara na bula desses produtos quanto às suas constituições nanotecnológicas, mesmo naqueles que foram registrados como medicamentos novos. Na bula destinada aos pacientes essa informação não consta em nenhum dos produtos, enquanto que naquela destinada aos profissionais há apenas a referência ao tamanho nanométrico daqueles constituídos por lipossomas. As embalagens também não indicam claramente tratar-se de um medicamento nanotecnológico. Ressalte-se, portanto, que devido à dificuldade de encontrar informações sobre a presença de constituintes nanométricos e a não referência a esta característica quando do registro do medicamento, limitou-se a busca, podendo haver outros registros não identificados. Sant'Anna et al.3939. Sant'Anna LS, Ferreira AP, Maria Alencar MSM. Patents, drug delivery and public health protection: health risk management for nanopharmaceuticals. J Technol Manag Innov 2013, 8(2):107-118. identificaram, também outros medicamentos nanotecnológicos comercializados no Brasil: Doxil(r) (doxorubicin), Amphocil(r) e Abelcet(r) (anfotericina B), Rapamune(r) (sirolimus), Emend(r) (aprepitant,MK869), TriCor(r) (fenofibrate), Megace ES(r) (megaestrol, acetato), Abraxane(r) (paclitaxel), Elestrin(r) (estradiol).
Como não há uma informação clara que esses medicamentos são nanotecnológicos nenhum monitoramento específico tem sido feito com seus usuários, não fornecendo valiosos dados para a avaliação da segurança desses medicamentos. Todos esses fatos evidenciam a necessidade de uma correta regulação dos medicamentos nanotecnológicos, para que estes possam entrar no mercado corretamente, de forma que todos os seus benefícios sejam aproveitados e seus riscos minimizados.
A VISA enfrenta desafios em relação às novas tecnologias, já que é sua competência regular boa parte daquelas em saúde e, inclusive, monitorar os eventos adversos (e riscos) dos recursos tecnológicos, produtos e serviços utilizados pelo sistema de saúde. No caso de medicamentos nanotecnológicos, há, além das dificuldades usuais, a ausência, a insuficiência ou a incerteza de informações científicas. Nestes casos, as decisões regulatórias devem levar em conta o princípio da precaução, o qual propõe o uso controlado dos medicamentos até que novos resultados sobre a avaliação do risco sejam obtidos, de forma a proteger o ambiente, o consumidor e também o trabalhador4040. Schulte PA, Salamanca-Buentello F. Ethical and scientific issues of nanotechnology in the workplace. Cien Saude Colet 2007, 12(5):1319-1332.,4141. Von Hohendorff R, Engelmann W, Oshirov M. As nanotecnologias no meio ambiente do trabalho: a precaução para equacionar os riscos do trabalhador. Cadernos Ibero-Americanos de Direito Sanitário 2013, 2(2):668-683.. No contexto do princípio da precaução, o gerenciamento de risco da nanotecnologia deve dar origem a estudos que façam uma análise do possível custo/benefício dos produtos nanotecnológicos que entrarão no mercado, permitindo que produtos com um risco aceitável entrem e tenham seus benefícios aproveitados, já que nem sempre é possível reduzir o risco a zero. Essa análise e a regulação de entrada e comercialização devem estar em constante atualização de acordo com novos dados científicos que surjam e devem ser realizadas de forma específica por categoria do produto. Para isso, é necessário desenvolver e incorporar métodos científicos de avaliação e gerenciamento de riscos, assim como técnicas que permitam a avaliação da eficácia, da segurança e da relação custo/benefício1919. Barreto ML. O conhecimento científico e tecnológico como evidência para políticas e atividades regulatórias em saúde. In: Costa AE, organizadora. Vigilância Sanitária desvendando o enigma. Salvador: EDUFBA; 2008. p. 91-106.. A VISA deve contar com laboratórios modernos e bem equipados, assim como com profissionais qualificados para fornecer resultados fidedignos na avaliação da qualidade de produtos e nas caracterizações de riscos e agravos para a saúde dos usuários4242. Costa EA, Rozenfeld S. Constituição da Vigilância Sanitária no Brasil. In: Rozenfeld S, organizador. Fundamentos da Vigilância Sanitária. Rio de Janeiro: Fiocruz; 2009. p. 15-40..
Em alguns países, as atividades de pesquisa estão vinculadas direta ou indiretamente ao Ministério da Saúde facilitando a articulação entre a produção do conhecimento científico, as decisões políticas e as atividades regulatórias no campo da saúde1919. Barreto ML. O conhecimento científico e tecnológico como evidência para políticas e atividades regulatórias em saúde. In: Costa AE, organizadora. Vigilância Sanitária desvendando o enigma. Salvador: EDUFBA; 2008. p. 91-106.. No Brasil, as pesquisas em nanotecnologia estão vinculadas ao MCTI, mas cabe à Anvisa o papel de avaliar os benefícios obtidos com o desenvolvimento científico e, ao mesmo tempo, agir de modo a garantir a precaução no domínio da saúde pública, permitindo assim que apenas medicamentos seguros entrem no mercado4343. Dallari SG. Vigilância Sanitária: Responsabilidade pública na proteção e promoção da saúde. In: Costa AE, organizador. Vigilância Sanitária desvendando o enigma. Salvador: EDUFBA; 2008. p. 45-52..
O fato do conceito brasileiro de biossegurança se restringir a pesquisas de organismos geneticamente modificados (OGM), de acordo com a Lei Federal nº 11.105, de 24 de março de 2005, também dificulta as ações de avaliação de risco das pesquisas em N&N3232. Silva RP. A nova lei brasileira de biossegurança e o instituto da responsabilidade civil. Biblioteca juridical virtual del instituto de investigaciones jurídicas de la UNAM. 2007. [acessado 2010 dez 26]. Disponível em: http://www.juridicas.unam.mx.
http://www.juridicas.unam.mx...
.
Outra ação da VISA e, portanto, desafio, é a ação de comunicação científica e técnica assim como a educação sanitária da população. Para isso, esta deve reunir informações científicas e apreender a percepção popular a fim de transmitir esses conhecimentos de forma compreensível para o público. Desta maneira pode contribuir para a construção de uma consciência sanitária, permitindo tanto a escolha quanto a aceitação de risco mais qualificada e dando meios de defesa contra inúmeros riscos e práticas nocivas do sistema produtivo4242. Costa EA, Rozenfeld S. Constituição da Vigilância Sanitária no Brasil. In: Rozenfeld S, organizador. Fundamentos da Vigilância Sanitária. Rio de Janeiro: Fiocruz; 2009. p. 15-40.. Entretanto, essa ação ainda parece ser tímida, especialmente em relação à N&N.
Há ainda o desconhecimento ou a baixa percepção do risco da nanotecnologia no meio acadêmico e nas indústrias farmacêuticas. Schulte e Salamanca-Buentello4040. Schulte PA, Salamanca-Buentello F. Ethical and scientific issues of nanotechnology in the workplace. Cien Saude Colet 2007, 12(5):1319-1332. destacaram como questões éticas para a saúde do profissional que trabalha com nanotecnologia a identificação e comunicação dos riscos por cientistas, autoridades e empregadores e sua aceitação por parte desses trabalhadores. Entretanto, ainda existem profissionais da área farmacêutica e biomédica que manipulam produtos nanotecnológicos apesar de não possuírem o conhecimento, a infraestrutura e as roupas adequadas para tal. O fato de a população não ter ainda informações suficientes é evidenciada pela ausência de organizações sociais nos processos decisivos para debater ou questionar as decisões governamentais, a fim de que as necessidades sociais sejam atendidas e não só os interesses econômicos55. Foladori G, Figueroa S, Edgard Z, Invernizz i N. Características distintivas del desarrollo de las nanotecnologias en América Latina. Sociologias 2012; 14(30):330-363..
Conclusão
Os desafios que a Anvisa terá para regular os medicamentos nanotecnológicos não difere muito daqueles que já enfrenta atualmente. Entretanto, no caso da nanotecnologia eles serão acentuados, pois os testes exigirão pessoas mais especializadas, equipamentos mais sofisticados e as avaliações de qualidade deverão abranger novos parâmetros como a caracterização do tamanho de partícula. Além disso, a falta de pesquisas e incentivos na caracterização dos riscos da nanotecnologia dificulta a avaliação e o gerenciamento pela Anvisa dos riscos dos medicamentos nanotecnológicos.
Tendo em vista essa falta de comprovação científica do risco, sugere-se que a regulação adotada deva ser baseada no princípio da precaução e que a avaliação de risco seja feita caso a caso, seguindo os modelos implantados pelo FDA e pela EMA. As principais ações que devem ser contempladas na regulação dos medicamentos nanotecnológicos são:
-
registro como medicamento novo
-
acompanhamento estreito do Programa de Farmacovigilância da indústria produtora
-
efetivação de programas de investigação dos efeitos toxicológicos dos medicamentos nanotecnológicos
-
comunicação à população e aos profissionais de saúde sobre a nanotecnologia e (a falta de informação sobre) seus efeitos, tanto pela inserção de informações no sítio da Anvisa como pela utilização de outras estratégias
-
obrigatoriedade de informar claramente na embalagem e na bula que se trata de um produto nanotecnológico
-
programa de monitoramento específico do desenvolvimento clínico e do uso do medicamento pelo produtor
Conclui-se que o principal desafio para a regulação da nanotecnologia consiste na conscientização de todos os atores envolvidos - pesquisadores, trabalhadores, reguladores, produtores e consumidores. Em face às insuficientes informações científicas sobre a segurança desses produtos, sugere-se que a regulação considere o princípio da precaução, sendo o registro feito como medicamento novo, a população e os profissionais de saúde informados e o uso monitorado de forma a que novos resultados sobre a avaliação de seu risco sejam obtidos e novos conhecimentos possam subsidiar a avaliação da decisão regulatória, de forma a ratificá-la se os benefícios se mostrarem superiores aos riscos ou, ao contrário, retificá-la em face à descoberta de graves eventos adversos oriundos de seu uso.
Referências
-
1Melo CP, Pimenta M. Nanociências e nanotecnologia. Parcerias estratégicas 2004; 18:9-21.
-
2Medeiros ES, Paterno LG, Mattoso LHC. Nanotecnologia. In: Durán N, Mattoso LHC, Morais PC, organizadores. Nanotecnologia Introdução, preparação e caracterização de nanomateriais e exemplos de aplicação. São Paulo: Artliber; 2006. p. 13-29.
-
3Agência Brasileira de Desenvolvimento Industrial (ABDI). Cartilha sobre nanotecnologia. 2010. [acessado 2010 dez 13]. Disponível em: http://www.abdi. com.br/?q=system/files/Cartilha.pdf.
» http://www.abdi. com.br/?q=system/files/Cartilha.pdf -
4Agência Brasileira de Desenvolvimento Industrial (ABDI). Nanotecnologia. Estudo Prospectivo Nanotecnologia: 2008-2025. (Sem Data). [acessado 2010 dez 14] Disponível em: http://www.abdi.com.br/?q=system/files/Relatorio_INI_ Nanotecnologia_Estudo+Prospectivo.pdf.
» http://www.abdi.com.br/?q=system/files/Relatorio_INI_ Nanotecnologia_Estudo+Prospectivo.pdf -
5Foladori G, Figueroa S, Edgard Z, Invernizz i N. Características distintivas del desarrollo de las nanotecnologias en América Latina. Sociologias 2012; 14(30):330-363.
-
6Almeida Filho NA. O conceito de saúde e a Vigilância Sanitária: notas para a compreensão de um conjunto organizado de práticas de saúde. In: Costa AE, organizadora. Vigilância Sanitária desvendando o enigma. Salvador: EDUFBA; 2008. p. 19-43.
-
7Centro Ecológico. Nanotecnologia: A manipulação do invisível. Novas Tecnologias 2009; 44p.
-
8Nunes J. Pedidos de Patente sobre Nanotecnologia publicados no 1º semestre de 2010. INPI/DART/CEDIN/DIESPRO. Alerta Tecnológico nº 29; 2010. [acessado 2010 dez 14]. Disponível em: www.inpi. gov.br/menu-esquerdo/...em.../alerta_nano_jan_jun_2010.pdf.
» www.inpi. gov.br/menu-esquerdo/...em.../alerta_nano_jan_jun_2010.pdf -
9Nunes J, Rohem-Santos P. Pedidos de Patente sobre Nanotecnologia publicados no 2º semestre de 2009. INPI/DART/CEDIN/DIESPRO. Alerta Tecnológico nº 20; 2010. [acessado 14 dez. 2010]. Disponível em: http://www.inpi.gov.br/menu-esquerdo/informacao/alerta_nano_20.pdf.
» http://www.inpi.gov.br/menu-esquerdo/informacao/alerta_nano_20.pdf -
10Rossi-Bergman, B. A nanotecnologia: da saúde para além do determinismo tecnológico. Cienc Cult 2008; 60(2):54-57.
-
11Nunes J, Rohem-Santos P. Pedidos de Patente sobre Nanobiotecnologia publicados no 2º semestre de 2008. INPI/DART/CEDIN/DIESPRO. Alerta Tecnológico nº 18; 2010. [acessado 14 dez. 2010]. Disponível em: http://www.inpi.gov.br/menu-esquerdo/ informacao/alerta_nanobio_n18.pdf.
» http://www.inpi.gov.br/menu-esquerdo/ informacao/alerta_nanobio_n18.pdf -
12Fernandes MFM, Filgueiras CAL. Um panorama da nanotecnologia no Brasil (e seus macro-desa fios). Quim. Nova 2008; 31(8):2205-2213.
-
13Brasil. Ministério da Ciência e Tecnologia (MCT). Nanotecnologia. Investimentos, Resultados e Demandas. 2006. [acessado 2010 dez 12]. Disponível em: http://www.mct.gov.br/upd_blob/0019/19536.pdf.
» http://www.mct.gov.br/upd_blob/0019/19536.pdf -
14Brasil. Ministério do Planejamento, Orçamento e Gestão (MPOG), Secretaria de Planejamento e Investimentos Estratégicos. Plano plurianual 2008-2011: projeto de lei. Brasília. MP 2007; 2: 540 p. [acessado 2010 dez 14]. Disponível em: http://www. sigplan.gov.br/download/avisos/001mensagempresidencial_internet.pdf.
» http://www. sigplan.gov.br/download/avisos/001mensagempresidencial_internet.pdf -
15Brasil. Ministério do Planejamento, Orçamento e Gestão (MPOG), Secretaria de Planejamento e Investimentos Estratégicos. Plano plurianual 2012-2015: projeto de lei. Brasília. MP 2011; 278 p. [acessado 2012 jul 19]. Disponível em: http://www. planejamento.gov.br/secretarias/upload/Arquivos/spi/PPA/2012/mensagem_presidencial_ppa.pdf
» http://www. planejamento.gov.br/secretarias/upload/Arquivos/spi/PPA/2012/mensagem_presidencial_ppa.pdf -
16Martins C. MCTI prepara lançamento do programa Iniciativa Brasileira em Nanotecnologia. Boletim Eletrônico de Notícias da Sociedade Brasileira de Química de 19 de julho de 2012 - Nº 1034. [acessado 2012 jul 19]. Disponível em: http://boletim.sbq. org.br/noticias/n464.php
» http://boletim.sbq. org.br/noticias/n464.php -
17Agência Brasileira de Desenvolvimento Industrial (ABDI). Panorama Nanotecnologia. Série Cadernos da Indústria ABDI. Volume XIX. Brasília; 2010. [acessado 2010 dez 14]. Disponível em: http://www.abdi .com.br/Estudo/PanoramadeNanotecnologia.pdf.
» http://www.abdi .com.br/Estudo/PanoramadeNanotecnologia.pdf -
18Chuankrerkkul N, Sangsuk S. Current Status of Nanotechnology Consumer Products and Nano-Safety Issues. JOM 2008, 18(1):75-79.
-
19Barreto ML. O conhecimento científico e tecnológico como evidência para políticas e atividades regulatórias em saúde. In: Costa AE, organizadora. Vigilância Sanitária desvendando o enigma. Salvador: EDUFBA; 2008. p. 91-106.
-
20Williams RA, Kulinowski KM, White R, Louis G. Risk Characterization for Nanotechnology. Risk Anal 2010; 30(11):1671-1679.
-
21Marchant GE, Sylvester DJ, Abbott KW. What Does the History of Technology Regulation Teach Us about Nano Oversight? J Law Med Ethics 2009; 37(4):724-731.
-
22Web of Science. [acessado 2010 dez 15 e 2013 mar 27]. Disponível em: http://apps.webofknowledge. com/UA_GeneralSearch_input.do?product=UA&search_mode=GeneralSearch&SID=R2SR2hVWJrfIwa JjMJJ&preferencesSaved=
» http://apps.webofknowledge. com/UA_GeneralSearch_input.do?product=UA&search_mode=GeneralSearch&SID=R2SR2hVWJrfIwa JjMJJ&preferencesSaved= -
23Food and Drug Administration (FDA). FDA Continues Dialogue on 'Nano' Regulation. FDA Consumer Health Information / U. S. Food and Drug Administration. 2012. [acessado 2012 jul 20]. Disponível em: http://www.fda.gov/downloads/For Consumers/ConsumerUpdates/UCM258691.pdf
» http://www.fda.gov/downloads/For Consumers/ConsumerUpdates/UCM258691.pdf -
24Food and Drug Administration (FDA). Fact Sheet: Nanotechnology. Nanotechnology Overview. 2012. [acessado 2012 jul 20]. Disponível em: http:// www.fda.gov/Food/GuidanceComplianceRegulatoryInformation/GuidanceDocuments/ucm300914.htm-12k-2012-04-20
» http:// www.fda.gov/Food/GuidanceComplianceRegulatoryInformation/GuidanceDocuments/ucm300914.htm-12k-2012-04-20 -
25European Union (UE). Commission Staff Working Paper. Types and uses of nanomaterials, including safety aspects. Accompanying the Communication from the Commission to the European Parliament, the Council and the European Economic and Social Committee on the Second Regulatory Review on Nanomaterials. Brussels: EU; 2012.
-
26European Union (UE). Commission Staff Working Paper. Accompanying document to the Communication From The Commission To The European Parliament, The Council And The European Economic And Social Committee Regulatory Aspects Of Nanomaterials. Summary of legislation in relation to health, safety and environment aspects of nanomaterials, regulatory research needs and related measures. Brussels: EU; 2008.
-
27Pepe VLE, Reis LGC, Noronha MF, Schramm JM. Avaliação em Saúde e Vigilância Sanitária: conceitos, estratégias e metodologias. In: De Seta MH, Pepe VLE, Oliveira GO, organizadores. Gestão e Vigilância Sanitária: modos atuais do pensar e fazer. Rio de Janeiro: Fiocruz; 2006. p. 251-276.
-
28Brasil. Projeto de Lei No 5.076, de 2005. Deputado Edson Duarte. Brasília, DF. 2005. [acessado 2011 mar 25]. Disponível em: http://www.camara.gov.br/sileg/integras/297210.pdf.
» http://www.camara.gov.br/sileg/integras/297210.pdf -
29Brasil. Câmara dos Deputados Comissão de Finanças e Tributação. Relatório do Projeto de Lei No 5.076, de 2005. Relator Deputado Duarte Nogueira. Brasília, DF. 2008a. [acessado 2011 mar 25]. Disponível em: http://www.camara.gov.br/sileg/integras/602144. pdf
» http://www.camara.gov.br/sileg/integras/602144. pdf -
30Brasil. Comissão de Ciência e Tecnologia, Comunicação e Informática. Relatório do Projeto de Lei No 5.076, de 2005. Relatora Deputada Luiza Erundina. Brasília, DF. 2008b. [acessado 2011 mar 25]. Disponível em: http://www.camara.gov.br/sileg/integras/567046.pdf
» http://www.camara.gov.br/sileg/integras/567046.pdf -
31Brasil. Comissão de Desenvolvimento Econômico, Indústria e Comércio. Relatório do Projeto de Lei No 5.076, de 2005. Relator Deputado Léo Alcântara. Brasília, DF. 2005. [acessado 2011 mar 25]. Disponível em: http://www.camara.gov.br/sileg/integras/315967.pdf
» http://www.camara.gov.br/sileg/integras/315967.pdf -
32Silva RP. A nova lei brasileira de biossegurança e o instituto da responsabilidade civil. Biblioteca juridical virtual del instituto de investigaciones jurídicas de la UNAM. 2007. [acessado 2010 dez 26]. Disponível em: http://www.juridicas.unam.mx.
» http://www.juridicas.unam.mx -
33Caballero NED. Debate: Propaganda de produtos com nanopartículas. In: Emerick ME, Montenegro KBM, Degrave W, organizadores. Novas Tecnolo gias na Genética Humana: Avanços e Impactos para a Saúde. Rio de Janeiro: Fiocruz; 2007.
-
34Brasil. Senado Federal. Projeto de Lei do Senado Nº 131, de 2010. Secretaria-Geral da Mesa. [acessado 2012 ago 14]. Disponível em: http://www.senado. gov.br/atividade/materia/detalhes.asp?p_cod_mate=96840.
» http://www.senado. gov.br/atividade/materia/detalhes.asp?p_cod_mate=96840 -
35Brasil. Senado Federal. Comissão de Assuntos Sociais. Parecer sobre o Projeto de Lei do Senado Nº 131, de 2010. Relator Senador Cícero Lucena. 2013. [acessado 2013 mar 27]. Disponível em: http://www. senado.gov.br/atividade/materia/getPDF.asp?t=124324&tp=1.
» http://www. senado.gov.br/atividade/materia/getPDF.asp?t=124324&tp=1 -
36Gava CM, Bermudez JAZ, Pepe VLE, Reis ALA. Novos medicamentos registrados no Brasil: podem ser considerados como avanço terapêutico? Cien Saude Colet 2010; 15(3):3403-3412.
-
37Brasil. Decreto nº 3.961, de 10 de outubro de 2001. Altera o Decreto no 79.094, de 5 de janeiro de 1977, que regulamenta a Lei no 6.360, de 23 de setembro de 1976. Diário Oficial da União 2001; 11 out.
-
38Brasil. Ministério da Saúde (MS). Agência Nacional de Vigilância Sanitária (Anvisa). Resolução RDC nº 136, de 29 de maio de 2003. Dispõe sobre o registro de medicamento novo. Diário Oficial da União 2003; 12 ago.
-
39Sant'Anna LS, Ferreira AP, Maria Alencar MSM. Patents, drug delivery and public health protection: health risk management for nanopharmaceuticals. J Technol Manag Innov 2013, 8(2):107-118.
-
40Schulte PA, Salamanca-Buentello F. Ethical and scientific issues of nanotechnology in the workplace. Cien Saude Colet 2007, 12(5):1319-1332.
-
41Von Hohendorff R, Engelmann W, Oshirov M. As nanotecnologias no meio ambiente do trabalho: a precaução para equacionar os riscos do trabalhador. Cadernos Ibero-Americanos de Direito Sanitário 2013, 2(2):668-683.
-
42Costa EA, Rozenfeld S. Constituição da Vigilância Sanitária no Brasil. In: Rozenfeld S, organizador. Fundamentos da Vigilância Sanitária. Rio de Janeiro: Fiocruz; 2009. p. 15-40.
-
43Dallari SG. Vigilância Sanitária: Responsabilidade pública na proteção e promoção da saúde. In: Costa AE, organizador. Vigilância Sanitária desvendando o enigma. Salvador: EDUFBA; 2008. p. 45-52.
Datas de Publicação
-
Publicação nesta coleção
Jul 2014
Histórico
-
Recebido
27 Mar 2013 -
Aceito
29 Jul 2013