RESUMO
O objetivo do trabalho foi avaliar a diminuição da replicação viral (BoHV-1 Colorado) em embriões murinos após tratamento do extrato etanólico da casca de Punica granatum (EEPg). Camundongos fêmeas Swiss com idade entre 6 e 8 semanas foram superovuladas com 0,2 mL a 5 UI de hormônios (eCG e hCG), e acasaladas com machos da mesma idade. Após 18 horas, as fêmeas sofreram eutanásia em câmara de CO2 e, através de abertura no peritônio, os zigotos foram coletados e lavados com solução de pronase 0,5%.Os zigotos foram divididos em quatro grupos: G1 (controle), G2 (expostos aos vírus BoHV-1 Colorado a 108 TCID50/mL), G3 (expostos ao EEPg) e G4 (expostos aos vírus e ao EEPg). Os grupos foram mantidos a 37,5ºC em meio TCM199 (100µL) com 10% de soro fetal bovino em estufa a 5% de CO2 e 95% de umidade. Após 24 h, analisamos a taxa de clivagem (teste exato de Fisher; p<0,05), a morfologia (por microscopia óptica), a nested-PCR e a titulação dos embriões em cocultura com células MDBK após mais 72 h do tratamento (teste de Mann-Whitney; p<0,05) e microscopia eletrônica de transmissão (ME). Os embriões murinos tratados com EEPg apresentaram resultados satisfatórios: sem alterações morfológicas, taxa de clivagem semelhante ao controle e, apesar da detecção da presença do vírus pela nested-PCR e ME, houve diminuição do título viral após tratamentos com esse extrato, o que sugere interferência desse tratamento no ciclo viral do BoHV-1 Colorado sem alterar o desenvolvimento dos embriões.
PALAVRAS-CHAVE:
extrato etanólico; romã; embriões murinos; BoHV-1; diminuição da replicação viral
ABSTRACT
The aim of this study was to evaluate the reduction of viral replication (Colorado BoHV-1) in murine embryos after the treatment of ethanol extract of Punica granatum peel (PgEE). Swiss female mice aged 6 to 8 weeks were superovulated with 0.2 mL of the 5 UI hormones (eCG and hCG) and mated with males of the same age. After 18 hours, the females were euthanized in a CO2 chamber, and through the opening in the peritoneum, zygotes were collected and washed with 0.5% pronase solution. The zygotes were divided into four groups: G1 (control), G2 (exposed to the virus Colorado BoHV -1 to 108 TCID50/mL), G3 (exposed to PgEE) and G4 (exposed to the virus and to PgEE). The groups were maintained at 37.5ºC in TCM199 (100 mL) with 10% fetal bovine serum in an incubator at 5% CO2 and 95% humidity. After 24 h, we analyzed the cleavage rate (Fisher's exact test; p<0.05), the morphology (by light microscopy), the nested-PCR and the titration of embryos in co-culture with MDBK cells after over 72 h of treatment (Mann-Whitney test; p<0.05) and transmission electron microscopy (TEM). The murine embryos treated with PgEE showed satisfactory results: no morphological changes, cleavage rate similar to controls, despite the detection of the presence of virus by nested PCR and TEM, there was a decrease of the viral titer after the treatment with this extract, which suggests interference of this treatment in the viral cycle BoHV-1 Colorado without altering the embryo development.
KEYWORDS:
ethanol extract; pomegranate; murine embryos; BoHV-1; reduction of viral replication
INTRODUÇÃO
A lavagem sequencial (LS) e o tratamento de tripsina (TT), tratamentos sugeridos e estabelecidos pela International Embryo Transfer Society (IETS) cuja finalidade é tentar impedir o deslocamento de patógenos junto aos embriões, durante a produção in vitro (PIV), até o momento da transferência embrionária em animais de produção não possuem eficácia. Inúmeros trabalhos demonstram a ineficiência desses tratamentos (Singh et al., 1982SINGH, E.L.; THOMAS, F.C.; PAPP-VID, G.; EAGLESOME, M.D.; HARE, W.C. Embryo transfer as a means of controlling the transmission of viral infections II: the in vitro exposure of preimplantation bovine embryos to infectious bovine rhinotracheitis virus. Theriogenology , v.18, n.2, p.133-140, 1982.; Stringfellow et al., 1990STRINGFELLOW, D.A.; LAUERMAN, L.H.; NASTI, K.B.; GALIK, P.K. Trypsin treatment of bovine embryos after in vitro exposure to infectious bovine rhinotacheitis virus or bovine herpes virus-4. Theriogenology v.34, n.3, p.427-434, 1990.; Palazzi, 2010PALAZZI, E.G. Efetividade da tripsina sobre embriões murinos infectados experimentalmente com BoHV-1 . 2010. 77f. Dissertação (Mestrado em Biotecnologia) - Instituto de Ciências Biomédicas, Universidade de São Paulo, São Paulo, 2010.), pois são limitados ao meio externo dos embriões (Stringfellow; Givens, 2000STRINGFELLOW, D.A.; GIVENS, M.D. epidemiologic concerns relative to in vivo and in vitro production of livestock embryos. Animal Reproduction Science , v.60-61, p.629-642, 2000.), não tendo efeito aos patógenos que já se encontram dentro das células, segundo inúmeros ensaios in vitro (Palazzi, 2010PALAZZI, E.G. Efetividade da tripsina sobre embriões murinos infectados experimentalmente com BoHV-1 . 2010. 77f. Dissertação (Mestrado em Biotecnologia) - Instituto de Ciências Biomédicas, Universidade de São Paulo, São Paulo, 2010.). Dentre os diversos patógenos com relevância, os herpesvírus bovinos configuram entre os agentes com distribuição mundial e importância econômica significativa (Colodel et al., 2002COLODEL, E.M.; NAKAZATO, L.; WEIBLEN, R.; MELLO, R.M.; SILVA, R.R.P.; SOUZA, M.A.; OLIVEIRA FILHO, J.A.; CARON, L. Meningoencefalite necrosante em bovinos causada por herpesvírus bovino no Estado de Mato Grosso, Brasil. Ciência Rural , v.32, n.2, p.293-298, 2002.; Kunrath et al., 2004KUNRATH, C.F.; VOGEL, F.S.F.; OLDONI, I.; FLORES, E.F.; WEIBLEN, R.; DEZENGRINI, R.; TORRES, F.D.; PAN, K.A. Soroneutralização e imunofluorescência utilizando anticorpos monoclonais no diagnóstico rápido de infecções pelo herpesvírus bovino tipos 1 e 5 (BHV-1 e BHV-5). Ciência Rural , v.34, n.6, p.1877-1883, 2004.). São inúmeras as doenças causadas pelos herpesvírus: rinotraqueíte infecciosa bovina (IBR), conjuntivite, vulvovaginite pustular infecciosa (IPV), balanopostite pustular infecciosa (IPB), reabsorção embrionária, aborto, infertilidade temporária, nascimento de animais fracos e infecções sistêmicas que podem resultar em meningoencefalite (Cerqueira et al., 2000CERQUEIRA, R.B.; CARMINATI, R.; SILVA, J.M.; SOARES, G.C.; MEYER, R.; SARDI, S. Serological survey for bovine herpesvirus 1 in cattle from different regions in the state of Bahia, Brazil. Brazilian Journal of Veterinary Research and Animal Science , v.37, n.6, p.1-8, 2000.; Vieira et al., 2003VIEIRA, S.; BRITO, W.M.E.D.; SOUZA, W.J.; ALFAIA, B.T.; LINHARES, D.C.L. Anticorpos para o herpesvírus bovino 1 (BHV-1) em bovinos do Estado de Goiás. Ciência Animal Brasileira , v.4, n.2, p.131-137, 2003.). Não há, até o momento, antivirais relacionados às células reprodutivas para serem usados em Centrais de Fertilização. Por isso, o objetivo deste trabalho foi o de avaliar a eficiência do extrato etanólico de Punica granatum (EEPg), in vitro, em relação à diminuição da replicação viral do BoHV-1 Colorado em embriões murinos pelas seguintes análises: morfologia, taxa de clivagem, nested PCR (n-PCR), cocultivo em células MDBK, titulação viral e microscopia eletrônica de transmissão (MET).
MATERIAL E MÉTODOS
Vírus
Foi utilizado o herpesvírus bovino tipo-1 (BoHV-1), estirpe Colorado, 7ª passagem em células MDBK, com título de 108 TCID 50/mL mantida em meio Eagle MEM sem soro fetal bovino à -80 oC. A amostra foi cedida, gentilmente, pelo Prof. Paulo Michel Roehe da Universidade Federal do Rio Grande do Sul, Instituto de Biociências, Departamento de Microbiologia.
Titulação dos vírus
Volumes de 0,1 mL contendo 3x104 (30 mil) células foram distribuídos em cada cavidade de placas de microtitulação com 96 poços. As placas foram incubadas a 37 a 38ºC em estufa com 5% de CO2 e, após 24 horas, lavadas com solução salina de Hanks. Os monoestratos foram inoculados com 0,1 mL de diluições de base 10 variando de 10-1 a 10-8 das amostras dos sobrenadantes das culturas e do lisado celular. As placas foram novamente incubadas nas condições já descritas e examinadas após 24 e 48 horas para a verificação da ocorrência de efeito citopático (CPE). Os títulos foram calculados em dose infectante por cultura de tecido 50% (TCID50/mL) expressa em logaritmo decimal (Reed; Muench, 1938REED, L.J.; MUENCH, H. A simple method of estimating fifty per cent endpoints. American Journal of Hygiene , v.27, n.3, p.493-497, 1938.).
Métodos de detecção do BoHV-1 em cultivo de células
As amostras foram inoculadas em monoestratos de células MDBK e, após 48 h de incubação a 38ºC em estufa com 5% de CO2 e 95% de umidade, foi verificada a presença ou não de CPE. O BoHV-1 Colorado induz um CPE focal, com arredondamento das células e subsequente lise (Palazzi, 2010PALAZZI, E.G. Efetividade da tripsina sobre embriões murinos infectados experimentalmente com BoHV-1 . 2010. 77f. Dissertação (Mestrado em Biotecnologia) - Instituto de Ciências Biomédicas, Universidade de São Paulo, São Paulo, 2010.).
Punica granatum
Arbusto ramoso de até 3 m de altura, com folhas simples, cartáceas, dispostas em grupo de 2 ou 3, de 4 a 8 cm de comprimento. Flores solitárias constituídas de corola vermelho-alaranjada e um cálice esverdeado, duro e coriáceo. Frutos do tipo baga, globoides, medindo até 12 cm, com numerosas sementes envolvidas por arilo róseo, cheio de um líquido adocicado. Provavelmente originária da Ásia e espalhada em toda a região do Mediterrâneo e cultivada em quase todo o mundo, inclusive no Brasil, onde recebe o nome de romã (Lorenzi; Matos, 2002LORENZI, H.; MATOS, F.J.A. Punica granatum L. In: LORENZI, H.; MATOS, F.J.A. Plantas medicinais no Brasil : nativas e exóticas. Nova Odessa: Instituto Plantarum de Estudo da Flora Ltda, 2002. p.394-395.). Seus frutos são comestíveis, sendo o pericarpo, que é a parte externa do fruto, usado para tratamento de inflamações na boca e na garganta. A análise fitoquímica dessa planta registra, além dos alcaloides, a presença de até 28% de taninos nas cascas do caule e dos frutos e, em menor quantidade, nas folhas; na semente foi registrada 7% de um óleo fixo, que entre seus ácidos graxos está principalmente o ácido punícico (Sousa et al., 1991SOUSA, M.P.; MATOS, F.J.A.; MATOS, M.E.O.; MACHADO, M.I.L.; CRAVEIRO, A.A. Constituintes químicos ativos e propriedades biológicas de plantas medicinais brasileiras . Fortaleza: UFC, 1991. 416p.). Os ensaios farmacológicos realizados com extratos do pericarpo mostraram atividade contra bactérias patogênicas e inibição do crescimento de tumores experimentais, enquanto os taninos do pericarpo se mostraram ativos contra o vírus HVS-2 do herpes genital, inibindo sua replicação e bloqueando, em cultura de células, a adsorção nas células já testadas (Lorenzi; Matos, 2002LORENZI, H.; MATOS, F.J.A. Punica granatum L. In: LORENZI, H.; MATOS, F.J.A. Plantas medicinais no Brasil : nativas e exóticas. Nova Odessa: Instituto Plantarum de Estudo da Flora Ltda, 2002. p.394-395.).
Extrato etanólico de Punica granatum (EEPg)
O pericarpo do fruto (2,5 kg) foi seco em estufa, triturado e colocado em béqueres, por 72 horas com etanol absoluto 97 ºGL. Após esse período, o líquido foi filtrado e colocado em pequeno balão e levado ao rotaevaporador. Sob pressão reduzida e temperatura de 50ºC houve a separação do extrato e o etanol. O solvente recuperado foi novamente adicionado às mesmas partes das plantas trituradas e submetido à maceração por mais 24 horas, sendo, em seguida, filtrado e evaporado, como descrito anteriormente. Esse procedimento foi repetido novamente, por mais duas vezes, num total de três extrações. Os extratos obtidos foram reunidos formando o extrato hidroalcoólico. Posteriormente, o extrato puro foi diluído em várias concentrações em solução fisiológica esterilizada para teste de toxicidade.
Coleta dos zigotos murinos
Foram utilizados 120 camundongos Swiss, púberes, nulíparas, com aproximadamente 8 semanas de idade. Após 48 h da superovulação ovariana das fêmeas com 0,2 mL (5 UI) de Gonadotrofina Coriônica Equina (eCG), as fêmeas receberam, também intraperitonealmente, 0,2 mL (5 UI) de Gonadotrofina coriônica humana (hCG) sendo, então, colocadas 2 fêmeas por macho para acasalamento. Após 18 h da aplicação do hCG para a coleta dos zigotos foi realizada a eutanásia em câmara de CO2 (CETEA-IB nº 088/09). Os zigotos foram lavados com TCM199 para remoção das células do cúmulos (Hogan et al., 1986HOGAN, B.; CONSTANTINI, F.; LACY, E. Developmental genetics and embryology of the mouse: past, present, and future. In: HOGAN, B.; CONSTANTINI, F.; LACY, E. (Eds.). Manipulating the mouse embryo : a laboratory manual. Cold Spring Harbor: Cold Spring Harbor Laboratory, 1986. p.12-14.) e separados em quatro grupos para as análises: G1 (zigotos não expostos aos vírus; controle), G2 (zigotos expostos a 10 µL de BoHV-1 Colorado a 108/mL TCID50/mL), G3 (grupo exposto a 10 µL de EEPg a 0,001% em solução salina esterilizada) grupo G4 (expostos a 10µL de BoHV-1 Colorado a 108/mL TCID50/mL e a 10µL de EEPg a 0,001% em solução salina esterilizada). Foram usados como parâmetros para as análises: aspectos morfológicos, taxa de clivagem, presença das partículas virais pela n-PCR e ECP dos zigotos em cocultura com células MDBK após 72 h.
Aspectos morfológicos
Foram analisadas as alterações morfológicas nos blastômeros e zona pelúcida dos embriões após 24 h por microscópio óptico invertido (Galuppo, 2005GALUPPO, A.G. Avaliação da sensibilidade de zigotos murinos à Brucella abortus para o estabelecimento de um modelo experimental em estudos de interações embriões-patógenos 2005. 74 f. Dissertação (Mestrado em Epidemiologia Experimental e Aplicada à Zoonozes) - Faculdade de Medicina Veterinária e Zootecnia, Universidade de São Paulo, São Paulo, 2005.).
Taxa de clivagem
Foi obtida pelo número de zigotos clivados pelo número de total de zigotos após 24 h. Foi utilizado o teste exato de Fisher para verificar a significância entre os grupos (α=0,05) (D'Angelo, 1998D'ANGELO, M. Interação do herpesvirus bovino tipo-1 (BoHV-1) com oócitos bovinos maturados in vitro. 1998. 52f. Tese (Doutorado em Microbiologia) - Departamento de Microbiologia do Instituto de Ciências Biomédicas, Universidade de São Paulo, São Paulo, 1998.).
Cocultivo dos zigotos em MDBK
Os embriões foram colocados em cocultivo com células MDBK para a análise da viabilidade viral, pelo ECP e titulação (REED; MUENCH, 1938REED, L.J.; MUENCH, H. A simple method of estimating fifty per cent endpoints. American Journal of Hygiene , v.27, n.3, p.493-497, 1938.), após 72 h. Foi utilizado o teste de Mann Whitney para verificar a significância entre os grupos (α=0,05) (Palazzi, 2010PALAZZI, E.G. Efetividade da tripsina sobre embriões murinos infectados experimentalmente com BoHV-1 . 2010. 77f. Dissertação (Mestrado em Biotecnologia) - Instituto de Ciências Biomédicas, Universidade de São Paulo, São Paulo, 2010.).
Extração do DNA
Para cada 75 µL de amostra de lavado de embrião de todos os grupos, foram adicionados 225 µL de Trizol LS Reagent(r) (Invitrogen), agitados em vórtex por 15 s, incubados a 30ºC durante 5 min. Foram adicionados 60 µL de clorofórmio (Merck(r)), homogeneizados e novamente incubadas à temperatura de 30ºC por 5 min. A mistura foi centrifugada a 12.000 x g a 4ºC, por 15 min. Descartou-se o sobrenadante e adicionaram-se 90 µL de etanol 100% (ETOH 100%), por 3 min. Foram centrifugados novamente (5 min a 5.000 x g). Em seguida o pellet foi lavado com 300 mL citrato de sódio em 10% de etanol e incubado por 15 min sob agitação constante. O sobrenadante foi descartado e o pellet lavado com 300 µL de etanol 75% e incubado por 10 min sob agitação constante (850 rpm) em temperatura ambiente e centrifugados por 5 minutos a 5.000 x gEsse passo foi repetido e depois do descarte do sobrenadante acrescentou-se 45 µL de NaOH para a ressuspensão do pellet . Os tubos foram centrifugados por 5 min a 12.000 x g a 4ºC. Transferiram-se para um novo tubo 30 µL do sobrenadante e acrescentaram-se 7,5 µL de uma solução tampão (HEPES). As amostras de DNA extraídas foram estocadas a -70ºC até a etapa de amplificação.
Iniciadores, PCR e n-PCR
A identificação do BoHV-1 foi realizada utilizando primers específicos desenhados a partir da região da glicoproteína I. Foi usado o kit comercial PCR Master Mix (PROMEGA) para PCR e n-PCR (Whitbeck et al., 1988WHITBECK, J.C.; BELLO, L.J.; LAWRENCE, W.C. Comparison of the bovine herpesvirus 1 gI gene and the herpes simplex virus type 1gB gene. Journal of Virology , v.62, n.9, p.3319-3327, 1988.). O volume total foi de 25 µL, contendo PCR Master Mix 1X (50u/mL Taq DNA Polymerase; 400 µM de cada DNTP e 3,0 mM MgCl2), 0,5 µM de cada primer e 5 µL de DNA. Para a reação de n-PCR, obteve-se volume total de 25 µL contendo PCR Master Mix (50u/mL Taq DNA Polymerase; 400 µM de cada DNTP e 3,0 mM MgCl2 ), 0,5 µM de cada primer e 2 µL de DNA já amplificado.
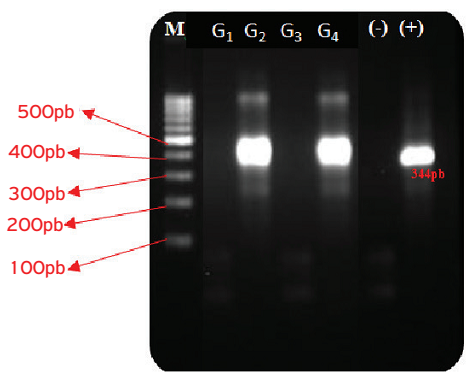
Cada amplificação foi analisada em gel de agarose a 2%, preparado em tampão TAE 1X e submetido à eletroforese. O tamanho dos fragmentos de DNA foi comparado com um padrão de peso molecular apresentando incrementos de 100 pb (DNA ladder de 100 pb - Fermentas(r)). O tamanho esperado do produto do PCR é de 468 bp, porém a reação de nPCR produz um produto de 344 bp.
Microscopia eletrônica
Para a MET, após o período de 24 h, os zigotos murinos foram lavados em PBS e fixados por 1 hora em glutaraldeído 2,5% em tampão PBS 0,1 M e pH 7,4. Foram emblocados em agarose 2% (blocos de aproximadamente 2 mm2) e preparados para serem cortados. Foram realizadas 3 lavagens de 15 min em tampão PBS seguida por pós-fixação em tetróxido de ósmio 1% em PBS durante 1 h e 3 lavagens de 15 min em água destilada. Imersão de 1 h em uranila a 0,5% em água destilada e novamente 3 lavagens de 15 min em água. Em seguida, para desidratação, 15 min de lavagem em acetona 50%, depois 15 min em acetona 70%, mais 15 min em acetona 90% e finalmente 2 banhos de 10 min seguidos por um último de 15 min em acetona 100%. Os zigotos murinos foram colocados na resina Spurr e após 72 h foram cortados com o ultramicrótomo em corte semifino (2 µm). Essas secções semifinas foram coradas com azul de toluidina a 2% em solução de borato de sódio 1% em água destilada. Para análise ultraestrutural os blocos foram seccionados e os cortes ultrafinos recolhidos em telas de níquel. As telas foram lavadas em BSA com Tween 20 em PBS, pH 7,0, incubadas em cloreto de amônio 5 Mm (para bloquear e evitar a ligação específica de anticorpos em grupamento aldeídico livre presente nas células fixadas) e lavadas em BSA com Tween 20 em PBS, pH 7,0. A seguir as telas foram incubadas com anticorpo primário 1:80 em PBS/BSA 1% por 4 h, lavadas em BSA com Tween 20 em PBS, pH 7,0, incubadas com anticorpo secundário (proteína A-ouro) 1:10 em PBS/BSA 1%, lavadas em PBS, pH 7,0 e fixadas com glutaraldeído 2,5% em água. Após lavagem em água as telas foram contrastadas com acetato de uranila e citrato de chumbo. No início e final do processamento as telas foram tratadas com metaperiodato de sódio (solução saturada) (Knutton, 1995KNUTTON, S. Electron microscopical methods in adhesion. Methods in Enzymology , v.253, p.145-158, 1995.; Padrón, 1998 apudAthayde, 2007ATHAYDE, C.S. Interação do parvovírus suíno com oócitos suínos durante o período de maturação in vitro. 2007. 52f. Dissertação (Mestrado em Biotecnologia) - Instituto de Ciências Biomédicas, Universidade de São Paulo, São Paulo, 2007.). As telas foram gravadas com auxílio do microscópio eletrônico de transmissão Jeol Jem 1010 no Instituto de Ciências Biomédicas/Universidade de São Paulo. Verificamos a morfologia dos zigotos/embriões murinos (Zona Pelúcida membrana plasmática, organelas e carioteca) e a presença das partículas virais após tratamento com EEPg.
Toxicidade do extrato etanólico da Punica granatum em células MDBK e em embriões murinos
Inicialmente foram realizados testes de toxicidade do EEPg em células MDBK com a finalidade de encontrar um parâmetro (ampla sintonia) para os testes definitivos de toxicidade em zigotos. O EEPg foi diluído em solução fisiológica esterilizada nas seguintes concentrações: 20; 15; 10; 5; 4; 3; 2; 1; 10-1; 10-2; 10-3; 10-4; 10-5; 10-6 e 10-7%. Um volume de 10 µL de cada uma das concentrações foi adicionado às células MDBK cultivadas em placas de 96 poços em estufa, durante 24 h, a 37ºC e 5% de CO2, sendo que cada poço continha 110 µL de meio de cultura TCM 199. Ao final, cada poço continha 120 µL (meio de cultura + extrato). Posteriormente, repetimos o teste com zigotos, no entanto, com concentrações do EEPg próximas à concentração não tóxica para células MDBK.
Teste do extrato etanólico da Punica granatum em embriões murinos infectados experimentalmente por BoHV-1
Os zigotos coletados, mantidos em gotas de meio TCM 199 suplementado com 10% de soro bovino fetal (SBF) livre do vírus da diarreia viral bovina (BVDV) e BoHV-1 e 0,2% de piruvato de sódio, sob óleo mineral esterilizado, foram divididos nos seguintes grupos: controle (G1; com 100 µL de meio TCM199 + 10% de SFB + 20 µL de solução fisiológica esterilizada), expostos aos vírus (G2; com 100 µL de meio TCM199 + 10% de SFB + 10 µL da suspensão de vírus com título de 108 TCID50/mL + 10 µL de solução fisiológica esterilizada); expostos ao EEPg (G3: com 100 µL de meio TCM199 + 10% de SFB + 10 µL de EEPg a 0,001% + 10 µL de solução fisiológica esterilizada); expostos aos vírus e ao EEPg (G4; com 100 µL de meio TCM199 + 10% de SFB + 10 µL de EEPg a 0,001% + 10 µL da suspensão de vírus com título de 108 TCID50/mL).
As culturas foram mantidas em estufa a 5% de CO2, 90% de umidade e 37ºC. Após 24 h de contaminação os zigotos foram separados em subgrupos para avaliação da morfologia, taxa de clivagem, cocultivo em MDBK e ME.
Este trabalho foi realizado conforme os princípios éticos da experimentação animal estabelecidos pela Comissão de Ética na Experimentação Animal (CETEA-IB) conforme consta em declaração de 27/11/13, sob o protocolo nº 124/12.
RESULTADOS
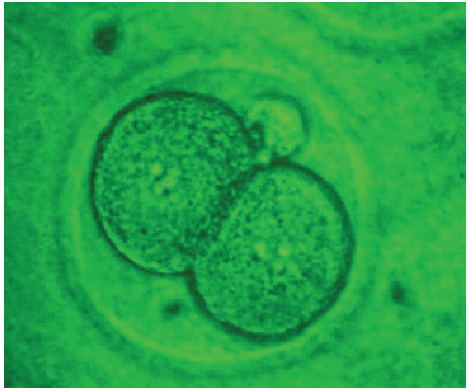
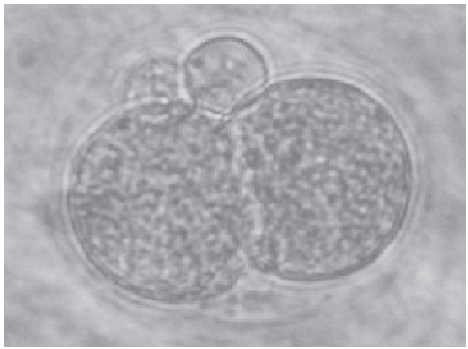
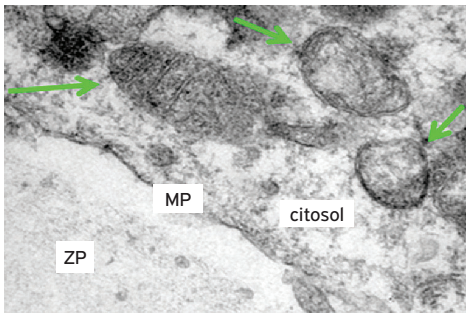
Os grupos G1, G3 e G4 (grupos teste) não apresentaram embriões com alterações morfológicas após 24, 48 e 96 h (Figs. 1, 3, 4 e 5). O grupo G2 apresentou alterações morfológicas, como falha na divisão e aumento do espaço periplasmático (Fig. 2). Após 24 h, foram constatadas as seguintes taxas de clivagens: G1 igual a 76% (254/336); G2 igual a 63% (234/370); G3 igual a 72% (75/104) e G4 igual a 75% (206/274). Não foi constatada diferença significativa (p<0,05) com relação à taxa de clivagem entre os grupos G1 x G2; G1 x G3 e G1 x G4. As médias relacionadas a quatro titulações da cocultura dos embriões em células MDBK (G2=107 TCID50/mL e G4=102 TCID50/mL) apresentaram diferença significativa (p<0,05). A incubação dos embriões do grupo G4 tratados com EEPg em células MDBK apresentaram ECP discreto (Fig. 7), que é compatível com diminuição das partículas virais constatada pela titulação viral após 72 h. Segundo a n-PCR, os grupos G1 e G3 apresentaram resultados negativos, enquanto G2 e G4, positivos (Fig. 8). Após análise da ME, foi possível verificar a conservação das principais estruturas celulares (zona pelúcida, membrana plasmática, mitocôndria e carioteca) dos embriões do grupo teste (G4) (Figs. 13, 14 e 15), apesar do abaulamento da membrana plasmática (Fig. 15). Não foi possível a detecção das partículas virais no grupo G4, somente no grupo G2 (Fig. 12). A perturbação da membrana plasmática também foi detectada no grupo G2 (Fig. 10). As Figuras 9 e 11 demonstram as "estruturas" conservadas do grupo controle (G1).
Embrião do grupo G1 (controle) sem alterações morfológicas após 24 h de incubação. É possível verificar a zona pelúcida íntegra e o corpúsculo polar (100x, 5,7x zoom).
Embrião exposto aos vírus (Grupo G2) sem clivagem após 24 h de incubação. Aumento do espaço periplasmático (seta em vermelho) (100x, 5,7x zoom).
Embrião exposto aos ao extrato etanólico da casca de Punica granatum_(G3), blastômeros simétricos, com citoplasma uniforme após 24 h de incubação. Presença dos dois corpúsculos polares na região apical da foto (100x, 5,7x zoom).
Embrião exposto aos vírus e ao extrato etanólico da casca de Punica granatum (Grupo G4) após 48 h de incubação. Com duas clivagens e quatro células (100x, 5,7x zoom).
Embrião exposto aos vírus e ao extrato etanólico da casca de Punica granatum_(Grupo G4) após 72h de incubação. Com três clivagens e oito células (100x, 5,7x zoom).
Monocamadas de células MDBK em cultura com TCM199 acrescentado em 10% de soro bovino fetal (100x, 4x zoom).
Cultura MDBK inoculadas com embrião do grupo G4 (Punica granatum) com "discreto efeito citopático" (seta) (100x, 4,1x zoom)
Nested PCR. M: padrão de peso molecular DNA ladder de 100 pb; G1 : controle; G2: exposto aos vírus; G3: exposto ao extrato etanólico da casca de Punica granatum; G4: exposto aos vírus e ao extrato etanólico da casca de Punica granatum; (-): controle negativo; (+): controle positivo.
Embrião do grupo controle (Grupo G1). ZP: zona pelúcida; MP: membrana plasmática. Todas estruturas conservadas. Aumento: 7.500x.
Embrião exposto aos vírus (Grupo G2). ZP: zona pelúcida; MP: membrana plasmática. Note (seta) perturbação da membrana plasmática. Aumento: 30.000x.
Embrião do grupo controle G1. Em destaque hetreocromatina (seta); C: carioteca íntegra. Aumento: 30.000x.
Embrião exposto aos vírus (Grupo G2). Destaque para as partículas virais (setas verdes) encontradas no citosol. Aumento: 120.000x.
Embrião exposto aos vírus e ao extrato etanólico da casca de Punica granatum (Grupo G4). ZP: zona pelúcida; MP: membrana plasmática. Todas estruturas conservadas. Aumento: 4.000x.
Embrião exposto aos vírus e ao extrato etanólico da casca de Punica granatum (Grupo G4). ZP: zona pelúcida; MP: membrana plasmática. Setas verdes: mitocôndrias. Todas as estruturas conservadas. Aumento: 20.000x.
Embrião exposto aos vírus e ao extrato etanólico da casca de Punica granatum (Grupo G4). ZP: zona pelúcida; MP: membrana plasmática. Setas vermelhas: perturbação da membrana plasmática, porém, sem rompimento. Setas verdes: mitocôndrias preservadas. Aumento: 20.000x.
DISCUSSÃO
A produção in vitro (PIV) tem sido difundida em diversos países e de forma destacada no Brasil a partir da década de 1990, sendo que hoje o Brasil é reconhecido internacionalmente pela técnica de Fertilização in vitro. Paradoxalmente, a biotecnologia da reprodução, que permite maior controle das células reprodutivas, pode ao mesmo tempo ser disseminadora de patógenos com maior rapidez e fornecer prejuízos consideráveis em escala mundial (Stringfellow et al., 2004STRINGFELLOW, D.A.; GIVENS, M.D.; WALDROP, J.G. Biosecurity issues associated with current and emerging embryo technologies. Reproduction, Fertility and Development , v.16, n.1-2, p.93-102, 2004.; Palazzi et al., 2012PALAZZI, E.G; GONÇALVES, F.R.; HANSEN, D.; FELICIO, J.D.; ALMEIDA, M.L.; ALVES, M.F.; NOGUEIRA, A.H.C.; STURARO, L.G.R.; PITUCO, E.M.; PAVÃO, D.L.; D'ANGELO, M. Evaluation of Pomegranate (Punica granatum) as replication inhibitor of BoHV-1 Colorado strain of experimentally infected murine zygotes. In: XXIII BRAZILIAN CONGRESS OF VIROLOGY & VII MERCOSUR MEETING OF VIROLOGY, 2012, Foz do Iguaçu. v. 17, n. 2, Foz do Iguaçu: 2012. p.394.). Justifica-se, portanto, a pesquisa em busca de novos meios de controle sanitário através de agentes antivirais com possível ação intra e extracelular.
Para os testes com antivirais, foram escolhidos embriões murinos, pois se apresentam como um modelo de alta confiabilidade segundo inúmeros trabalhos (Mallek et al., 1984MALLEK, Z.; GUERIN, B.; NIBART, M.; PAREZ, M.; THIBIER, M. Conséquences de la contamination in vitro des embryons de souris et de vaches par B. abortus . Bulletin de l'Académie Veterinari de France , v.57, p.479-490, 1984.; Nagy et al., 2003NAGY A, GERTSENSTEIN M, VINTERSTEN K, BEHRINGER R.. Manipulating the mouse embryo : a laboratory manual New York: 3th Ed Cold Spring Harbor Laboratory Press, 2003. p.251-273.; Palazzi et al., 2009PALAZZI, E.G.; GOES, A.C; PICCOLOMINI, M.M.; PAVÃO, D.L.; BATISTA, M.L.; ALVES, M.F.; D'ANGELO, M. Avaliação da taxa de clivagem em zigotos murinos infectados, experimentalmente, com o vírus da Rinotraqueíte Infecciosa Bovina (BoHV-1), amostra Colorado. SBM in Foco , n.9, p.132, 2009.; Palazzi, 2010PALAZZI, E.G. Efetividade da tripsina sobre embriões murinos infectados experimentalmente com BoHV-1 . 2010. 77f. Dissertação (Mestrado em Biotecnologia) - Instituto de Ciências Biomédicas, Universidade de São Paulo, São Paulo, 2010.) além de serem sensíveis ao BoHV-1, de fácil acesso e baixo custo (Galuppo, 2002GALUPPO, A.G.; D'ANGELO, M.; PIATTI, R.M; BARRA, S.H.C.; GONÇALVES, R.F. Detection of bovine herpesvirus type 1 (BHV-1) in experiments with in vitro-infected murine zygotes by the Nested-PCR technique. Theriogenology , v.57, p.571, 2002.).
Zhang et al. (1995ZHANG, J.; ZHAN, B.; YAO, X.; GAO, Y.; SHONG J. Antiviral activity of tannin from the pericarp of Punica granatum L. against genital Herpes virus in vitro . Zhongguo Zhong Yao Za Zhi , v.20, n.9, p.556-558, 1995.) verificaram que o extrato da casca de Púnica granatum mostrou ação contra o Herpes simplex vírus humano 1 e 2 in vitro . Jadhav et al. (2012JADHAV, P.; KAPOOR, N.; THOMAS, B.; LAL, H.; KSHIRSAGAR, N. Antiviral potential of selected Indian medicinal (ayurvedic) plants against herpes simplex virus 1 and 2. North American Journal of Medical Sciences, v.4, n.12, p.641-647, 2012.) pesquisaram inúmeras plantas, como Azadirachta indica, Curcuma longa (açafrão da família do gengibre), Punica granatum (romã), Ocimum sanctum, Nyctanthes arbortristis , Carica papaya (mamão) e Holarrhena antidysentrica . Todas provenientes de Gujarat, estado da Índia. Foram obtidos 24 extratos, sendo que apenas 5 indicaram ação contra o herpesvírus. Segundo a pesquisa, o pó liofilizado de Punica grantum exibiu atividade antiviral promissora. Porém, não existe nenhuma pesquisa com foco em células reprodutivas proveniente da PIV.
Dados de nossa pesquisa indicam também que o extrato etanólico do pericarpo de Punica granatum mostrou ação contra o herpesvírus bovino tipo 1 ao reduzir a replicação viral. Não houve bloqueio total, pois o resultado da n-PCR acusou a presença da partícula viral nos grupos testes, G4 (Fig. 8), e foi detectado ECP em células MDBK (Fig. 7), no entanto, de forma moderada. Provavelmente encontramos todos os embriões dos grupos que foram submetidos ao BoHV-1 Colorado positivo pela n-PCRdevido ao alto título intencionalmente usado (108 TCID50/mL). Segundo Stringfellow et al. (2004STRINGFELLOW, D.A.; GIVENS, M.D.; WALDROP, J.G. Biosecurity issues associated with current and emerging embryo technologies. Reproduction, Fertility and Development , v.16, n.1-2, p.93-102, 2004.), há a necessidade de que os títulos virais, in vitro ,estejam em altas concentrações para promover máxima oportunidade de adsorção vírus-células. Mesmo assim, a titulação demonstrou uma queda de partículas virais: a média das 4 titulações do grupo G2 foi de 3,70x107 TCID50/mL, enquanto a do grupo G4 foi de 6,51x102, demonstrando diferença significativa entre os grupos G2 e G4, segundo teste estatístico Mann-Whitney (p=0,02; α=5%). Outro fator importante é que não encontramos diferença significativa na taxa de clivagem relativa aos grupos G1 (controle) e G4 (teste) segundo teste exato de Fisher (p=0,92; α=5%). Resultados favoráveis, também, foram observados em relação à morfologia por microscopia óptica, onde não observamos alterações morfológicas no grupo teste, G4 (Figs. 4 e 5), quando comparado ao grupo controle, G1 (Fig. 1), e grupo exposto aos vírus, G2 (Fig. 2).
Os resultados de MET demonstraram que todos os embriões murinos que passaram pelos tratamentos com extratos não romperam a zona pelúcida (ZP) e mantiveram suas estruturas conservadas (Figs. 9,10, 11, 13, 14 e 15). Foi possível encontrar somente partículas virais por MET no grupo G2 (Fig. 12), o que não significa que não havia vírus no grupo G4, conforme resultados de cocultivo e titulação que demonstraram presença de vírus viável, apesar de também indicarem a redução da taxa viral do BoHV-1. Os embriões expostos aos vírus apresentaram "pertubações" na membrana plasmática (MP), provavelmente pela ação viral (Figs. 14 e 15). Essa deformação presente na MP dos embriões murinos pode estar relacionada à liberação das partículas virais por exocitose (Wild et al., 2002WILD, P.; SCHRANER, E.M.; CANTIENI, D.; LOEPFE, E.; WALTHER, P.; MÜLLER, M.; ENGELS, M. The significance of the Golgi complex in envelopment of bovine herpesvirus 1 (BHV-1) as revealed by cryobased electron microscopy, Micron , v.33, n.4, p.327-337, 2002.) ou por interferir em mecanismos relacionados ao equilíbrio da MP e da célula, como a proteína quinase dependente de cálcio (CaMK), que é um importante sinalizador celular (Miyake; Mcneil, 1995MIYAKE, K.; MCNEIL, P.L. Vesicle accumulation and exocytosis at sites of plasma membrane disruption. Journal of Cell Biology , v.131, n.6, pt.2, p. 1737-1745, 1995.; Silva et al., 2009SILVA, B.V.; HORTA, B.A.C.; ALECASTRO, R.B.; PINTO, A.C. Proteínas quinases: características estruturais e inibidores químicos. Química Nova , v.32, n.2, p.453-462, 2009. Disponível em: <Disponível em: http://www.scielo.br/scielo.php?script=sci_arttext&pid=S0100-40422009000200032&lng=en&nrm=iso
>. Acesso em: 15 fev. 2014.
http://www.scielo.br/scielo.php?script=s...
).
Todos estes dados, analisados em conjunto, refletem a redução das partículas virais pela ação do extrato ao compararmos com o grupo exposto aos vírus e não tratado com EEPg, permitindo, desta forma, o desenvolvimento do embrião. Cabe destacar que esclarecimentos da(s) molécula(s) envolvidas do EEPg são necessários para potencializar a ação e o entendimento desse efeito com futuros trabalhos. Além disso, salientamos que os experimentos foram realizados in vitro , por isso não contamos, evidentemente, com mecanismos in vivo como disposição tecidual, sistema imunológico, entre outros. Por isso, consideramos sempre que a transposição de sistemas in vitro para in vivo exige cautela(D´Angelo, 1998D'ANGELO, M. Interação do herpesvirus bovino tipo-1 (BoHV-1) com oócitos bovinos maturados in vitro. 1998. 52f. Tese (Doutorado em Microbiologia) - Departamento de Microbiologia do Instituto de Ciências Biomédicas, Universidade de São Paulo, São Paulo, 1998.).
Mesmo com as últimas ponderações, consideramos que o EEPg demonstra resultados promissores para uso em protocolos de FIV de bovinos por diminuir, significativamente, a replicação viral e, ao mesmo tempo, permitir o pleno desenvolvimento dos embriões murinos.
Agradecimentos
Ao Dr. Ricardo S. Jordão pela essencial ajuda ao ceder espaço e todo suporte no biotério, e ao apoio financeiro imprescindível do Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq) do Brasil.
REFERÊNCIAS
- ATHAYDE, C.S. Interação do parvovírus suíno com oócitos suínos durante o período de maturação in vitro. 2007. 52f. Dissertação (Mestrado em Biotecnologia) - Instituto de Ciências Biomédicas, Universidade de São Paulo, São Paulo, 2007.
- CERQUEIRA, R.B.; CARMINATI, R.; SILVA, J.M.; SOARES, G.C.; MEYER, R.; SARDI, S. Serological survey for bovine herpesvirus 1 in cattle from different regions in the state of Bahia, Brazil. Brazilian Journal of Veterinary Research and Animal Science , v.37, n.6, p.1-8, 2000.
- COLODEL, E.M.; NAKAZATO, L.; WEIBLEN, R.; MELLO, R.M.; SILVA, R.R.P.; SOUZA, M.A.; OLIVEIRA FILHO, J.A.; CARON, L. Meningoencefalite necrosante em bovinos causada por herpesvírus bovino no Estado de Mato Grosso, Brasil. Ciência Rural , v.32, n.2, p.293-298, 2002.
- D'ANGELO, M. Interação do herpesvirus bovino tipo-1 (BoHV-1) com oócitos bovinos maturados in vitro. 1998. 52f. Tese (Doutorado em Microbiologia) - Departamento de Microbiologia do Instituto de Ciências Biomédicas, Universidade de São Paulo, São Paulo, 1998.
- GALUPPO, A.G.; D'ANGELO, M.; PIATTI, R.M; BARRA, S.H.C.; GONÇALVES, R.F. Detection of bovine herpesvirus type 1 (BHV-1) in experiments with in vitro-infected murine zygotes by the Nested-PCR technique. Theriogenology , v.57, p.571, 2002.
- GALUPPO, A.G. Avaliação da sensibilidade de zigotos murinos à Brucella abortus para o estabelecimento de um modelo experimental em estudos de interações embriões-patógenos 2005. 74 f. Dissertação (Mestrado em Epidemiologia Experimental e Aplicada à Zoonozes) - Faculdade de Medicina Veterinária e Zootecnia, Universidade de São Paulo, São Paulo, 2005.
- HOGAN, B.; CONSTANTINI, F.; LACY, E. Developmental genetics and embryology of the mouse: past, present, and future. In: HOGAN, B.; CONSTANTINI, F.; LACY, E. (Eds.). Manipulating the mouse embryo : a laboratory manual. Cold Spring Harbor: Cold Spring Harbor Laboratory, 1986. p.12-14.
- JADHAV, P.; KAPOOR, N.; THOMAS, B.; LAL, H.; KSHIRSAGAR, N. Antiviral potential of selected Indian medicinal (ayurvedic) plants against herpes simplex virus 1 and 2. North American Journal of Medical Sciences, v.4, n.12, p.641-647, 2012.
- KNUTTON, S. Electron microscopical methods in adhesion. Methods in Enzymology , v.253, p.145-158, 1995.
- KUNRATH, C.F.; VOGEL, F.S.F.; OLDONI, I.; FLORES, E.F.; WEIBLEN, R.; DEZENGRINI, R.; TORRES, F.D.; PAN, K.A. Soroneutralização e imunofluorescência utilizando anticorpos monoclonais no diagnóstico rápido de infecções pelo herpesvírus bovino tipos 1 e 5 (BHV-1 e BHV-5). Ciência Rural , v.34, n.6, p.1877-1883, 2004.
- LORENZI, H.; MATOS, F.J.A. Punica granatum L. In: LORENZI, H.; MATOS, F.J.A. Plantas medicinais no Brasil : nativas e exóticas. Nova Odessa: Instituto Plantarum de Estudo da Flora Ltda, 2002. p.394-395.
- MALLEK, Z.; GUERIN, B.; NIBART, M.; PAREZ, M.; THIBIER, M. Conséquences de la contamination in vitro des embryons de souris et de vaches par B. abortus . Bulletin de l'Académie Veterinari de France , v.57, p.479-490, 1984.
- MIYAKE, K.; MCNEIL, P.L. Vesicle accumulation and exocytosis at sites of plasma membrane disruption. Journal of Cell Biology , v.131, n.6, pt.2, p. 1737-1745, 1995.
- NAGY A, GERTSENSTEIN M, VINTERSTEN K, BEHRINGER R.. Manipulating the mouse embryo : a laboratory manual New York: 3th Ed Cold Spring Harbor Laboratory Press, 2003. p.251-273.
- PALAZZI, E.G.; GOES, A.C; PICCOLOMINI, M.M.; PAVÃO, D.L.; BATISTA, M.L.; ALVES, M.F.; D'ANGELO, M. Avaliação da taxa de clivagem em zigotos murinos infectados, experimentalmente, com o vírus da Rinotraqueíte Infecciosa Bovina (BoHV-1), amostra Colorado. SBM in Foco , n.9, p.132, 2009.
- PALAZZI, E.G; GONÇALVES, F.R.; HANSEN, D.; FELICIO, J.D.; ALMEIDA, M.L.; ALVES, M.F.; NOGUEIRA, A.H.C.; STURARO, L.G.R.; PITUCO, E.M.; PAVÃO, D.L.; D'ANGELO, M. Evaluation of Pomegranate (Punica granatum) as replication inhibitor of BoHV-1 Colorado strain of experimentally infected murine zygotes. In: XXIII BRAZILIAN CONGRESS OF VIROLOGY & VII MERCOSUR MEETING OF VIROLOGY, 2012, Foz do Iguaçu. v. 17, n. 2, Foz do Iguaçu: 2012. p.394.
- PALAZZI, E.G. Efetividade da tripsina sobre embriões murinos infectados experimentalmente com BoHV-1 . 2010. 77f. Dissertação (Mestrado em Biotecnologia) - Instituto de Ciências Biomédicas, Universidade de São Paulo, São Paulo, 2010.
- REED, L.J.; MUENCH, H. A simple method of estimating fifty per cent endpoints. American Journal of Hygiene , v.27, n.3, p.493-497, 1938.
- SILVA, B.V.; HORTA, B.A.C.; ALECASTRO, R.B.; PINTO, A.C. Proteínas quinases: características estruturais e inibidores químicos. Química Nova , v.32, n.2, p.453-462, 2009. Disponível em: <Disponível em: http://www.scielo.br/scielo.php?script=sci_arttext&pid=S0100-40422009000200032&lng=en&nrm=iso >. Acesso em: 15 fev. 2014.
» http://www.scielo.br/scielo.php?script=sci_arttext&pid=S0100-40422009000200032&lng=en&nrm=iso - SOUSA, M.P.; MATOS, F.J.A.; MATOS, M.E.O.; MACHADO, M.I.L.; CRAVEIRO, A.A. Constituintes químicos ativos e propriedades biológicas de plantas medicinais brasileiras . Fortaleza: UFC, 1991. 416p.
- SINGH, E.L.; THOMAS, F.C.; PAPP-VID, G.; EAGLESOME, M.D.; HARE, W.C. Embryo transfer as a means of controlling the transmission of viral infections II: the in vitro exposure of preimplantation bovine embryos to infectious bovine rhinotracheitis virus. Theriogenology , v.18, n.2, p.133-140, 1982.
- STRINGFELLOW, D.A.; LAUERMAN, L.H.; NASTI, K.B.; GALIK, P.K. Trypsin treatment of bovine embryos after in vitro exposure to infectious bovine rhinotacheitis virus or bovine herpes virus-4. Theriogenology v.34, n.3, p.427-434, 1990.
- STRINGFELLOW, D.A.; GIVENS, M.D. epidemiologic concerns relative to in vivo and in vitro production of livestock embryos. Animal Reproduction Science , v.60-61, p.629-642, 2000.
- STRINGFELLOW, D.A.; GIVENS, M.D.; WALDROP, J.G. Biosecurity issues associated with current and emerging embryo technologies. Reproduction, Fertility and Development , v.16, n.1-2, p.93-102, 2004.
- VIEIRA, S.; BRITO, W.M.E.D.; SOUZA, W.J.; ALFAIA, B.T.; LINHARES, D.C.L. Anticorpos para o herpesvírus bovino 1 (BHV-1) em bovinos do Estado de Goiás. Ciência Animal Brasileira , v.4, n.2, p.131-137, 2003.
- WILD, P.; SCHRANER, E.M.; CANTIENI, D.; LOEPFE, E.; WALTHER, P.; MÜLLER, M.; ENGELS, M. The significance of the Golgi complex in envelopment of bovine herpesvirus 1 (BHV-1) as revealed by cryobased electron microscopy, Micron , v.33, n.4, p.327-337, 2002.
- WHITBECK, J.C.; BELLO, L.J.; LAWRENCE, W.C. Comparison of the bovine herpesvirus 1 gI gene and the herpes simplex virus type 1gB gene. Journal of Virology , v.62, n.9, p.3319-3327, 1988.
- ZHANG, J.; ZHAN, B.; YAO, X.; GAO, Y.; SHONG J. Antiviral activity of tannin from the pericarp of Punica granatum L. against genital Herpes virus in vitro . Zhongguo Zhong Yao Za Zhi , v.20, n.9, p.556-558, 1995.
-
**
Parte da tese de doutoramento do primeiro autor realizado junto ao Programa de Pós-Graduação Interunidades em Biotecnologia da Universidade de São Paulo.
Datas de Publicação
-
Publicação nesta coleção
2015
Histórico
-
Recebido
24 Set 2013 -
Aceito
20 Mar 2015